- Characteristics Control of Phytoncide-containing Copoly(Styrene-Acrylic Acid) Nanoparticles by Layer-by-Layer Assembly Method
Department of Textile System Engineering, Kyungpook National Univertsity, 80 Daehak-ro, Puk-gu, Daegu 41566, Korea
*Department of Carbon Fusion New Material, Korea Polythecnics, 222 Palgong-ro, Dong-gu, Daegu 41027, Korea- 다중박막적층법을 이용한 피톤치드 담지 Copoly(Styrene-Acrylic Acid) 나노입자의 특성 제어
경북대학교 섬유시스템공학과, *한국폴리텍대학 탄소융합신소재과
Reproduction, stored in a retrieval system, or transmitted in any form of any part of this publication is permitted only by written permission from the Polymer Society of Korea.
Mean particle size, colloidal stability, and release profile of copoly(styrene-acrylic acid) nanoparticles were controlled by layer-by-layer (LbL) assembly method using chitosan (CS) and carboxy methylcellulose (CMC) aqueous solutions. From FTIR analysis, successful layer assembly of CS and CMC was confirmed. Optimum conditions of LbL assembly was also confirmed by scanning electro microscopy (SEM) and particle size analyzer (PSA) analyses. Colloidal stability was evaluated by measuring zeta potential of particles. Release profile of core material (phytoncide oil) was measured by using UV-Vis spectrophotometer and high performance liquid chromatography (HPLC). (St-AA)NP prepared by miniemulsion copolymerization shows mean particle size and zeta potential of 351.0 nm and -39.77 mV, respectively. Mean particle size of LbL assembled particles can be controlled from 351 nm to 2,803 nm by optimization of LbL assembly conditions. Zeta potential values above ±40 mV evidence the coilloidal stability of particles. LbL assembled particles show controlled release profiles of phytoncide oil over 2 months.
다중박막적층법(LbL)을 이용하여 copoly(styrene-acrylic acid) 나노입자((St-AA)NP)의 입경, 분산안정성 및 방출거동을 제어하였다. LbL 적층에는 키토산(CS)과 카르복시 메틸셀룰로오스(CMC) 수용액이 사용되었으며, FTIR을 통해 박막적층이 성공적으로 이루어졌음을 확인하였다. 주사전자현미경(SEM)과 입도분석기(PSA) 분석을 통해 LbL 최적 조건 또한 결정되었다. 분산안정성은 입자의 제타전위 변화를 통해 확인하였으며, 심물질로 피톤치드 오일을 사용하고 UV-Vis 분광분석기 및 고성능 액체 크로마토그래피(HPLC) 분석을 통해 방출거동을 평가하였다. (St-AA)NP는 351.0 nm의 평균 입경과 -39.77 mV의 제타전위를 가지며, LbL 박막적층에 의해 평균 입경을 351-2803 nm 범위에서 조절하였다. 제타전위는 ±40 mV 이상의 값을 나타내어 분산안정성을 확보하였다. 심물질의 방출 또한 2개월 이상의 기간에 대해 균일한 누적 방출 특성을 보이도록 제어하였다.
Layer-by-layer assembly of copoly(styrene-acrylic acid) nanoparticles ((St-AA)NP) was conducted by using chitosan (CS) and carboxy methylcellulose (CMC) as stacking polymers. Colloidal stability of particles was confirmed by zeta potential of above ¡¾40 mV. Suspended release of phytoncide oil from particles was also confirmed.
Keywords: layer-by-layer assembly method, zeta potential, miniemulsion copolymerization, ccolloidal stability, suspended release.
이 논문은 2021년도 정부(산업통상자원부)의 제원으로 한국산업기술진흥원의 지원을 받아 수행된 연구임 (P0017002, 2021년 산업혁신인재성장지원사업).
저자들은 이해상충이 없음을 선언합니다.
기능성 물질을 담지한 고분자 나노입자는 담지물에 대한 외부 환경으로부터의 보호와 서방성의 특성을 나타내기 때문에 유효 기능의 장기간 발현이라는 장점을 가지고 있어 약물전달체계,1-5 조직공학,6-9 bone cement10-13 등의 의료분야 뿐 아니라 기능성 목재,14 건축재료,15,16 섬유가공제17-20 등으로도 활발한 응용이 이루어지고 있다. 그러나 나노입자는 콜로이드 상태에서의 번한 입자간 회합에 의해 분산성이 낮다는 문제점을 가지고 있다. 많은 연구자들이 나노입자의 분산성을 높이기 위한 다양한 연구를 시도하였는데, Kowalczyk와 Kaminska는21 폴리에스터 직물에 ZnO와 AgCu 나노입자를 도입하면서 나노입자의 분산성에 미치는 pH, 계면활성제 및 전해질의 영향에 대해 보고하였다. 이들은 제타전위를 통한 나노입자 분산성 예측의 타당성을 제시하였는데, 이는 zein 나노입자의 콜로이드 분산안정성에 대해 보고한 Yu 등의 연구결과에서도22 확인할 수 있다. 또한 Salazar-Bryam 등은23 인지질을 계면활성제로 사용하여 은 나노입자의 분산안정성을 향상시키고자 하였으며, pH의 영향에 따른 제타전위의 변화를 분산안정성의 기준으로 제시하였다. 이 밖에도 많은 연구자들이 제타전위의 증가를 근거로 나노입자의 분산안정성 확보를 보고한 바 있다.24-31 특히 Pochapski 등은32 제타전위와 콜로이드 분산안정성의 상관관계를 실험 조건과 동역학 측면에서 이론적으로 설명하였는데, 제타전위가 ±30 mV에서 ±40 mV 사이인 경우를 적당한 정전기적 안정(moderate electrostatic stability)으로 명명하였으며, ±40 mV 이상의 제타전위를 갖는 경우에 대해 나노입자가 높은 수준의 분산안정성을 갖는 정전기적 안정상태에 있다고 규정하였다.
다중박막적층법(layer-by-layer (LbL) assembly method)은 층과 층 사이의 물질들에 대해, 정전기적 인력, 수소결합 또는 공유결합 등의 인력을 작용하여 연속되는 양과 음의 상반되는 인력의 물질들을 수용액 환경에서 교대로 흡착시켜 제조하는 방법으로, 보통 특정 기판에 대해 연속적으로 박막을 형성하는 것을 의미한다. 침지법이나 스프레이법과 같이 제조가 용이하고, 공정이 단순하며, 사용하는 물질 및 인력에 따라 박막의 두께와 같은 표면특성을 조절할 수 있다는 장점이 있다.33 LbL에 의해 구성된 박막층은 구조적으로 매우 안정하며, 박막이 형성되는 기질의 크기나 형태와 관계없이 다층초박막을 형성할 수 있어서 광학필름, 약물전달체계, 디스플레이, 바이오센서 등 다양한 분야에서 활용되고 있다.34 특히 LbL은 나노입자의 표면에 대해 적용하는 것도 가능한데, 많은 연구자들이 금속35-38 및 고분자39-42 나노입자의 표면에 정전기적 인력을 이용하여 다중박막을 유도함으로 입자의 회합을 방해하고 분산안정성을 확보하는 연구를 보고한 바 있다.
섬유 제품의 방향가공에 사용되는 기존 폴리스티렌 나노입자는 낮은 정전기적 반발력으로 인해 분산안정성이 부족하고, 이로 인한 입자 간 회합, 노즐 막힘, 침전물 생성 등의 문제가 발생하고 있다. 또한 나노입자의 벽체가 brittle하다는 점 때문에 물리적 확산에 의한 서방성보다는 나노입자의 벽체 파괴에 따른 단기 성능 발현의 문제점도 가지고 있다. 본 연구에서는 미니에멀전 중합을 통해 섬유 제품의 방향가공에 적용하기 위한 피톤치드 오일을 담지한 스티렌(styrene, St)-아크릴산(acrylic acid, AA) 공중합 나노입자(copoly(St-AA) nanoparticle, (St-AA)NP)를 제조하고, 양전하를 갖는 키토산 (chitosan, CS) 수용액과 음전하를 띄는 카복시메틸 셀룰로오스(carboxy methylcellulose, CMC) 수용액을 이용하여 LbL 박막적층을 시도함으로서 나노입자의 분산안정성과 방출성을 제어하고자 하였다.
시약 및 재료. 단량체인 St(Aldrich Chem., USA, 1급) 및 AA(Aldrich Chem., USA, 1급)은 정제를 통해 중합금지제를 제거한 후 사용하였다. Sodium dodecyl sulfate(SDS, Daejung Chem., Korea, 1급), n-Hexane(Alfa Aesar, UK, 1급), Divinyl benzene(DVB, Aldrich Chem., USA, 1급) 및 2,2-azobisisobutyronitrile (AIBN, Junsei, Japan, 1급)은 각각 미니에멀전 중합을 위한 계면활성제, 공계면활성제, 가교제 및 개시제로 사용되었다. 각각 양전하와 음전하를 갖는 고분자인 CS(Chitosan 100, Wako, Japan, 1급)와 CMC(Duksan Chem., Korea, 1급)은 LbL 박막적층에 적용되었다. 심물질은 피톤치드 오일을 사용하였으며, ㈜씨앤지(Daegu, Korea)에서 제공받아 사용하였다. 이 밖의 용매류는 모두 시약 1급이었으며, 모든 실험 과정에서 2차 증류수(Milli-Q plus, Millipore, France)를 사용하였다.
미니에멀젼 공중합을 통한(St-AA)NP 합성. (St-AA)NP의 합성은 이미 보고된 선행연구의 최적 조건을31 이용하였다. 1.0×10-3 mol의 SDS를 80 mL의 증류수에 60 ℃에서 1시간 동안 300 rpm으로 교반하면서 용해시켰다(A용액). 단량체 (0.172 mol, [AA]/[St]=0.33), 피톤치드 오일(10 g), DVB(250 mg) 및 n-Hexane(450 mg)을 상온에서 1시간 동안 300 rpm으로 교반하여 B용액을 준비하였다. B용액을 A용액에 적가한 후, 균질화기(T25 digital Ultra Turrax, IKA, Germany)를 이용하여 상온에서 19000 rpm으로 10분간 유화하였다. 이후 3-neck 둥근 플라스크에 환류냉각기와 질소관을 설치하고, 반응조 내의 수분 및 불순물을 제거하기 위하여 1시간 동안 질소 환경에서 degassing을 실시하였다. 반응 온도인 60 ℃로 승온한 이후, 개시제인 AIBN(2.0×10-3 mol/mol of monomer)을 투입하고 5시간 동안 중합을 진행하였다. 제조된 (St-AA)NP는 메탄올 침전, 필터링과 수세를 3회 반복한 후, 80 mL 증류수에 대한 수분산 상태로 보관하였다.
(St-AA)NP 박막적층. 양이온성 박막적층을 위해 증류수 80 mL에 아세트산 0.8 g을 용해시키고 정해진 양의 CS(0.3, 0.5, 0.7, 1.0 wt%)를 첨가한 다음, 60 ℃에서 1시간 동안 300 rpm으로 교반하여 CS 수용액을 제조하였다. CS 수용액에 당량의 (St-AA)NP 수분산액을 첨가한 후, 60 ℃에서 4시간 동안 300 rpm으로 교반하면서 박막을 형성하였다. 에탄올 침지 후 필터링과 수세를 3회 반복하여 미반응 CS를 제거하였다. 제조된 [(St-AA)NP]@CS 캡슐은 필터칭 후 24시간 건조하였다.
음이온 박막적층을 위한 CMC 수용액 제조를 위해 증류수 80 mL에 NaOH 0.8 g을 용해한 후, 정해진 양의 CMC(0.3, 0.5, 0.7, 1.0 wt%)를 투입하여 50 ℃에서 1시간 동안 300 rpm으로 교반하였다. 증류수 80 mL에 [(St-AA)NP]@CS 캡슐을 분산시킨 후, 두 용액을 혼합하여 60 ℃에서 4시간 동안 300 rpm으로 교반하면서 박막을 형성하였다. 에탄올 침지 후 필터링과 수세를 3회 반복하여 미반응 CMC를 제거하였다. 제조된 [[(St-AA)NP]@CS]@CMC 캡슐은 필터링 후 24시간 건조하였다. 상기 과정의 반복을 통해(St-AA)NP에 대한 LbL 박막적층을 진행하였다.
특성해석. 나노입자 및 마이크로캡슐의 크기와 외관은 주사전자현미경(scanning electro microscopy, SEM, SU8220, Hitachi, Japan)을 이용하여 분석하였다. 나노입자 및 마이크로캡슐의 평균 입도와 제타전위는 10 mW 수직 편광 He-Ne 레이저가 장착된 입도분석기(particle size analyzer, PSA, EL8000, Photal Otsuka Electronics, Japan)를 통해 상온에서 평가되었다. 심물질의 방출거동은 에탄올 분산액에 대해 2개월간 UV-Vis 분광분석기(Lambda 265, Perkin Elmer, USA)와 고성능 액체 크로마토그래피(high performance liquid chromatography, HPLC, Prominence, Shimadzu, Japan)를 통해 확인하였다. 총 담지량 평가는 22,000 rpm에서 30분간 원심분리 후 HPLC를 측정하여 분석하였다. LbL 박막적층된 마이크로캡슐의 구조는 푸리에 변환 적외선 분광법(Fourier transform infrared spectroscopy FTIR, Frontier, Perkin Elmer, USA)을 통해 확인하였다.
[(St-AA)NP]@CS(no. of LbL cycle: 1). Figure 1은 CS, (St-AA)NP 및 [(St-AA)NP]@CS의 FTIR 스펙트럼을 나타낸 것이다. FTIR 분석에 사용된[(St-AA)NP]@CS는 0.7 wt%의 CS 수용액에서 제조되었다. CS의 특성 피크는 N-H 신축진동(3250-3400 cm-1)과 C-O 신축진동(1026 cm-1)에서 확인할 수 있다. (St-AA)NP와 달리[(St-AA)NP]@CS에서는 CS의 특성 피크가 발현되는 것으로부터 CS 박막이 형성되었음을 확인하였다.
CS의 농도에 따른[(St-AA)NP]@CS의 외관을 Figure 2에서 보였다. CS 농도가 0.7 wt% 이하인 경우에는 비교적 균일한 표면을 갖는 [(St-AA)NP]@CS가 형성되었으나, CS 농도가 1.0 wt%인 경우, 과량의 CS로 인해 입자간 회합이 일어나는 것을 확인할 수 있다. 이는 Table 1에서 보인[(St-AA)NP]@CS의 CS 농도에 따른 입도와 제타전위 변화에서도 확인할 수 있다. 박막적층 이전의 (St-AA)NP는 351.0 nm의 평균 입경을 나타내었으며, CS의 적층에 따라 입경이 증가하는 것을 확인할 수 있다. CS의 농도가 0.3-0.7 wt%의 범위인 경우 580-685 nm의 크기를 나타내는 데 반해, 1.0 wt%에서는 1120 nm 이상의 급격한 입경 증가를 나타내어 입자간 회합에 의한 평균 입경의 증가가 이루어짐을 알 수 있다. AA에 의해 -39.77 mV의 제타전위를 갖는 (St-AA)NP는 양전하를 갖는 CS의 적층에 의해 제타전위가 양의 값으로 전환됨을 확인할 수 있었는데, CS 농도 0.3 wt%인 경우는 매우 미약한 제타전위를 나타내는 반면, 0.5-1.0 wt%에서는 +40 mV 이상의 제타전위를 나타내어 Pochapski 등이32 규정한 높은 수준의 분산안정성을 확보하였음을 확인하였다. 제타전위는 CS 농도 0.7 wt%에서 가장 높은 값인 +52.10 mV를 나타내었으며, 1.0 wt%에서는 도리어 감소하는 경향을 나타내었다. 이는 높은 CS 농도로 인해 입자간 회합이 발생하기 때문으로 추정되며, [(St-AA)NP]@CS의 최적 제조는 CS 농도 0.7 wt%에서 가능한 것으로 판단되었다.
[[(St-AA)NP]@CS]@CMC (no. of LbL cycle: 2). Figure 3은 [(St-AA)NP]@CMC, [[(St-AA)NP]@CS]@CMC 및 CMC의 FTIR 스펙트럼을 나타낸 것이다. FTIR 분석에 사용된 [[(St-AA)NP]@CS]@CMC는 0.5 wt%의 CMC 수용액에서 제조되었다. CMC의 O-H 신축진동은 3300 cm-1 부근에서 폭 넓게 나타나고 있으며, C-O 단일결합 신축진동은 1000-1100 cm-1 부근에서 나타난다. 이들 특성 피크는 [(St-AA)NP]@CS에서도 동일하게 나타나지만, 피크의 강도가 증가한다는 점에서 CMC 박막이 형성되었음을 예측할 수 있었다. 이와 같은 예측은 Table 2에서 보이는 제타전위의 변화에서 타당성을 확인할 수 있었는데, +52.10 mV의 제타전위를 가지고 있는 [(St-AA)NP]@CMC에 대해 음전하를 갖는 CMC를 적층함에 따라 음의 제타전위 값으로 전환됨을 통해 검증하였다. CMC 농도가 0.3 wt%인 경우에는 -27.55 mV의 제타전위를 나타내어 분산안정성이 부족하였으며, CMC 농도가 0.5-1.0 wt%인 경우에는 -40 mV 이상의 제타전위 값을 나타내어 높은 수준의 분산안정성을 확보하였음을 확인하였다. CMC 농도에 따른 [[(St-AA)NP]@CS]@CMC의 평균 입경은 CMC 농도가 증가함에 따라 929 nm에서 1636 nm까지 증가하여 마이크로캡슐의 범위에 해당하였으며, 이는 적층되는 CMC 층이 농도 증가에 따라 두터워지기 때문으로 예상되었다.
CMC의 농도에 따른 [[(St-AA)NP]@CS]@CMC의 외관을 Figure 4에 보였다. CMC 농도가 0.5 wt% 이하인 경우에는 비교적 균일한 표면을 갖는 [[(St-AA)NP]@CS]@CMC가 형성되었으나, CMC 농도가 0.7 및 1.0 wt%인 경우, 과량의 CMC로 인해 입자간 회합이 일어나는 것을 확인할 수 있었다. 상기 결과로부터 [[(St-AA)NP]@CS]@CMC의 최적 제조는 CMC 농도 0.5 wt%에서 가능한 것으로 판단되었다.
LbL 박막적층. [[(St-AA)NP]@CS]@CMC에 대해 CS 및 CMC 수용액에 대한 LbL 박막적층을 순차적으로 시행하였으며, 각각의 시료를 Layer3(no. of LbL cycle: 3) 및 Layer4 (no. of LbL cycle: 4)로 표기하였다. Layer3은 0.5 wt%의 CMC로 박막적층된 [[(St-AA)NP]@CS]@CMC에 대한 CS 적층을 보인 것이며, Layer4는 0.5 wt%의 CS로 적층된 Layer3에 대해 CMC로 적층하였다. Figure 5는 박막적층에 사용된 CS 농도에 따른 Layer3의 외관을 보인 것이다. CS 농도가 0.3 및 0.5 wt%인 경우에는 상대적으로 입자의 표면이 균일하고 응집이 발생하지 않았으나, 0.7 wt% 이상의 CS 농도에서는 급격한 입자 간 회합이 발생하였다. Layer4의 경우에도 CMC 농도가 0.7 wt% 이상인 경우에서 급격한 입자간 회합이 발생하였으며, 이는 다음의 Figure 6에서 확인할 수 있다.
Table 3에서 Layer3와 Layer4 시료에 대해 각각 CS 및 CMC 농도가 평균 입도 및 제타전위에 미치는 영향을 보인 것이다. Layer3와 Layer4 모두 각각 적층되는 CS와 CMC의 농도가 증가할수록 입경이 급격히 증가하는 경향을 보였다. 제타전위는 CS와 CMC가 각각 0.3 wt%로 적용되는 경우에는 정전기적 특성의 전환은 관찰되었으나, ±30 mV 이하의 범위에 해당하여 충분한 분산안정성은 확보하지 못한 것으로 판단되었다. 0.5 wt%가 적용된 경우에는 Layer3과 Layer4 모두 ±40 mV 이상의 제타전위를 나타내어 높은 수준의 분산안정성을 나타내었다. 그러나 두 시료 모두에게서 0.7 wt% 이상의 농도로 적층하는 경우 분산안정성이 도리어 감소함을 확인할 수 있는데, 이는 Figure 5와 6에서 보인 것처럼 입자 간 회합이 증가하기 때문으로 판단되었다. Figure 7은 LbL cycle에 따른 zeta potential의 변화를 나타낸 것이다. Fig. 7
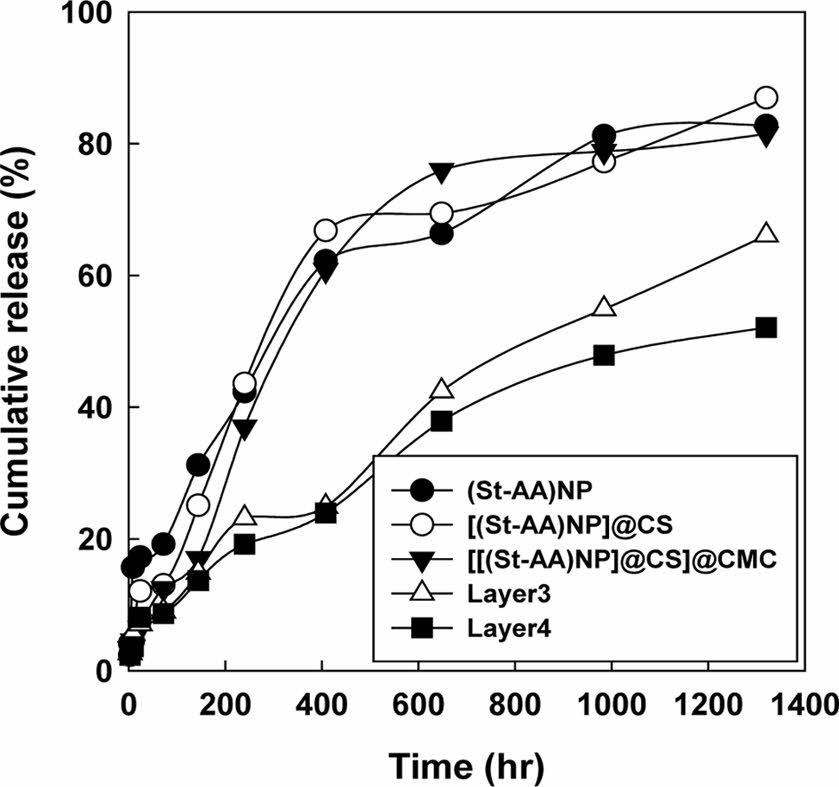
방출거동 평가. 심물질인 피톤치드 오일의 방출거동을 확인하기 위하여 UV-Vis 분광분석기를 통해 피톤치드 오일의 최대흡수파장 λmax가 229 nm임을 확인하였다. 결정된 λmax에 대해 HPLC를 이용하여 구한 검량선을 기준으로 총 담지량과 2개월간의 방출거동을 각각 Table 4와 Figure 8에 보였다. Table 4에 보인 바와 같이, (St-AA)NP의 총 담지량이 4000 ppm 이상인데 반해 LbL 박막적층된 입자들의 총 담지량은 3300-3700 ppm의 값을 나타내고 있는데, Figure 8의 방출 초기거동에서 (St-AA)NP의 급격한 방출이 감소하고 있다는 점에서 (St-AA)NP 표면에 잔존하는 피톤치드 오일이 LbL 박막적층 과정에서 제거되기 때문으로 판단되었다. (St-AA)NP, [(St-AA)NP]@CS 및 [[(St-AA)NP]@CS]@CMC의 경우, 400시간 정도까지는 급격한 방출이 이루어지지만, 그 이후로는 누적 방출량의 변화가 완만해지는 것을 확인하였으며, 이는 피톤치드 오일의 방출에 따른 기능의 저하가 발생되는 원인으로 파악되었다. Layer3와 Layer4는 2개월이 지난 뒤에도 총 담지량의 50-60%의 방출이 이루어졌으며, 누적 방출량이 일정한 속도로 증가하는 것을 확인하였다. 따라서 LbL 박막적층에 의해 심물질의 효과적인 방출 제어와 장기 성능의 향상이 가능하다고 판단되었다.

|
Figure 1 FTIR specta of (a) CS; (b) (St-AA)NP; (c) [(St-AA)NP]@CS. |

|
Figure 2 SEM photographs of [(St-AA)NP]@CS prepared at CS concentrations of (a) 0.3 wt%; (b) 0.5 wt%; (c) 0.7 wt%; (d) 1.0 wt%, respectively. |

|
Figure 3 FTIR specta of (a) CMC; (b) [(St-AA)NP]@CS; (c) [[(StAA)NP]@CS]@CMC. |

|
Figure 4 SEM images of [[(St-AA)NP]@CS]@CMC at varying CMC concentrations: (a) 0 wt%; (b) 0.3 wt%; (c) 0.5 wt%; (d) 0.7 wt%; (e) 1.0 wt%. |

|
Figure 5 SEM images of Layer3 at varying CS concentrations: (a) 0.3 wt%; (b) 0.5 wt%; (c) 0.7 wt%; (d) 1.0 wt%. |

|
Figure 6 SEM images of Layer4 at varying CMC concentrations: (a) 0.3 wt%; (b) 0.5 wt%; (c) 0.7 wt%; (d) 1.0 wt%. |

|
Figure 7 Changes in zeta potential according to the LbL cycles. |

|
Figure 8 Cumulative release profiles of phytoncide oil. |
|
Table 1 Effects of CS Concentrations on Mean Particle Size and Zeta Potential of [(St-AA)NP]@CS |

|
Table 2 Effects of CMC Concentrations on Mean Particle Size and Zeta Potential of [[(St-AA)NP]@CS]@CMC |

|
Table 3 Effects of CS and CMC Concentrations on Mean Particle Size and Zeta Potential of Layer3 and Layer4, Respectively |

본 연구에서는 (St-AA)NP의 분산안정성과 서방성을 확장하기 위하여 심물질을 피톤치드 오일로 하는 (St-AA)NP를 미니에멀전 공중합으로 제조한 뒤, CS와 CMC 수용액을 각각 양전하와 음전하를 갖는 박막 물질로 선정하고 LbL 박막적층법을 시행하여 각 입자의 제타전위, 평균 입도 및 방출성을 평가하였으며, LbL 박막적층법의 최적조건 또한 확인하였다. 이를 통해 피톤치드 오일을 담지한 기능성 입자의 평균 입경을 최적 조건 기준으로 351-2803 nm까지 조절할 수 있었으며, 제타전위 또한 ±40 mV 이상의 조건을 확립하여 매우 높은 수준의 분산안정성을 확보하였다. 다중박막이 적층됨에 따라 심물질의 방출 또한 2개월 이상의 기간에 대해 균일한 누적 방출 특성을 보이는 서방형으로 제어할 수 있었다. 본 연구를 통해 기능성 입자의 크기와 분산성 제어가 가능하고, 지속적인 방출성을 갖는 입자형 가공제의 개발이 가능할 것으로 예측되며, 다양한 분야에서의 응용이 기대된다.
- 1. Mühlen, A.; Schwarz, C.; Mehnert, W. Solid Lipid Nanoparticles (SLN) for Controlled Drug Delivery – Drug Release and Release Mechanism. Eur. J. Pharm. Biopharm. 1998, 45, 149-155.
-

- 2. Suri, G. S.; Kaur, A.; Sen, T. A Recent Trend of Drug-Nanoparticles in Suspension for the Application in Drug Delivery. Nanomedicine 2016, 11, 2861-2876.
-

- 3. Yuan, Q.; Shah, J.; Hein, S.; Misra, R. D. K. Controlled and Extended Drug Release Behavior of Chitosan-based Nanoparticle Carrier. Acta Biomater. 2010, 6, 1140-1148.
-

- 4. Park, J. H.; Kim, G.; Le, T. P.; Kim, D. H.; Seol, E.; Huh, K. M. Injectable Thermogel/Microsphere Hybrid Formulation System for Intratympanic Delivery of Dexamethasone. Polym. Korea 2023, 47, 16-25.
-

- 5. Kim, P. Y.; Jung, J. J.; Kim, N. Y.; Kim, J. W.; Choi, J. M.; Lee, W. C.; Song, J. E.; Khang, G. Dissolution Properties of Controlled Release Capsules Containing Quetiapine Fumarate. Polym. Korea 2020, 44, 715-724.
-

- 6. Godoy-Gallardo, M.; Eckhard, U.; Delgado, L. M.; Puente, Y. J. D. R.; Hoyos-Nogués, M.; Gil, F. J.; Perez, R. A. Antibacterial Approaches in Tissue Engineering Using Metal Ions and Nanoparticles: From Mechanisms to Applications. Bioactive Mater. 2021, 6, 4470-4490.
-

- 7. Ezhilarasu, H.; Vishalli, D.; Dheen, S. T.; Bay, B.; Srinivasan, D. K. Nanoparticle-Based Therapeutic Approach for Diabetic Wound Healing. Nanomaterials 2020, 10, 1234.
-

- 8. Lavanya, K.; Chandran, S. V.; Balagangadharan, K.; Selvamurugan, N. Temperature- and pH-responsive Chitosan-based Injectable Hydrogels for Bone Tissue Engineering. Mater. Sci. Eng. C 2020, 111, 110862.
-

- 9. Kim, M. S.; Park, S. J.; Gu, B. K.; Kim, C. H. Biodegradable Nanoparticles for Nanomedicines. Polym. Korea 2015, 39, 831-836.
-

- 10. Karahaliloglu, Z.; Kilicay, E. In vitro Evaluation of Bone Cements Impregnated with Selenium Nanoparticles Stabilized by Phosphatidylcholine (PC) for Application in Bone. J. Biomater. Appl. 2020, 35, 385-404.
-

- 11. Jacquart, S.; Girod-Fullana, S.; Brouillet, F.; Pigasse, C.; Siadous, R.; Fatnassi, M.; Grimoud, J.; Rey, C.; Roques, C.; Combes, C. Injectable Bone Cement Containing Carboxymethyl Cellulose Microparticles as a Silver Delivery System Able to Reduce Implant-associated Infection Risk. Acta Biomater. 2022, 145, 342-357.
-

- 12. Liu, S.; Chen, J.; Huang, S.; Lin, S.; Chen, W. Enhanced Cell Osteogenic Differentiation in Alendronate Acid and Flufenamic Acid Drug- Impregnated Nanoparticles of Mesoporous Bioactive Glass Composite Calcium Phosphate Bone Cement In Vitro. Pharmaceuticals 2023, 16, 680.
-

- 13. Wall, V.; Nguyen, T.; Nguyen, N.; Tran, P. A. Controlling Antibiotic Release from Polymethyl-methacrylate Bone Cement. Biomedicines 2021, 9, 26.
-

- 14. Liu, Y.; Yan, L.; Heiden, P.; Laks, P. Use of Nanoparticles for Controlled Release of Biocides in Solid Wood. J. Appl. Polym. Sci. 2001, 79, 458-465.
-

- 15. Shen, F.; Qiao, M.; Shan, G.; Gao, N.; Chen, J.; Wu, Q.; Ran, Q. Enhancement of Bubble Stability in Cement-based Materials by a Sustained-release Effect of Silica Nanoparticles. Constr. Build. Mater. 2023, 362, 129739.
-

- 16. Dong, L.; Zhang, Y.; Guo, Y.; Shu, X.; Ran, Q.; Feng, P. Effects of Controlled Release Silica Nanocapsules Containing Sucrose on the Heat Release of Cement Hydration. Colloids Surf. A 2023, 670, 131593.
-

- 17. Gadkari, R. R.; Ali, S. W.; Joshi, M.; Rajendran, S.; Das, A.; Alagirusamy, R. Leveraging Antibacterial Efficacy of Silver Loaded Chitosan Nanoparticles on Layer-by-layer Self-assembled Coated Cotton Fabric. Int. J. Biol. Macromol. 2020, 162, 548-560.
-

- 18. Heravi, M. E. M. Effects of Hydrodynamic Diameter of Nanoparticles on Antibacterial Activity and Durability of Ag-treated Cotton Fabrics. Fiber. Polym. 2020, 21, 1173-1179.
-

- 19. Perinelli, D. R.; Palmieri, G. F.; Cespi, M.; Bonacucina, G. Encapsulation of Flavours and Fragrances into Polymeric Capsules and Cyclodextrins Inclusion Complexes: An Update. Molecules 2020, 25, 5878.
-

- 20. Sohn, S. O.; Lee, S. M.; Kim, Y. M.; Ghim, H. D. Characteristics and Release Behaviors of Aromatic Poly(vinyl acetate) Nanoparticles Prepared by Emulsification-Diffusion Technique. Polym. Korea 2007, 31, 177-183.
- 21. Kowalczyk, D.; Kaminska, I. Effect of pH and Surfactants on the Electrokinetic Properties of Nanoparticles Dispersions and Their Application to the PET Fibres Modification. J. Mol. Liq. 2020, 320, 114426.
-

- 22. Yu, Y.; Wang, C.; Chen, T.; Wang, Z.; Yan, J. Enhancing the Colloidal Stabilities of Zein Nanoparticles Coated with Carboxylic Curdlans. LWT 2021, 137, 110475.
-

- 23. Salazar-Bryam, A. M.; Yoshimura, I.; Santos, L. P.; Moura, C. C.; Santos, C. C.; Silva, V. L.; Lovaglio, R. B.; Marques, R. F. C.; Junior, M. J.; Contiero, J. Silver Nanoparticles Stabilized by Ramnolipids: Effect of pH. Colloids Surf. B 2021, 205, 111883.
-

- 24. Xu, R. Progress in Nanoparticles Characterization: Sizing and Zeta Potential Measurement. Particuology 2008, 6, 112-115.
-

- 25. Babito; Sharma, S. K.; Gupta, S. M. Preparation and Evaluation of Stable Nanofluids for Heat Transfer Application: A Review. Exp. Therm. Fluid Sci. 2016, 79, 202-212.
-

- 26. Kumar, A.; Aerry, S.; Goia, D. V. Preparation of Concentrated Stable Dispersions of Uniform Ag Nanoparticles Using Resorcinol as Reductant. J. Colloid Interface Sci. 2016, 470, 196-203.
-

- 27. Bao, Z.; Bing, N.; Zhu, X.; Xie, H.; Yu, W. Ti3C2Tx MXene Contained Nanofluids with High Thermal Conductivity, Super Colloidal Stability and Low Viscosity. Chem. Eng. J. 2021, 406, 126390.
-

- 28. Sen, S.; Govindarajan, V.; Pelliccione, C. J.; Wang, J.; Miller, D. J.; Timofeeva, E. V. Surface Modification Approach to TiO2 Nanofluids with High Particle Concentration, Low Viscosity, and Electrochemical Activity. ACS Appl. Mater. Interfaces 2015, 7, 20538-20547.
-

- 29. Ilyas, S. U.; Pendyala, R.; Marnenil, N. Preparation, Sedimentation, and Agglomeration of Nanofluids. Chem. Eng. Technol. 2014, 37, 2011-2021.
-

- 30. Lim, G. N.; Kim, S. Y.; Kim, M. J.; Park, S. N. Physical Characteristics and In vitro Transdermal Delivery of PCL-b-PEG Micelles Containing Quercetin and Rutin. Polym. Korea 2012, 36, 420-426.
-

- 31. Lee, E. J.; Lim, K. Preparation of (−)-Epigallocatechin Gallate (EGCG)-encapsulated Gelatin Nanoparticles by Nanoprecipitation and Their Characteristics. Polym. Korea 2021, 45, 322-328.
-

- 32. Pochapski, D. J.; Santos, C. C.; Leite, G. W.; Pulcinelli, S. H.; Santilli, C. V. Zeta Potential and Colloidal Stability Predictions for Inorganic Nanoparticle Dispersions: Effects of Experimental Conditions and Electrokinetic Models on the Interpretation of Results. Langnuir 2021, 37, 13379-13389.
-

- 33. Decher, G. Fuzzy Nanoassemblies: Toward Layered Polymeric Multicomposites. Science 1997, 277, 1232-1237.
-

- 34. Hong, J.; Han, J. Y.; Yoon, H.; Joo, P.; Lee, T.; Seo, E.; Char, K.; Kim, B. Carbon-based layer-by-layer Nanostructures: from Films to Hollow Capsules. Nanoscale 2011, 3, 4515-4531.
-

- 35. Schneider, G.; Decher, G. Functional Core/Shell Nanoparticles via Layer-by-Layer Assembly. Investigation of the Experimental Parameters for Controlling Particle Aggregation and for Enhancing Dispersion Stability. Langmuir 2008, 24, 1778-1789.
-

- 36. Aliev, F. G.; Correa-Duarte, M. A.; Mamedov, A.; Ostrander, J. W.; Giersig, M.; Liz-Marzán, L. M.; Kotov, N. A. Layer-by-Layer Assembly of Core-Shell Magnetite Nanoparticles: Effect of Silica Coating on Interparticle Interactions and Magnetic Properties. Adv. Mater. 1999, 11, 1006-1010.
-

- 37. Kommireddy, D. S.; Patel, A. A.; Shutava, T. G.; Mills, D. K.; Lvov, Y. M. Layer-by-Layer Assembly of TiO2 Nanoparticles for Stable Hydrophilic Biocompatible Coatings. Nanosci. Nanotech. 2005, 5, 1081-1087.
-

- 38. Elbakry, A.; Zaky, A.; Liebl, R.; Rachel, R.; Goepferich, A.; Breunig, M. Layer-by-Layer Assembled Gold Nanoparticles for siRNA Delivery. Nano Lett. 2009, 9, 2059-2064.
-

- 39. Ramasamy, T.; Haidar, Z. S.; Tran, T. H.; Choi, J. Y.; Jeong, J.; Shin, B. S.; Choi, H.; Yong, C. S.; Kim, J. O. Layer-by-layer Assembly of Liposomal Nanoparticles with PEGylated Polyelectrolytes Enhances Systemic Delivery of Multiple Anticancer Drugs. Acta Biomater. 2014, 10, 5116-5127.
-

- 40. Mohanta, V.; Patil, S. Enhancing Surface Coverage and Growth in Layer-by-Layer Assembly of Protein Nanoparticles. Langmuir 2013, 29, 13123-13128.
-

- 41. Zhou, J.; Pishko, M. V.; Lutkenhaus, J. L. Thermoresponsive Layer-by-Layer Assemblies for Nanoparticle-Based Drug Delivery. Langmuir 2014, 30, 5903-5910.
-

- 42. Kim, M.; Hwang, Y.; Ghim, H. D. Electronically Stabilized Copoly(Styrene-Acrylic Acid) Submicrocapsules Prepared by Miniemulsion Copolymerization. Polymers 2017, 9, 291.
-

- Polymer(Korea) 폴리머
- Frequency : Bimonthly(odd)
ISSN 0379-153X(Print)
ISSN 2234-8077(Online)
Abbr. Polym. Korea - 2023 Impact Factor : 0.4
- Indexed in SCIE
 This Article
This Article
-
2024; 48(5): 460-466
Published online Sep 25, 2024
- 10.7317/pk.2024.48.5.460
- Received on Jan 9, 2024
- Revised on Jun 23, 2024
- Accepted on Jun 24, 2024
 Services
Services
Shared
 Correspondence to
Correspondence to
- Han Do Ghim
-
Department of Textile System Engineering, Kyungpook National Univertsity, 80 Daehak-ro, Puk-gu, Daegu 41566, Korea
- E-mail: hdghim@knu.ac.kr
- ORCID:
0009-0001-2945-0270










 Copyright(c) The Polymer Society of Korea. All right reserved.
Copyright(c) The Polymer Society of Korea. All right reserved.