- Degree of Unsaturation Dependence of Curing Reaction for Butyl Rubber Complexes
Department of Chemical Engineering, Hongik University, Seoul 04066, Korea
*Yongjin Fine Chemical Co., Ulsan 44785, Korea- 불포화도에 따른 부틸고무 복합체의 가교 반응 연구
홍익대학교 화학공학과, *용진유화
Reproduction, stored in a retrieval system, or transmitted in any form of any part of this publication is permitted only by written permission from the Polymer Society of Korea.
Curing reaction for butyl rubber complexes applicable to a tire bladder is investigated as a function of the degree of unsaturation (DU). High molecular weight butyl rubbers with various DU were synthesized by cationic polymerization, providing three butyl rubbers between 1.8 and 8.4 mol% of DU. Dynamic mechanical measurement and swelling test were conducted for the systematic study of curing rate, curing density, aging, and curing mechanism. Our findings shed new light on technologically important butyl rubber-based materials.
본 연구에서는 부틸고무의 불포화도에 따른 블래더용 부틸고무 복합체의 가교 반응 속도를 연구하였다. 양이온 중합법을 이용하여 다양한 고불포화도를 갖는 고분자량 부틸고무를 합성하였다. 상용 부틸고무는 2 mol% 내외의 불포화도를 포함하고 있지만, 본 연구에서는 불포화도를 8.4 mol%까지 변화시킴으로써, 부틸고무 시스템에서 불포화도에 따른 가교 속도, 가교 밀도, 노화 및 가교 메커니즘에 대해 체계적으로 연구하였다. 본 연구는 부틸고무를 사용하는 블래더를 포함한 다양한 제품 생산의 품질 향상과 공정조건 최적화에 활용될 수 있다.
Curing kinetics of rubber complexes are investigated as a function of the degree of unsaturation (DU). Systematic control of unsaturation degree in high-molecular-weight butyl rubber by cationic polymerization, and their curing characteristics such as rate, density, and kinetics are presented.
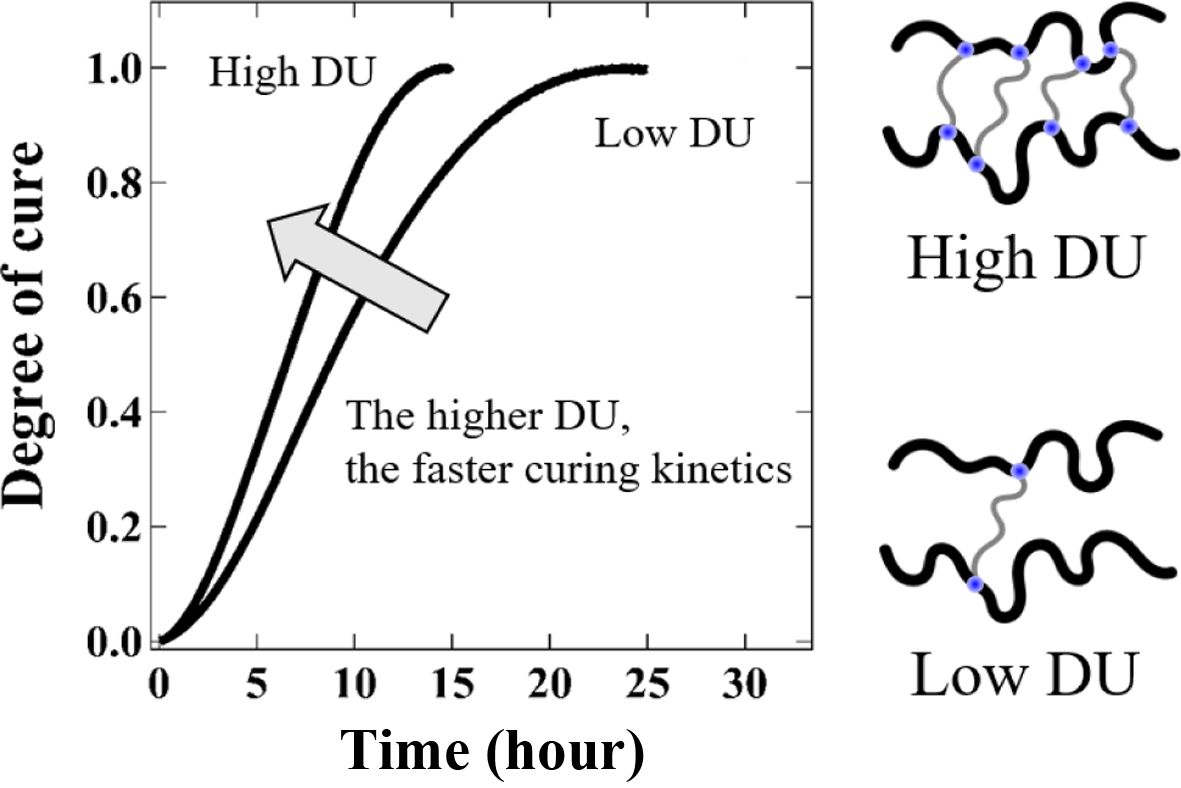
Keywords: butyl rubber, bladder, curing rate, unsaturation.
본 연구는 한국연구재단 선도연구센터지원사업(NRF-2018R1A5A1024127)과 산업기술평가원 바이오의료기기 산업핵심기술 개발사업 (10048633), 홍익대학교 학술연구진흥비에 의하여 진행되었으며, 이에 감사드립니다.
부틸고무는 이소부틸렌(isobutylene, IB, ~98 mol%)과 소량의 이소프렌(isoprene, IP, ~2 mol%)으로 이루어진 랜덤 공중합체다. 대표적인 특징으로 다른 고무들에 비해 가스투과도가 매우 낮고, 제동(damping) 성능이 우수하기 때문에, 타이어 블래더와 신발의 아웃솔 등에 많이 이용되고 있다.1-4 특히, 블래더는 타이어 생산 공정에서 가교 전 타이어가 모양을 잡을 수 있도록 내부 지지체 역할을 하며, 이때 뜨거운 기체가 블래더 내부로 들어가 타이어 안쪽 부분에서 팽창한다. 즉, 낮은 가스투과도가 요구되고, 연속적인 수축/팽창 공정 중에 물리화학적 변형이 적어야 한다. 이를 위해 블래더는 부틸고무에 페놀 수지 기반의 가교제, 가속제, 캐스터 오일, 충전제(e.g., carbon black (CB) 등), 윤활유 등이 첨가된다.
생산 측면에서 짧은 시간 내에 충분한 가교가 이루어지는 것이 중요하다. 과거 부틸고무 가교 속도에 영향을 주는 온도, 다른 고무와의 혼합, 가교제 및 가속제 종류, 충전제 등에 대한 연구가 이루어져 왔다.5-7 Sloan 연구팀은 부틸고무에 CB 충전제 양이 증가함에 따라 페놀 수지를 이용한 가교도 및 가교 속도가 증가함을 보고하였다.1 이는 CB의 열전도도가 높아 시료 내 온도를 높여 가교 반응을 가속시킨 결과이다. Caron 연구팀은 Kamal-Sourour 모델과 N차 반응 모델을 이용하여, 페놀 수지의 양과 촉매의 양이 증가할수록 같은 온도에서 반응 속도 상수가 증가함을 보고하였다.2 Formela 연구팀은 부틸고무에 ground tire rubber(GTR)를 혼합하여 가교 속도를 제어하였고, GTR 함량이 증가할수록 전체적인 가교 속도가 증가하는 것을 보고하였다.8 하지만, 분자량이 큰 두 종류 이상의 고분자는 시료내에서 상분리가 일어나는 상용성(compatibility) 문제가 있기 때문에, 두 고무의 직접적인 혼합을 통한 물성 증가는 어려웠다. 또한 가교 속도 증가는 상분리된 GTR의 빠른 가교 속도를 반영한 결과였다. Dorko 연구팀은 부틸고무 내의 이소프렌 함량을 0.5-2.8 mol%로 조절하여 황 및 페놀 수지를 이용한 가교 과정을 관찰하였고, 부틸고무의 이소프렌 함량이 증가할수록 가교도는 증가하지만 가교 속도는 차이가 보이지 않음을 보고하였다.3 하지만, 불포화도가 상대적으로 작아 불포화도의 영향을 보기 위해서는 더 넓은 영역에서 불포화도에 따른 부틸고무 가교반응의 연구가 필요하다.
본 연구에서는 이중결합 함량을 조절한 부틸고무 합성과 이를 이용한 이중결합 함량에 따른 부틸고무 가교 속도에 대한 연구를 진행하였다. 특히, 양이온 중합을 통해 상용 부틸고무와 비슷한 분자량을 보이지만, 이중결합의 함량이 높은 (최대 8.4 mol%) 부틸고무를 합성하였다.9-12 블래더 제조에 사용되는 페놀 수지를 이용한 가교제, 가속제, CB 등을 섞은 복합체를 제조한 후, 시간에 따른 동적기계적 물성을 측정하고 가교 속도를 분석하였다.
부틸고무 합성. 이소부틸렌(>99%, Sigma Aldrich, USA)은 황산 칼슘과 활성탄 컬럼을 이용하여 정제한 후, 액체질소를 이용해 포집하였다. 이소프렌(98%, ACROS, USA)은 3 mL의 n-부틸리튬(Sigma Aldrich, USA)과 30분간 교반 후, 진공 증류를 통해 정제된 이소프렌을 포집하였다. 정제된 두 단량체는 정해진 이소프렌 함량에 따라 혼합하였다. 개시제와 촉매는 각각 스테아르산(98%, Alfa Aesar, USA)과 트리스(펜타플루오로페닐)붕화수소(97%, Alfa Aesar, USA)를 이용하였다. 용매인 염화메틸(99.5%, Sigma Aldrich, USA)은 황산 칼슘과 활성탄 컬럼을 이용하여 정제하였다.
부틸고무의 합성은 각각 0.043 g(0.15 mmol)의 스테아르산과 0.154 g(0.30 mmol)의 트리스(펜타플루오로페닐)붕화수소를 2 mL의 염화메틸렌에 녹여 200 g의 염화메틸이 포함된 반응기에 투입하여 30분간 교반하였다. 반응기 온도는 아세톤과 드라이아이스를 이용하여 -78 ºC로 유지하였다. 약 50 g의 이소부틸렌과 이소프렌의 혼합 단량체를 투입하여 2시간 동안 반응 후 무수 메탄올 5 mL를 첨가하여 반응을 종결하였다. 이후 반응기를 상온 상태로 두어 염화메틸을 증발 시키고, 톨루엔에 부틸고무를 다시 녹인 후 2 L의 메탄올에 침전하여 최종 결과물을 얻었다.
부틸고무 분석. 합성된 부틸고무의 불포화도는 1H-NMR (500 MHz, INNOVA 500, USA)을 이용하여 분석하였다. 분자량과 분자량 분포는 젤 투과 크로마토그래피(GPC, Yunglin YL9100-HPLC, Korea)를 이용하여 분석하였고, 테트라하이드로퓨란을 이동상으로 40 oC에서 측정하였다. 분자량 계산을 위해 폴리스티렌(PS) 표준 시료를 이용하였으며, PS의 Mark-Houwink parameter a와 k는 0.725와 0.001120 cm3/g를 이용하였고, 부틸고무의 a와 k는 0.72와 0.000126 cm3/g를 이용하였다.13,14
불포화 결합 분포를 분석하기 위해 0.5 g의 합성 부틸고무를 30 mL 염화메틸렌과 30 mL의 n-헥세인 혼합 용매에 녹여, 드라이아이스와 아세톤을 혼합한 -78 ºC 냉각조에서 오존과 6시간 동안 반응시켰다. 이후, 흄후드에서 24시간 동안 환기 후 메탄올에 침전 및 건조하여 결과물을 얻었다.
가교 시료 제조. 가교 실험에 사용될 부틸고무 복합체는 타이어 블래더 생산의 배합비를 이용하였다. 부틸고무 100 g을 기준으로, 레귤러 카본블랙 30 g, 열전도성 카본블랙 35 g, 캐스터오일 5 g, 윤활제 3 g, 균질배합제 5 g, 페 놀수지 7 g, 산화아연 5 g, 클로로프렌 고무 5 g을 배합하였다. 최종 시료는 롤밀러를 이용하여 1 mm 두께 시트로 준비하였다.
가교 속도 측정. 회전형 유변 물성 측정: 배합된 부틸고무의 가교 속도는 회전형 유변물성 측정기(MCR 302, Anton Paar, Austria)를 이용하여 측정하였다. 일반적인 블래더의 레오미터 측정온도인 180 oC를 유지하며, 1 rad/s의 frequency와 1%의 strain의 조건에서 2.5분 간격으로 시간에 따라 토크(M)를 측정하였다. 토크에 따른 가교도(X)는 (M – Mmin)/(Mmax – Mmin)로 정의되며, Mmax와 Mmin은 각각 최대 토크와 최소 토크를 의미한다. 가교 속도 지수(curing rate index, CRI)는 ASTMD 1646 Part C를 참조하여 아래와 같이 계산하였다.15

여기서, tX 는 가교도 X%까지 도달하는데 걸리는 시간이고, tmax와 tmin은 각각 최대 토크 및 최소 토크까지 걸리는 시간이다. 산업현장에서는 가교도가 1%되는 지점(t1)까지 걸리는 시간(스코치 시간)과 가교도가 90%되는 시간(t90, 가교 반응이 끝난 상태로 가정)이 중요한 공정 척도로써 CRI 가 두 값을 기준으로 정의된다.
시차 주사 열량 측정: 배합된 부틸고무의 가교 속도 및 반응열은 시차 주사 열량계(DSC 25, TA instrument, USA)를 이용하였다. 측정 온도는 25-300 oC까지 5 oC/min 속도로 질소 대기 하에 측정을 진행하였다.
가교 밀도 측정. 가교된 부틸고무의 가교 밀도 v는 팽윤 실험과 Flory-Rhener 모델을 이용하여 계산하였다.16,17 Flory-Rhener 모델은 아래와 같다.
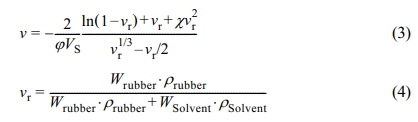
여기서, j, VS, vr, c는 각각 가교점 수, 상온에서 용매의 몰 부피, 팽윤이 평형 상태에 도달했을 때 고무의 부피 분율, Flory-Huggins interaction parameter이다. Wi 와 ρi는 각각의 무게와 밀도를 의미하며, 부틸고무의 밀도는 0.92 g/cm3, 톨루엔의 밀도는 0.867 g/cm3를 인용하였다.5 가교점 수의 경우, 서로 다른 부틸고무 사슬의 이중결합을 페놀 수지가 반응하여 가교를 형성하기 때문에 4로 가정하였다.17,18 Flory-Huggins interaction parameter의 경우 아래와 같이 정의된다.

여기서, χs는 0.34를 이용하였고, kB는 볼츠만 상수, T는 절대온도, δ는 Hildebrand 용해도 지수이다.8,13,19 V0는 격자 부피로 m/Navρ이며 m, Nav, ρ는 각각 분자량, 아보가드로 수, 밀도이다.
이때, 첨가제가 들어간 고무의 경우 vr은 아래와 같이 Kraus model로부터 정의한다.20,21
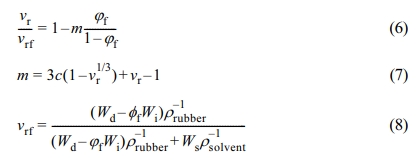
여기서, vrf 는 필러가 포함되었을 때의 샘플 내 고무의 부피분율이다. c는 첨가제의 종류에 따른 상호작용 상수로 본 연구에서 이용한 카본 블랙의 경우 일반적으로 많이 이용하는 high abrasion furnace (HAF) 카본 블랙의 1.17을 이용하였다.20 또한 φf 는 첨가제의 부피 분율로 카본 블랙의 밀도 1.83 g/cm3를 이용하여 계산하였다.22 Wd와 Wi, Ws는 각각 팽윤 후 다시 건조했을 때의 샘플 무게, 초기 샘플의 무게, 평형 상태에 도달했을때 샘플에 흡수된 용매 무게이다. 가교된 부틸고무 샘플은 팽윤 전 진공오븐에서 24시간 건조한 후 무게를 측정하고, 상온의 톨루엔에 48시간 팽윤시킨 후 무게를 측정하는 것을 5회 반복하였다.
가교 반응 속도론. 가교 반응 속도론은 Deng-Isayev 모델을 통해 속도 상수 및 반응 차수, 활성화 에너지를 구할 수 있다.7,23,24

여기서, α(t)는 가교된 정도로써, α(t) = (M(t) – Mmin)/(Mmax – Mmin)로 정의된다. n은 반응 차수이고, t1은 스코치 시간 k는 반응 속도 상수로써 아래 아레니우스 식을 따른다.

이때, k0는 빈도 인자, E0는 활성화 에너지, T는 절대 온도, R은 기체상수이다.
본 연구에서는 불포화도가 높은 고분자량의 부틸고무를 합성하고, 부틸고무 불포화도에 따른 타이어 블래더용 고무 복합체의 가교 속도 측정과 분석을 진행하였다. 상대적으로 높은 불포화도와 고분자량을 갖는 부틸고무 합성을 위해서는 양이온의 사슬 이동이 너무 급격하게 일어나지 않아야 하며,9-12 이를 위해 적절한 Lewis Base를 이용하여 반응에 참여하는 양이온의 반응성을 낮추거나, 반응 온도를 낮게 유지하여야 한다.11,12,25 양이온 중합반응에서는 개시 반응 때 이탈한 음이온이 사슬 성장 중인 양이온 중간체에 강하게 결합하여 사슬 성장을 방해하기 때문에, 구조적 방해 및 양이온 중간체와 약한 결합을 유도할 수 있는 거대한 음이온 분자를 이용하는 합성방법이 연구되어 왔다.11,12 본 연구에서는 스테아르산을 개시제로, 트리스(펜타플루오로페닐)붕화수소를 촉매로 이용하여 사슬 성장 단계의 중간체의 반응성을 제어하였다.9-12 특히, 양이온의 안정성이 떨어지는 이소프렌의 경우에도 지속적인 사슬 성장이 가능하게 되어, 고불포화도 및 고분자량의 부틸고무 합성이 가능하였다.
상용 부틸고무와 유사한 분자량을 유지하면서, 다양한 불포화도를 갖는 부틸고무 3종을 합성하였다. Figure 1에는 합성된 세 종류 부틸고무의 1H NMR과 GPC 결과를 나타내었고, 수평균 분자량은 각각 357, 309, 298 kg/mol이고, 분자량 분포는 각각 2.42, 2.07, 2.25 이다. 또한 불포화도는 1H NMR의 이중결합 피크(5.07 ppm)와 폴리이소부틸렌의 반복 단위체 중 2개의 수소를 갖는 피크(1.4 ppm) 면적비를 통해 계산하였으며, 각각 1.8, 6.3, 8.4 mol%이다. 부틸고무는 각각 IIR-1, IIR-2, IIR-3로 명명하였으며, Table 1에 고분자 특성을 나타내었다. 비교를 위해 상용 부틸고무인 L 301(LANXESS Butyl 301)의 결과도 같이 표시하였다.
부틸고무 내 이중결합의 분포는 오존반응을 이용한 이중결합 절단으로 확인하였다. Figure 1(b)에서 늦은 시간대의 피크들은 오존 반응 후의 부틸고무 결과이고, 분자량은 각각 7.1, 5.6, 4.8 kg/mol이다(Table 1). 따라서, 부틸고무에 포함된 이중결합은 거의 무작위적으로 분포되었음을 확인할 수 있다.
가교 실험은 타이어 블래더 제조에 사용되는 가교제 및 첨가제를 포함한 부틸고무 복합체를 이용하였다. 부틸고무 내 이소프렌의 이중결합과 페놀 수지 말단의 수산화기가 반응하여 산소 원자가 포함된 고리 화합물인 크로만화합물을 형성하며 부틸고무 사슬 간 가교가 이루어진다. 클로로프렌 고무와 산화 아연의 열에 의한 반응으로 생성된 염화아연이 촉매로 작용한다.26
Figure 2는 온도를 180 ºC로 유지한 상태에서 IIR-1, IIR-2, IIR-3의 가교 반응 시간에 따른 토크를 나타내고 있다. 일반적으로 토크가 최소값을 갖는 순간부터 가교가 시작되고, 최대 토크에 도달했을 때를 가교가 끝난 상태로 판단한다. 최대 토크 이후 부틸고무 가교 샘플은 열에 의한 노화가 진행되어, 토크가 감소한다. 본 연구에서는 초기 측정된 토크를 최소 토크로 하였으며(즉, tmin = 0.04시간), 최대 토크에 도달하는 시간은 IIR-1, IIR-2, IIR-3 각각 24.2, 18.4, 14.9시간으로 측정되었다. 이는 기존에 상용 부틸고무의 페놀 수지 가교 시스템으로 보고된 Dorko 연구팀의 20시간, Tawney 연구팀의 16시간 이상, Hopkins 연구팀의 25시간 가교 결과와 유사하다.3,27,28 참고로 실제 공정에서는 대량의 부틸고무가 준 단열공정으로 가교가 이루어지기 때문에 수 분내에 가교가 완료된다.
Table 2에는 IIR-1, IIR-2, IIR-3 복합체의 t1과 t90을 나타내었고, 이를 바탕으로 CRI를 나타내었다. 부틸고무의 불포화도가 증가할수록 CRI 값이 커지고, 이는 불포화도가 증가함에 따라 부틸고무 가교 속도가 빨라지는 것을 의미한다. 고무의 가교 속도는 불포화도, 촉매, 가교 종류, 첨가제 등 많은 영향을 받기 때문에 직접적인 비교가 힘들지만, 불포화도가 증가할 때 가교 속도가 증가하는 경향은 과거 보고된 결과와 일치한다.1-3 과거 Dorko 연구팀도 부틸고무의 불포화도를 조절하여 가교 현상을 관찰하였지만, 불포화도가 0.5-2.8 mol%로 낮아 가교 속도 차이가 크지 않게 보고되었다.3 하지만 Ahmadpour 연구팀은 페놀 수지를 이용한 에틸렌-프로필렌-다이엔고무(EPDM)의 가교 반응 연구에서 EPDM의 불포화도가 4.3 wt%에서 9 wt%로 증가할 때, CRI는 847 hr-1와 1081 hr-1으로 1.27배 증가하였다.5
Table 2에 나타내었듯이, 불포화도가 커짐에 따라 ∆M (=Mmax – Mmin)도 증가하였다. 고무 가교 과정에서 토크의 증가는 가교도의 증가를 의미한다. 또한, 팽윤실험의 결과로써, 불포화도가 증가함에 따라 최종 가교 밀도가 증가함을 확인하였다(Figure 3). 이러한 결과는 이중결합의 수의 증가에 기인한 것으로, 과거 가교 고무 연구의 결과와 일치한다.5,29,30 Zieliñska 연구팀은 EPDM 고무를 과산화물로 가교 반응 할 때, 가교 수를 조절하여 가교도와 가교 밀도를 조사하였다.30 이 연구에서 가교수가 증가하여 ∆M이 4 dN·m에서 6 dN·m로 증가할 때, 가교 밀도는 약 3.55×10-4 mol/cm3에서 약 7.5×10-4 mol/cm3로 증가하였다. 따라서, 불포화도가 큰 부틸고무일수록 더 촘촘한 가교를 형성하고, 이에 따른 토크 증가량도 크다.
하지만, 불포화도가 증가한 만큼 정량적으로 가교 밀도가 증가 하지 않는 것을 확인할 수 있는데 이는 불균일한 가교 형성에 기인한다.31,32 Hinchiranan 연구팀에서는 수소화 처리된 천연고무와 일반 천연고무의 비율을 체계적으로 바꿔가며, 과산화물 가교를 하여 ∆M을 측정하였다.6 수소화 처리된 천연 고무가 25, 50, 75, 90%로 증가할 수록 ∆M은 60.1, 55.6, 58.0, 31.7 dN·m로 감소하는 경향을 보였다. 샘플 내 불포화도가 감소하며 ∆M이 감소하는 경향성은 같지만, 불포화도가 90%에서 25%로 약 3.6배 감소할 때, ∆M은 약 1.9배 감소하였다. 이는 이중결합의 정량적 감소가 가교도의 감소와 정비례 하지 않음을 보이는 사례이다.
Figure 2에서 최대 토크 값을 지난 후, 세 샘플 모두 토크 감소를 보인다. 일반적으로 가교 반응은 열에 의한 가교 형성 반응과 열에 의한 가교 분해 반응의 경쟁이 동시에 일어나며, 토크가 감소하는 것은 열에 의해 가교 분해 반응이 우세하게 일어나는 것으로 알려져 있다. 특히, IIR-2, IIR-3의 경우 최대 토크에 도달한 후 24시간이 지났을 때 토크의 변화가 거의 없지만, IIR-1은 다른 두 샘플에 비해 토크 감소가 더 크게 나타났다. 과거 다양한 고무 가교 실험에서 가교 밀도가 높으면 열 안정성이 증가한다는 연구 결과들이 보고되었다.33-36 Rybiñski 연구팀은 다이엔 고무 2종을 이용해 가교 밀도를 조절하여 가교 후 열 안정성을 연구하였고, 가교 밀도 증가가 활성화 에너지 증가 및 열에 의한 사슬 분해 반응 속도 감소로 이어진다고 보고하였다.36 이를 통해, 본 연구에서 부틸고무의 이중결합이 증가하면서 가교 밀도가 증가하고, 열에 의한 가교 결합 분해가 느려지는 것을 이해할 수 있다.
불포화도에 따른 가교 속도 분석을 위해 식 (9)를 이용하여, 시간에 따른 토크 결과를 피팅하였다(Figure 4).23,37 이를 통해, 반응 온도 160, 170, 180 ºC에서 IIR-3의 반응 속도 상수(k), 반응 차수(n), 활성화 에너지(Ea)를 구할 수 있었고, Table 3에 정리하였다. 반응 속도 상수(k)의 경우, 160, 170, 180 oC에서 각각 2.45, 4.30, 7.44×10-5 hr-1로써, 온도가 증가할수록 반응 속도도 빨라진다. 또한 부틸고무의 페놀 수지 가교 반응의 반응 차수의 경우 4차 반응으로 분석되며, 이는 선행연구의 분석결과의 범위 내에서 잘 일치함을 보인다. 대표적인 천연고무의 가황 반응의 경우 반응 속도 모델 분석 시 반응 차수가 2.5-4.5로 보고된 바 있다.7 또한 본 연구의 배합조건에서 부틸고무의 페놀 수지 가교에 필요한 활성화 에너지는 90.7 kJ/mol로 분석되었다. 이는 과거 Caron 연구팀과 Ivan 연구팀에서 보고한 부틸고무의 페놀 수지 가교반응 활성화 에너지로 보고된 84와 80.3 kJ/mol과 유사하다.2,38,39
Figure 5에는 가교 온도 180 oC에서 IIR-1, IIR-2, IIR-3의 시간에 따른 토크 변화량과 식 (9)를 이용한 피팅 결과를 나타내었다. 각 샘플들의 반응 차수, 활성화 에너지, 반응 속도를 Table 4에 나타내었다. 흥미롭게도, 반응 차수 및 활성화 에너지는 거의 동일하였지만, 반응 속도 상수는 불포화도에 따라 큰 차이를 보였다.
식 (9)는 n차 반응 속도식과 아레니우스 식을 따르는 반응속도 상수를 이용하여, 실험적으로 시간에 따른 토크 변화를 나타낸 모델이다. 부틸고무의 불포화도가 증가할수록 반응 속도는 증가하지만, 반응 차수 및 활성화 에너지는 큰 차이가 없는데, 이는 빈도 인자가 증가하는 것으로 이해될 수 있다. 즉, 이소프렌 함량이 증가할수록 가교 반응에서 유효 충돌이 증가하는 것을 의미한다. Khang 연구팀은 천연고무를 가황하여 Deng-Isayev 모델을 이용해 가교제의 양, 실리카의 양, 가교 가속제의 양에 따라 반응 속도 상수 및 반응 차수에 대해 보고하였다.7 가교제의 양이 0.25 phr에서 0.5 phr로 증가할 때 반응 차수는 4.5, 4.3으로 큰 차이가 없으나, 반응 속도 상수는 180 oC에서 2.30×10-6 s-1에서 8.07×10-6 s-1로 3.5배 증가했음을 보고하였다. 이는 반응물의 농도가 증가하여 빈도 인자가 증가하였기 때문이다. 따라서, 본 연구에서 부틸고무의 불포화도 증가는 가교 반응에서 유효 빈도 인자 증가를 유도한다고 이해될 수 있다.
Figure 6은 시차 주사 열량계(DSC)를 이용하여 25 ºC에서 300 ºC까지 승온 상태로 IIR-1, IIR-2, IIR-3의 반응열을 관측한 결과이다. 가교 온도 구간인 170-230 ºC 범위에서 측정된 총 반응열 ∆Htotal은 IIR-1, IIR-2, IIR-3 각각 3.9, 5.4, 6.3 J/g으로 측정되었다. 부틸고무의 경우 다른 고무들에 비해 이중결합 함량이 적어 반응열이 낮고, 이는 선행 연구의 결과와 잘 일치한다. Dziemidkiewicz 연구팀은 온도 범위 150-210 ºC에서 할로겐화 부틸고무의 ∆Htotal을 1.8-13.6 J/g으로 보고하였으며,40 Gopisathi 연구팀도 할로겐화 부틸고무의 가황반응에서 160 ºC 등온일 때 ∆Htotal = 8.12 J/g으로 보고하였다.41,42 이중결합 함량이 증가할수록 반응열이 증가하는 경향성을 보였으며, 단열 공정의 경우 불포화도가 높을수록 가교열이 높아 가교 속도를 촉진할 수 있다.

|
Figure 1 (a) 1H NMR spectra for IIR-1, IIR-2, and IIR-3. Degree of unsaturation is calculated with the peak at 5.07 ppm corresponding to C=C shown in the inset. As a comparison, 1H NMR of L 301 (LANXESS Butyl 301) is presented; (b) GPC traces for IIR-1, IIR2, and IIR-3 before (solid) and after (dashed) the ozonolysis. As a comparison, GPC trace for L 301 is presented. |

|
Figure 2 Time dependent torque obtained from IIR-1, IIR-2, and IIR-3 at 180 ºC. |

|
Figure 3 Crosslink density as a function of the degree of unsaturation (i.e., isoprene contents). |

|
Figure 4 Degree of cure for IIR-3 at 160, 170, 180 ºC, and the time-dependent torque is fitted by eq. (5) as a solid line. Inset illustrates ln k versus 1/T, resulting in the activation energy Ea. |

|
Figure 5 Degree of cure for IIR-1, 2, 3 at 180 ºC, and the timedependent torque is fitted by eq. (9) as a solid li |

|
Figure 6 DSC thermograms of IIR-1, 2, 3 upon heating at a ramping rate of 5 ℃/min between 25 ºC and 300 ºC. Thermograms are vertically shifted for clarity. |
|
Table 1 Characteristics of Butyl Rubber |

a Number-average molecular weight measured after the ozonolysis. |
본 연구에서는 양이온 중합을 이용하여 상용 부틸고무와 분자량은 비슷하면서, 서로 다른 불포화도를 갖는 부틸고무를 합성하여, 블래더 배합 조건 하에서 부틸고무 복합체의 가교 속도를 분석하였다. 천연고무 등을 이용하지 않고 불포화도를 조절함으로써 상분리가 발생하지 않는 조건에서 체계적으로 불포화도에 따른 가교 현상을 분석할 수 있었다. 불포화도가 증가할수록 가교 밀도가 증가하고, 높은 유효 빈도 인자에 의한 가교 속도 촉진 및 가교열이 증가한다. 본 연구는 부틸고무를 이용하여 블래더를 포함한 다양한 제품을 생산할 때, 품질 향상과 공정 조건 최적화에 기초자료로 활용될 수 있다.
- 1. Sloan, J. M. Butyl Rubber: Compound Development and Characterization; U.S. Army Research Laboratory: Aberdeen Poroving Ground, MD, April 2000.
-

- 2. Caron, P. A.; Larreteguy, A. E.; Porta, P. F. Cure Kinetics of Butyl Rubber Cured by Phenol Formaldehyde Resin. Lat. Am. Appl. Res. 2017, 47, 59-64.
-

- 3. Dorko, Z. J.; Edwards, D. C.; Lumb, P. B. Faster Curing Butyl Rubber. Rubber Chem. Technol. 1962, 35, 705-715.
-

- 4. Kim, S. M.; Cho, H. W.; Kim, J. W.; Kim, K. J. Effects of Processing Geometry on the Mechanical Properties and Silica Dispersion of Silica-Filled Isobutylene-Isoprene Rubber (IIR) Compounds. Elastomers. Compos. 2010, 45, 223-229.
- 5. Imanifar, M.; Movahed, S. O.; Ahmadpour, A. Effects of Peroxide and Phenolic Cure Systems on Characteristics of the Filled Ethylene-Propylene-Diene Monomer Rubber (EPDM). J. Appl. Polym. Sci. 2018, 135, 46213-46221.
-

- 6. Hinchiranan, N.; Lertweerasirikun, W.; Poonsawad, W.; Rempel, G. L.; Prasassarakich, P. Cure Characteristics and Mechanical Properties of Hydrogenated Natural Rubber/Natural Rubber Blends. J. Appl. Polym. Sci. 2009, 111, 2813-2821.
-

- 7. Khang, T. H.; Ariff, Z. M. Vulcanization Kinetics Study of Natural Rubber Compounds Having Different Formulation Variables. J. Therm. Anal. Calorim. 2012, 109, 1545-1553.
-

- 8. Formela, K.; Haponiuk, J. T. Curing Characteristics, Mechanical Properties and Morphology of Butyl Rubber Filled with Ground Tire Rubber (GTR). Iran Polym. J. 2014, 23, 185-194.
-

- 9. Garratt, S.; Guerrero, A.; Hughes, D. L.; Bochmann, M. Arylzinc Complexes as New Initiator Systems for the Production of Isobutene Copolymers with High Isoprene Content. Angew. Chem. Int. Ed. 2004, 43, 2166-2169.
-

- 10. Guerrero, A.; Kulbaba, K.; Bochmann, M. Alkyl Zinc Chlorides as New Initiators for the Polymerization and Copolymerization of Isobutene. Macromol. Chem. Phys. 2008, 209, 1714-1720.
-

- 11. Tse, C. K. W.; Penciu, A.; McInenly, P. J.; Kumar, K. R.; Drewitt, M. J.; Baird, M. C. Isobutene Homo- and Isobutene-Isoprene Copolymerization Initiated by Protic Initiators Associated with a Series of Novel, Weakly Coordinating Counteranions. Eur. Polym. J. 2004, 40, 2653-2657.
-

- 12. McInenly, P. J.; Drewitt, M. J.; Baird, M. C. High-Molecular-Weight Isobutene-Isoprene Copolymers Containing Unusually High Isoprene Content. Macromol. Chem. Phys. 2004, 205, 1707-1712.
-

- 13. Mark, J. E. Polymer Data Handbook, 2nd ed.; Oxford University Press: New York, USA, 1999.
- 14. Mrkvičková, L.; Lopour, P.; Pokorný, S.; Janča J. Gel Permeation Chromatography of Polyisobutylene in Tetrahydrofuran. Angew. Makromol. Chem. 1980, 90, 217-221.
-

- 15. Ahmed, K.; Nizami, S. S.; Raza, N. Z.; Shirin K. Cure Characteristics, Mechanical and Swelling Properties of Marble Sludge Filled EPDM Modified Chloroprene Rubber Blends. Adv. Mater. Phys. Chem. 2012, 2, 90-97.
-

- 16. Ayala, J. A.; Hess, W. M.; Kistler, F. D.; Joyce, G. A. Carbon-Black-Elastomer Interaction. Rubber Chem. Technol. 1991, 64, 19-39.
-

- 17. Mitra, S.; Chattopadhyay, S.; Bhowmick, A. K. Synthesis and Characterization of Chemically Crosslinked Styrene-Butadiene Rubber Nanogels and their Effect on Various Properties of the Rubber. Rubber Chem. Technol. 2008, 81, 842-864.
-

- 18. Mok, K. L.; Eng, A. H. Characterisation of Crosslinks in Vulcanised Rubbers: From Simple to Advanced Techniques. Mal. J. Chem. 2018, 20, 118-127.
-

- 19. Lund, R.; Willner, L.; Lindner, P.; Richter, D. Structural Properties of Weakly Segregated PS-PB Block Copolymer Micelles in n-Alkanes: Solvent Entropy Effects. Macromolecules 2009, 42, 2686-2695.
-

- 20. Kraus, G. Swelling of Filler-Reinforced Vulcanizates. J. Appl. Polym. Sci. 1963, 7, 861-871.
-

- 21. Moon, B.; Lee, J.; Park, S.; Seok, C.-S. Study on the Aging Behavior of Natural Rubber/Butadiene Rubber (NR/BR) Blends Using a Parallel Spring Model. Polymers 2018, 10, 658.
-

- 22. Mitra, S.; Chattopadhyay, S.; Bhowmick, A. K. Synthesis and Characterization of Chemically Crosslinked Styrene-Butadiene Rubber Nanogels and their Effect on Various Properties of the Rubber. Rubber Chem. Technol. 2008, 81, 842-864.
-

- 23. Isayev, A. I.; Deng, J. S. Nonisothermal Vulcanization of Rubber Compounds. Rubber Chem. Technol. 1988, 61, 340-361.
-

- 24. Yeoh, O. H. Mathematical Modeling of Vulcanization Characteri- stics. Rubber Chem. Technol. 2012, 85, 482-492.
-

- 25. Su, W. F. Principles of Polymer Design and Synthesis, Springer: Heidelberg, Germany, 2013.
- 26. Fisher, J. D. Phenolic Resins: A Century of Progress, Springer: Heidelberg, Germany, 2010.
- 27. Tawney, P. O.; Little, J. R.; Viohl, P. The Vulcanization of Butyl Rubber with Phenol Formaldehyde Derivatives. Rubber Chem. Technol. 1960, 33, 229-236.
-

- 28. Hopkins, W.; von Hellens, C. W. Curing of Butyl Rubber with a Phenolic Resin, European patent EP1016691A1, July 5, 2000.
- 29. Fei, Z.; Long, C.; Qingyan, P.; Shugao, Z. J. Influence of Carbon Black on Crosslink Density of Natural Rubber. Macromol. Sci. B 2012, 51, 1208-1217.
-

- 30. Zielińska, A. J.; Noordermeer, J. W. M.; Talma, A. G.; Van Duin, M. Crosslinking of Saturated Elastomers with Diazides. Part I: Mechanical Properties of Vulcanizates. Rubber Chem. Technol. 2011, 84, 243-257.
-

- 31. Chaikumpollert, O.; Yamamoto, Y.; Suchiva, K.; Kawahara, S. Mechanical Properties and Cross-linking Structure of Cross-linked Natural Rubber. Polym. J. 2012, 44, 772-777.
-

- 32. González, L.; Rodriguez, A.; Valentin, J. L.; Marcos-Fernández, A.; Posadas, P. Conventional and Efficient Crosslinking of Natural Rubber. KGK Rubberpoint 2005, 58, 638-646.
- 33. Krongauz, V. V. Crosslink Density Dependence of Polymer Degradation Kinetics: Photocrosslinked Acrylates. Thermochim. Acta. 2010, 503-504, 70-84.
-

- 34. Manaila, E.; Stelescu, M. D.; Craciun, G. Degradation Studies Realized on Natural Rubber and Plasticized Potato Starch Based Eco-Composites Obtained by Peroxide Cross-Linking. Int. J. Mol. Sci. 2018,19, 2862-2880.
-

- 35. Krumova, M.; López, D.; Benavente, R.; Mijangos, C.; Pereña, J. Effect of Crosslinking on the Mechanical and Thermal Properties of Poly(vinyl alcohol). Polymer 2000, 41, 9265-9272.
-

- 36. Rybiński, P.; Janowska, G. Effect of the Spatial Network Structure and Cross-link Density of Diene Rubbers on their Thermal Stability and Fire Hazard. J. Therm. Anal. 2014, 117, 377-386.
-

- 37. Kamal, M. R.; Sourour, S. Kinetics and Thermal Characterization of Thermoset Cure. Polym. Eng. Sci. 1973, 13, 59-64.
-

- 38. Ivan, G.; Bugaru, E.; Volintiru, T. A New Activation System for Resin Curing of Butyl Rubber. Acta Polym. 1988, 39, 647-651.
-

- 39. Hu, J.; Shan, J.; Zhao, J.; Tong, Z. Isothermal Curing Kinetics of a Flame Retardant Epoxy Resin Containing DOPO Investigated by DSC and Rheology. Thermochim. Acta. 2016, 632, 56-63.
-

- 40. Dziemidkiewicz, A.; Maciejewska, M.; Pingot, M. J. Thermal Analysis of Halogenated Rubber Cured with a new Cross-linking System. Therm. Anal. Calorim. 2018, 138, 4395-4405.
-

- 41. Sathi, S. G.; Jang, J. Y.; Jeong, K.-U.; Nah, C. Thermally Stable Bromobutyl Rubber with a High Crosslinking Density Based on a 4,4′-Bismaleimidodiphenylmethane Curing Agent. J. Appl. Polym. Sci. 2016, 133, 44092-44105.
-

- 42. Sathi, S. G.; Park, C.; Huh, Y. I.; Jeon, J.; Yun, C. H.; Won, J.; Jeong, K. U.; Nah, C. Enhancing the Reversion Resistance Crosslinking Density and Thermo-mechanical Properties of Accelerated Sulfur Cured Chlorobutyl Rubber Using 4,4′-Bis (maleimido) Diphenyl Methane. Rubber Chem. Technol. 2019, 92, 110-128.
-

- Polymer(Korea) 폴리머
- Frequency : Bimonthly(odd)
ISSN 0379-153X(Print)
ISSN 2234-8077(Online)
Abbr. Polym. Korea - 2023 Impact Factor : 0.4
- Indexed in SCIE
 This Article
This Article
-
2021; 45(4): 552-559
Published online Jul 25, 2021
- 10.7317/pk.2021.45.4.552
- Received on Feb 20, 2021
- Revised on Apr 14, 2021
- Accepted on Apr 15, 2021
 Services
Services
Shared
 Correspondence to
Correspondence to
- Soo-Hyung Choi
-
Department of Chemical Engineering, Hongik University, Seoul 04066, Korea
- E-mail: shchoi@hongik.ac.kr
- ORCID:
0000-0002-4078-6285












 Copyright(c) The Polymer Society of Korea. All right reserved.
Copyright(c) The Polymer Society of Korea. All right reserved.