- Sulfonated Poly(arylene ether sulfone) and Phosphonic Acid-Functionalized Polyhedral Oligomeric Silsesquioxane Composite Membranes for Polymer Electrolyte Membrane Fuel Cells
School of Chemical Engineering, Jeonbuk National University, 567 Baekje-Daero, Deokjin-gu, Jeonju-si, Jeollabuk-do 56896, Republic of Korea
- 고분자 전해질막 연료전지용 설폰화된 폴리(아릴렌 에테르 설폰)과 인산기를 포함한 POSS 복합체 전해질막
전북대학교 화학공학부
Reproduction, stored in a retrieval system, or transmitted in any form of any part of this publication is permitted only by written permission from the Polymer Society of Korea.
In this study, an average of 7 phosphoric acid groups capable of transferring hydrogen ions are introduced into polyhedral oligomeric silsesquioxane (POSS) through a substitution reaction, and the prepared POSSs are added to sulfonated poly(arylene ether sulfone) (SPAES) for a polymer electrolyte membrane for fuel cells with high proton conductivity and mechanical properties. As the POSS content in SPAES increases to 5 wt%, the proton conductivity and mechanical properties increase simultaneously. However, when the POSS content exceeds 5 wt%, the two characteristics tend to decrease. This is due to the change in both proton transfer and mechanical load transfer abilities according to the distribution of POSS in SPAES. In conclusion, when 5 wt% of POSS was added to SPAES, it shows a large proton conductivity of 3.83 × 10-1 S cm-1 at 120 °C and 100% relative humidity and a high tensile strength of 60 MPa.
본 연구에서는 기계적, 화학적 특성이 뛰어난 폴리헤드랄 올리고머릭 실세스퀴옥산(POSS)에 치환 반응을 통해 평균 7개의 인산기를 도입하고, 제조된 POSS 화합물을 설폰화된 폴리(아릴렌 에테르 설폰)(SPAES)에 첨가하여 연료전지용 고분자 전해질막을 제조하였다. SPAES 내 POSS의 함량이 5 wt%까지 증가함에 따라 수소이온전도도와 기계적 물성이 동반 상승하였으나 그 이상의 POSS 함량에서는 오히려 감소하는 경향을 보였다. 이는 SPAES 내 POSS의 분산 여부에 따른 수소이온전달 및 기계적 부하전달 능력 변화에 기인한 것이다. 결론적으로 SPAES 내 5 wt%의 POSS가 첨가될 시 120 oC, 100% 상대습도에서 3.83×10-1 S cm-1의 높은 수소이온전도도 및 60 MPa의 높은 인장강도를 보였다.
Multiple phosphonic acids group-functionalized POSS was incorporated into sulfonated poly(arylene ether sulfone) for polymer electrolyte membranes fuel cells. The composite membrane exhibits high proton conductivity of up to 3.83x10-1 S cm-1 at 120 oC and 100% relative humidity and large mechanical strength of 60 MPa.
Keywords: fuel cell, polymer electrolyte membrane, polyhedral oligomeric silsesquioxane, phosphonic acid, proton conductivity.
이 논문은 정부(과학기술정보통신부)의 재원으로 한국연구재단의 지원을 받아 수행된 기초연구사업임(과제번호: NRF-2021R1A2C1010085). 또한, 이 논문은 2022년도 전북대학교 연구기반 조성비 지원에 의하여 연구되었음.
저자는 이해상충이 없음을 선언합니다.
고분자 전해질막 연료 전지(polymer electrolyte membrane fuel cells, PEMFCs)는 자동차, 고정식, 및 휴대용 응용 분야를 위한 친환경적이고, 효율적인 에너지 전환 시스템으로 최근 많은 연구가 진행되고 있다.1-3 수소이온을 전달하고 연료 전지 시스템에서 반응 가스 연료와 전자를 차단할 수 있는 고분자 전해질막(PEM)은 PEMFC의 핵심 구성 요소로 간주된다.4 Nafion®과 같은 설폰화된 과불소계 이오노머는 높은 수소이온전도도와 뛰어난 화학적 안정성으로 인해 상업용 벤치마크 PEM으로 널리 사용되고 있다.5 그러나 이러한 전해질막은 낮은 유리전이온도, 80 oC 이상의 온도에서 열악한 열-기계적 특성, 심각한 연료 교차 특성 및 높은 비용을 포함하여 여러 가지 단점이 있다.6-9 이러한 결점은 설폰화 폴리(아릴렌 에테르 설폰)(sulfonated poly(arylene ether sulfone), SPAES)을 포함한 설폰화 탄화수소 고분자를 기반으로 한 대체 PEM의 개발을 촉발했다.10-12 예를 들어, 설폰화된 폴리이미드(SPI),13 설폰화된 폴리(에테르 에테르 케톤)(SPEEK),14,15 폴리벤즈이미다졸(PBI)16-18은 PEMFC 응용을 위한 대체 고분자로 현재 활발히 연구되고 있다. 이러한 탄화수소 고분자 중 SPAES는 높은 열안정성, 우수한 기계적 강도 및 비교적 저렴한 비용으로 제작될 수 있는 PEM으로 널리 연구되어 왔다.19 이러한 장점에도 불구하고, 일반적으로 SPAES 자체는 설폰화된 과불소계 고분자 전해질에 비해 낮은 수소이온 전도도를 가지고 있기 때문에 실제 응용 측면에서 제한이 많은 상황이다.20,21 SPAES의 수소이온전도도는 설폰화 정도(degree of sulfonation, DS)를 증가시킴으로써 향상될 수 있는 반면, 높은 DS를 갖는 SPAES는 PEMFC 작동을 위한 물리적 및 화학적 안정성이 떨어지게 된다.22 이런 문제점을 해결하고자 SPAES의 블록 공중합체,23 빗살 모양 중합체24 및 높은 DS를 갖는 SPAES를 기반으로 한 기공 충전 구조25 등의 새로운 접근들이 수행되었다. 이러한 접근법은 어느 정도 개선된 특성을 보여주긴 했으나 고분자 제조를 위한 복잡한 합성 절차와 전해질 막 제조를 위한 복잡한 공정과 같은 단점들 때문에 한계점을 노출하였다.
본 연구에서는 기계적, 화학적 물성이 뛰어난 polyhedral oligomeric silsesquioxane에 수소이온전달이 가능한 다수의 인산기(-PO3H2)를 도입한 나노 소재를 합성하고, 이를 SPAES 고분자 내 분산시킨 연료전지용 고분자 전해질막을 제조하였다. 이때 SPAES 내 POSS의 함량을 달리하여 최적의 복합체 전해질막 조성을 찾고자 하였다. 더불어, 각 복합체 전해질막의 분광학적, 물성적, 그리고 전기화학적 특성 비교 분석도 같이 병행하였다. 이 중 POSS의 함량이 SPAES 대비 5 wt% 첨가되었을 시 120 oC, 100% 상대습도에서 3.83×10-1 S cm-1의 높은 수소이온전도도 및 60 MPa의 높은 인장강도를 보였다.
PO(OH)2-POSS 합성. 다수의 인산기를 포함하는 POSS 화합물(PO(OH)2-POSS)은 우리 이전 연구 실험방법을 토대로 합성되었다.26
SPAES 합성(Na+ 형태). SPAES의 합성 절차는 다음과 같다. 먼저, 4,4'-dichlorodiphenylsulfone(DCDPS, 98.0%, Aldrich, USA)은 사용 전에 methanol과 toluene으로 각각 재결정화되었다. 3,3’-Disulfonate-4,4’-dichlorodiphenyl sulfone(SDCDPS)는 기존 발표된 문헌을 토대로 DCDPS로부터 합성하였다.27 4,4’-Dihydroxybiphenyl(BP, 97.0%, Aldrich, USA) 5.00 g (26.9 mmol), DCDPS 3.86 g(13.4 mmol), SDCDPS 6.60 g (13.4 mmol), K2CO3(99.0+%, Aldrich) 4.27 g(30.9 mmol), N-methyl-2-pyrrolidone(NMP, 99.0%, Junsei, Japan) 45.2 mL(~25 wt%), 22.6 mL toluene(99.7%, DAEJUNG, South Korea)를 질소 주입구, 기계적 교반기, 응축기 및 Dean-Stark 트랩이 장착된 3구 플라스크에 채웠다. 반응물을 145 oC에서 4시간 동안 가열하여 toluene과의 공비혼합물로서 완전한 탈수를 진행하였다. Toluene을 완전히 제거한 후 온도를 190 oC로 올리고 24시간 더 반응을 지속하여 약간 점성이 있는 용액을 얻었다. 실온으로 냉각시킨 후, NMP 10.0 mL를 첨가하여 이 용액을 희석시켰다. 균질한 용액을 여과하여 염을 제거하고 iso-propylalcohol(1000 mL, 99.7% DAEJUNG, South Korea)에 따라내어 중합체를 분리하고 침전물을 iso-propylalcohol로 여러 번 헹구었다. 이어서, 회백색 고체를 진공 하에 건조시켰다. 수율: >90%. Mn: 82789, Mw: 349244.
복합체 필름 제조. 용액 주조에 의해 SPAES(Na+ 형태) 및 포스폰화 에스테르 형태의 POSS(PO(OEt)2-POSS)를 상이한 wt%로 일련의 복합 전해질막을 제조하였다. SPAES 대비 PO(OEt)2-POSS의 중량비는 3, 5, 10, 20이었다. 예를 들어, 10 wt%의 PO(OEt)2-POSS를 함유하는 SPAES(Na+ 형태)는 다음과 같이 제조하였다: SPAES(Na+ 형태) 1.00 g 및 0.10 g의 PO(OEt)2-POSS를 80 oC에서 10.5 mL의 DMAc 용액에 용해시켰다. 그런 다음 혼합 용액을 깨끗한 평판 유리판에 펼쳤다. 용액의 두께는 조절 가능한 닥터 블레이드를 사용하여 조절되었고, 주조된 용액은 DMAc 증발이 관찰되지 않을 때까지 80 oC에서 12시간 동안 건조되도록 두었다. 실온으로 냉각시킨 후, 얻어진 필름을 증류수에 담그고 기재로부터 박리하였다. 생성된 필름을 60 oC에서 1시간 동안 젤 건조기를 사용하여 건조시킨 후, 필름을 진공 오븐에 넣어 12시간 동안 추가 건조하였다. PO(OEt)2-POSS를 포스폰산 형태의 포스폰산 형태(PO(OH)2-POSS)로 전환하기 위해, PO(OEt)2-POSS를 함유하는 복합막을 환류하에 농축된 HBr 용액에 72시간 동안 침지시켰다. 복합 필름을 증류수로 여러 번 철저히 세척하여 중화 및 과잉 산을 제거한 후 젤 건조기를 사용하여 60 oC에서 1시간 동안 건조시킨 후, 필름을 진공 오븐에 넣어 12시간 동안 추가 건조하였다. Na+ 형태의 복합막은 80 oC에서 2시간 동안 2 M H2SO4 수용액에 담가서 산 형태(H+)로 변형시켰다. 그 후, 얻어진 전해질막(산 형태)을 증류수로 여러 번 철저히 세척한 후, 젤 건조기를 사용하여 60 oC에서 1시간 동안 건조시킨 후, 전해질막을 진공 오븐에 넣어 12시간 동안 추가 건조시켰다.
분석.1H 핵자기 공명(NMR) 스펙트럼은 500 MHz의 양성자 주파수로 Bruker Avance 500(Germany)에서 수집되었다. 실험 중 용매로는 dimethylsulfoxide-d6를, 내부 표준물질로는 테트라메틸실란(TMS)을 사용하였다. 건조된 막 및 분말 시료의 FTIR 스펙트럼은 Nicolet 6700 기기(Thermo Scientific, USA)를 사용하여 4000-650 cm-1의 주파수 범위에서 감쇠 전반사(ATR) 모드로 기록되었다. 스펙트럼은 8 cm-1의 해상도로 32회 스캔의 평균으로 기록되었다. 압력과 침투 깊이로 인한 차이를 피하기 위해 각 샘플을 분광계 액세서리의 샘플링 플레이트와 물리적으로 동등하게 접촉시켰다. 분자량(Mn, Mw)은 Waters 510 HPLC 펌프, Polymer Laboratories의 3개 컬럼 PLgel 5 μm 가드, MIXED-C 및 MIXED-D 및 Viscoter T60A 이중 검출기로 구성된 젤 투과 크로마토그래피에 의해 35 oC에서 측정되었다. HPLC 등급 THF를 용리액으로 사용하고 유속은 1.0 mL min-1이었다. 교정은 폴리머 연구소의 폴리스티렌 표준으로 설정되었다. 기계적 물성은 만능시험기(Lloyd LR-10 K, UK)를 사용하여 측정하였다. 덤벨 시편은 ASTM 표준 D638(유형 V 시편 개뼈 모양의 시편)을 사용하여 준비되었다. 전해질막 샘플의 인장 특성은 게이지 길이와 크로스 헤드 속도가 각각 15 mm 및 5 mm min-1인 45% 상대 습도, 23 oC의 공기 중에서 측정되었다. 수분 흡수율(water uptake)은 다음 식을 통해서 계산되었다.
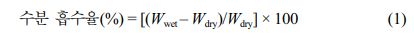
Wwet과 Wdry는 각각 수분을 흡수한 상태 전해질막과 건조된 전해질막을 의미한다. 수소이온전도도(σ)는 4전극 측정 장치가 장착된 BekkTech 전도도 셀(BT-552MX)을 사용하여 전기화학적 임피던스 분광법(EIS)으로 측정했다. 수소이온전도도(σ)는 σ = d/RS를 사용하여 계산되었으며, 여기서 d는 기준 전극과 감지 전극 사이의 거리이고 S는 전해질막의 단면적 (두께×너비)이다. 상대습도 사이클링을 통해 평형에 도달한 후 80 또는 120 oC의 다른 습도 조건에서 전도도를 측정하였다. 전지의 상대습도는 가습 컬럼을 통해 기체 흐름을 통과시켜 가습된 수소 기체를 공급함으로써 달성되었다. 원하는 상대습도를 보장하기 위해 셀과 가습 컬럼의 온도를 제어했다. 전도도 테스트는 BekkTech 테스트 프로토콜을 적용하였다. 측정은 1000 sccm(또는 500 sccm)의 입력 유량에서 100 kPa (또는 230 kPa)의 H2 80 oC(또는 120 oC)에서 수행되었다. 샘플을 80 oC(또는 120 oC) 및 70% 상대습도에서 2시간 동안 안정화 후 전도도 측정을 수행했다. 각 다음 상대습도에서 안정화 시간은 약 15분이었다.
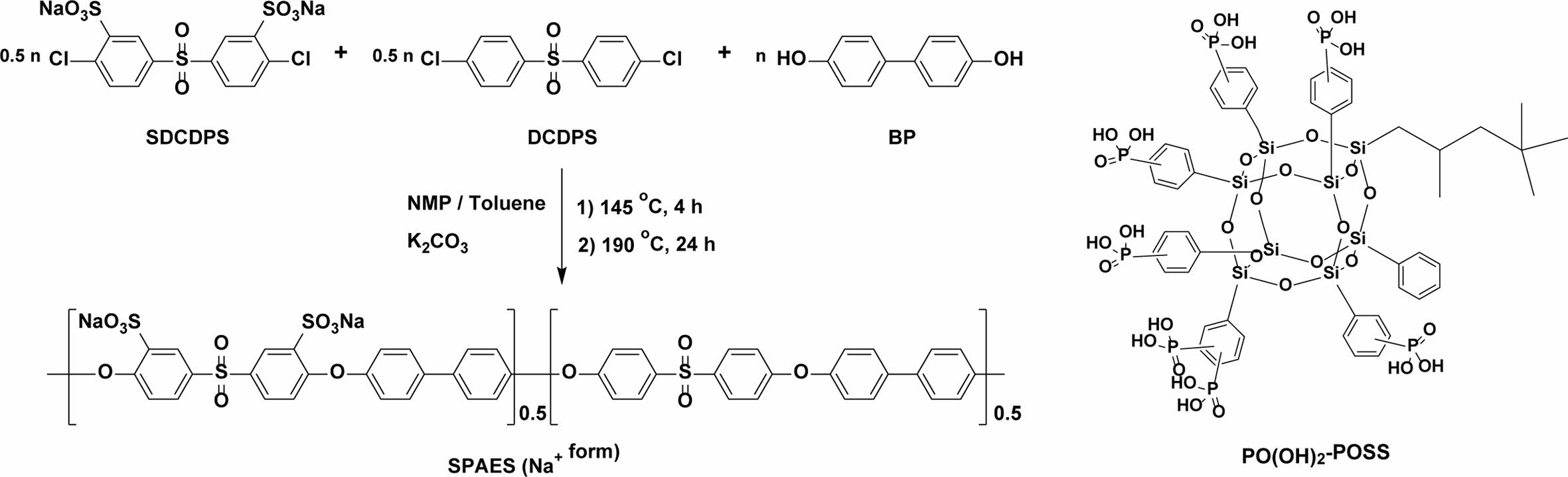
SPAES-POSS 복합체 전해질막 제조.설폰화된 폴리(아릴렌 에테르 설폰)(SPAES)은 Figure 1과 같이 BP와 같은 디히드록시 단량체와 DCDPS와 SDCDPS 같은 두 가지 유형의 디클로로 단량체 사이의 친핵성 방향족 치환 반응을 통해 성공적으로 합성되었다. 폴리스티렌 표준시료를 이용한 GPC 측정으로부터 계산된 수평균분자량(Mn)과 중량평균분자량(Mw)은 각각 82789와 349244이었다. 생성된 고분자의 화학구조(Na+ 형태)는 Figure 2와 같이 1H NMR 분광법으로 확인하였다. 단량체 DCDPS와 SDCDPS의 비율이 1:1이므로 설폰화도(mol%)는 50이 예상되었고, 실제로 1H NMR 스펙트럼의 피크 적분으로부터 계산된 SPAES의 설폰화도는 약 48에 가까운 것으로 밝혀졌다. 이 결과는 이미 보고된 바와 같이 DCDPS와 SDCDPS간의 구조적 차이에 의한 반응성 차이로 기인한 것이다.28
다수의 인산기를 포함하는 polyhedral oligomeric silses- quioxane 화합물은 iso-octylphenyl polyhedral oligomeric silsesquioxane의 브로민 치환, 포스폰화 에스테르 치환, 그리고 브롬화 수소를 통한 인산기 치환의 과정을 통해 합성되었다.26 이때 한 개의 POSS당 평균 7개의 인산기가 도입되었다. 인산기를 포함하는 POSS 및 H+ 형태 SPAES 등과 같이 산 형태의 시료들은 유기용매에 대한 용해도가 부족하기에 POSS의 경우 포스폰화 에스테르 형태(PO(OEt)2-POSS), SPAES의 경우 Na+ 형태에서 DMAc에 녹여 필름 제조를 먼저 선행하였다. 그 후 농축된 브롬화 수소를 통해 PO(OEt)2-POSS를 PO(OH)2-POSS(이하 POSS라 명칭)로 전환하였고, 그 후에 2 M 황산 수용액을 통해 Na+ 형태의 SPAES를 H+ 형태로 전환하여 최종적으로 수소이온전달 가능한 고분자 전해질막을 제조하였다. 복합체는 SPAES-POSS-X로 명칭한다. 여기서 X는 SPAES 대비 첨가된 POSS의 wt%이다.
제조된 복합체 전해질막은 ATR 모드 적외선 분광기를 통해 화학 구조를 분석하였다(Figure 3). 1580 및 1490 cm-1의 피크는 SPAES 내에 페닐 설폰 부분의 C=C 고리 스트레칭 흡수에 이에 의한 것이다. 각 스펙트럼의 지문 영역에서 1240 cm-1에서 강한 밴드가 발견되었으며 이는 에테르 결합의 C-O 스트레칭을 나타낸다. SPAES에서 설폰산 그룹의 진동은 1030(대칭 신장) 및 1082 cm-1(비대칭 신장) 및 1110 cm-1(비대칭 신장)에 의한 것이다. 또한 1101과 1143 cm-1에서 유사한 진동을 발견했다. POSS의 특징적인 피크로는 인산 결합(P=O) 스트레칭이 약 1680 cm-1에서 관찰되었다. 무엇보다도 1300-868 cm-1의 넓은 범위에서 POSS의 강한 밴드가 발견되는데, SPAES 내에 POSS의 함량이 증가함에 따라 이와 관련된 피크의 세기가 증가하는 것을 통해 SPAES 내 POSS 복합화가 성공적으로 잘 이루어진 것을 확인할 수 있었다.
수분 흡수율. SPAES 전해질막의 수분 흡수율(water uptake)이 Figure 4와 같이 POSS의 함량에 따라 측정되었다. 복합체 전해질막 전반적으로 큰 폭의 변화는 관찰되지는 않았으나, SPAES 대비 POSS의 함량이 10 wt%까지 증가함에 따라 복합체 전해질막의 수분 흡수율이 소폭 증가하는 것을 알 수 있다. SPAES-POSS-10의 수분 흡수율은 SPAES 대비 12% 높게 측정되었고 이는 친수성 인산기 도입으로 인한 수분 흡수율 상승에 기인한 것으로 판단된다. 반면에 10 wt% 초과로 POSS가 첨가될 시 수분 흡수율은 소폭 감소하는데 이는 친수성 인산기 보다도 POSS 내 소수성 -O-Si-O- 결합의 증가에 의한 것이다.
전해질막 기계적 물성. 건조된 SPAES-POSS 복합체 전해질막의 기계적 물성은 만능시험기를 통해 인장강도와 신장률 값으로 비교되었다(Table 1). SPAES의 경우 약 55 MPa의 인장강도를 가지나, SPAES 대비 POSS의 함량이 5 wt%까지 증가함에 따라 인장강도가 60 MPa로 증가한 것을 알 수 있다. 이는 일반적으로 POSS 나노 소재가 고분자 매트릭스 내에 균일하게 분산될 시 기계적 물성을 높이는 데 큰 역할을 하는 것으로 것으로부터 기인한 것이다.29 하지만 POSS의 함량이 SPAES 대비 5 wt%를 초과하였을 시에는 소폭 인장강도가 감소하는 것을 알 수 있는데, 이는 아마도 POSS가 SPAES 매트릭스 내에 과량으로 존재함으로 인한 응집 현상에 의한 것으로 판단된다.30 신장률의 경우 POSS가 들어 감에 따라 SPAES 대비 전체적으로 감소하는 것을 알 수 있고, 이는 뻣뻣한 POSS의 투입으로 인한 경도 증가에 기인한 것이다.
전해질막 수소이온전도도. 복합체 전해질막의 수소이온 전도도는 80 또는 120 oC 온도에서 상대습도를 20에서 100%로 변경하며 측정하였다(Figure 5). 온도와 무관하게 모든 SPAES-POSS 복합체 전해질막은 모든 상대습도 구간에서 SPAES보다 더 높은 수소이온전도도 값을 보인다. 높은 수소이온전도도는 POSS 내 포함된 다수의 인산기로 인한 이온 교환능이 높아지고, 긴 영역에서 수소이온 전달에 기여할 수 있는 넓은 영역에서의 유동적인 수소 결합이 형성됨으로 인한 것이다.31-33 특히, 50% 미만의 낮은 상대습도 범위에서 SPAES-POSS와 SPAES 전해질막 사이의 수소이온전도도 차이는 50% 이상의 높은 상대습도 범위에서 전해질막 간의 수소이온전도도 차이보다 더 큰 것을 확인할 수 있다. 예를 들어, 80 oC 온도, 20% 및 100% 상대습도에서 SPAES-POSS-5의 전도도 값은 각각 7.56×10-4 및 2.90×10-1 S cm-1이고, SPAES의 전도도 값은 각각 1.17×10-4 및 1.71×10-1 S cm-1이다. 즉, 따라서 20% 및 100% 상대습도 조건에서 SPAES 대비 SPAES-POSS-5의 전도도 비율은 각각 5.5 및 0.7이다. POSS에 의한 추가 인산 그룹의 도입은 앞서 살펴본 바와 같이 전해질막 내 수분 흡수율 상승을 가져옴과 더불어 수소이온 네트워크 형성을 통해 특히 저가습 조건에서의 수소이온 전달이 원활해짐을 확인할 수 있었다. 그러나 POSS의 함량이 5 wt%를 넘어선 경우는 오히려 같은 온도 및 상대습도 조건에서 소폭의 수소이온전도도 감소를 확인할 수 있다. 이는 큰 부피 새장 구조이며 수소이온 전달에 아무런 영향을 미치지 못하는 POSS 내 silsesquioxane이 과량 존재함으로 인한 응집에 기인한 것으로 판단된다. 하지만 여전히 SPAES-POSS-10, -20 복합체 전해질막은 SPAES보다 전체 상대습도 구간에서 더 높은 수소이온전도도를 보인다. 수소이온 전도도 측정 온도를 120 oC로 상승시킴으로 인해 전체적으로 복합체 전해질막의 수소이온 전도도가 전체 상대습도 구간에서 상승하였고, 80 oC에서 보였던 저가습 조건에서 복합체 전해질막의 높은 수소이온전도도 구현 현상 또한 관찰되었다. 특히, SPAES-POSS-5의 경우 100% 상대습도 구간에서 3.83×10-1 S cm-1의 높은 수소이온 전도도를 보였다. 이 값은 동일 비교 조건에서 기보고된 설폰화 고분자 전해질막의 수치 값과 유사하거나 혹은 더 높은 수치이다.34,35

|
Figure 1 (a) Synthesis of SPAES (Na+ form); (b) phosphonic acids-functionalized POSS. |

|
Figure 2 1H NMR spectroscopy of SPAES (Na+ form). |

|
Figure 3 ATR FTIR spectra of SPAES-POSS composites. |

|
Figure 4 Water uptakes (%) of SPAES-POSS composite membranes as a function of POSS contents. |

|
Figure 5 Proton conductivities of SPAES and SPAES-POSS composite membranes at (a) 80 ℃; (b) 120 ℃ as a function of relative humidity. |
|
Table 1 Tensile Strength and Elongation at Break Values of SPAES-POSS Composite Membranes |

본 연구에서는 다수의 인산기를 포함하는 POSS 화합물을 SPAES 고분자 내에 첨가하여 연료전지용 복합체 고분자 전해질막을 제조하였다. 합성된 SPAES는 약 50 mol%의 설폰화도를 가지고 있으며 유연한 전해질막으로 필름 제조가 가능하였다. 여기에 대략 7개의 인산기를 포함하고 있는 개질 된 POSS를 도입한 경우 높은 수소이온전도도와 기계적 물성을 보였다. 특히, POSS가 SPAES 대비 5 wt% 첨가되었을 시 높은 분산성으로 인해 120 oC, 100% 상대습도에서 3.83×10-1 S cm-1의 높은 수소이온전도도 및 60 MPa의 높은 인장강도를 보였다. 현재 많은 연구가 이루어지고 있는 SPAES 전해질막에 수소이온전달능이 있는 나노 소재 도입 및 분산 기술 개발을 고성능 연료전지용 고분자 전해질막으로의 응용가능성을 확인하였다.
- 1. Steele, B. C. H.; Heinzel, A. Materials for Fuel-cell Technologies. Nature 2001, 414, 345-352.
-

- 2. Hickner, M. A.; Ghassemi, H.; Kim, Y. S.; Einsla, B. R.; McGrath, J. E. Alternative Polymer Systems for Proton Exchange Membranes (PEMs). Chem. Rev. 2004, 104, 4587-4612.
-

- 3. Kim, K.; Heo, P.; Ko, T.; Lee, J.-C. Semi-interpenetrating Network Electrolyte Membranes Based on Sulfonated Poly(arylene ether sulfone) for Fuel Cells at High Temperature and Low Humidity Conditions. Electrochem. Commun. 2014, 48, 44-48.
-

- 4. Marrony, M.; Barrera, R.; Quenet, S.; Ginocchio, S.; Montelatici, L.; Aslanides, A. Durability Study and Lifetime Prediction of Baseline Proton Exchange Membrane Fuel Cell under Severe Operating Conditions. J. Power Sources 2008, 182, 469-475.
-

- 5. Carrette, L.; Friedrich, K. A.; Stimming, U. Fuel Cells-Fundamentals and Applications. Fuel Cells 2001, 1, 5-39.
-

- 6. Kim, K.; Heo, P.; Ko, T.; Kim, K.-H.; Kim, S.-K.; Pak, C.; Lee, J.-C. Poly(arlyene ether sulfone) Based Semi-interpenetrating Polymer Network Membranes Containing Cross-linked Poly(vinyl phosphonic acid) Chains for Fuel Cell Applications at High Temperature and Low Humidity Conditions. J. Power Sources 2015, 293, 539-547.
-

- 7. Li, Q.; Jensen, J. O.; Savinell, R. F.; Bjerrum, N. J. High Temperature Proton Exchange Membranes Based on Polybenzimidazoles for Fuel Cells. Prog. Polym. Sci. 2009, 34, 449-477.
-

- 8. Zhang, H.; Shen, P. K., Recent Development of Polymer Electrolyte Membranes for Fuel Cells. Chem. Rev. 2012, 112, 2780-2832.
-

- 9. Lee, J. W.; Lee, D. Y.; Kim, H.-J.; Nam, S. Y.; Choi, J. J.; Kim, J.-Y.; Jang, J. H.; Cho, E.; Kim, S.-K.; Hong, S.-A.; Lim, T.-H. Synthesis and Characterization of Acid-doped Polybenzimidazole Membranes by Sol-gel and Post-membrane Casting Method. J. Membr. Sci. 2010, 357, 130-133.
-

- 10. Li, N.; Wang, C.; Lee, S. Y.; Park, C. H.; Lee, Y. M.; Guiver, M. D. Enhancement of Proton Transport by Nanochannels in Comb-Shaped Copoly(arylene ether sulfone)s. Angew. Chem. Int. Ed. 2011, 50, 9158-9161.
-

- 11. Ko, T.; Kim, K.; Jung, B.-K.; Cha, S.-H.; Kim, S.-K.; Lee, J.-C. Cross-Linked Sulfonated Poly(arylene ether sulfone) Membranes Formed by in Situ Casting and Click Reaction for Applications in Fuel Cells. Macromolecules 2015, 48, 1104-1114.
-

- 12. Kim, D. J.; Choi, D. H.; Park, C. H.; Nam, S. Y. Characterization of the Sulfonated PEEK/sulfonated Nanoparticles Composite Membrane for the Fuel Cell Application. Int. J. Hydrog. Energy 2016, 41, 5793-5802.
-

- 13. Woo, Y.; Oh, S. Y.; Kang, Y. S.; Jung, B. Synthesis and Characterization of Sulfonated Polyimide Membranes for Direct Methanol Fuel Cell. J. Membr. Sci. 2003, 220, 31-45.
-

- 14. Xing, P.; Robertson, G. P.; Guiver, M. D.; Mikhailenko, S. D.; Wang, K.; Kaliaguine, S. Synthesis and Characterization of Sulfonated Poly(ether ether ketone) for Proton Exchange Membranes. J. Membr. Sci. 2004, 229, 95-106.
-

- 15. Nie, L.; Dong, H.; Han, X.; He, G.; Wu, H.; Jiang, Z. Enhanced Proton Conductivity under Low Humidity of Sulfonated Poly(ether ether ketone) Composite Membrane Enabled by Multifunctional Phosphonic Acid Polymeric Submicrocapsules. J. Power Sources 2013, 240, 258-266.
-

- 16. Jung, J.-W.; Kim, S.-K.; Lee, J.-C. Preparation of Polybenzimida- zole/Lithium Hydrazinium Sulfate Composite Membranes for High-Temperature Fuel Cell Applications. Macromol. Chem. Phys. 2010, 211, 1322-1329.
-

- 17. Kim, S.-K.; Kim, T.-H.; Ko, T.; Lee, J.-C. Cross-linked Poly(2,5-benzimidazole) Consisting of Wholly Aromatic Groups for High-temperature PEM Fuel Cell Applications. J. Membr. Sci. 2011, 373, 80-88.
-

- 18. Kim, S.-K.; Kim, T.-H.; Jung, J.-W.; Lee, J.-C. Polybenzimidazole Containing Benzimidazole Side Groups for High-temperature Fuel Cell Applications. Polymer 2009, 50, 3495-3502.
-

- 19. Wang, F.; Hickner, M.; Kim, Y. S.; Zawodzinski, T. A.; McGrath, J. E. Direct Polymerization of Sulfonated Poly(arylene ether sulfone) Random (Statistical) Copolymers: Candidates for New Proton Exchange Membranes. J. Membr. Sci. 2002, 197, 231-242.
-

- 20. Li, N.; Hwang, D. S.; Lee, S. Y.; Liu, Y.-L.; Lee, Y. M.; Guiver, M. D. Densely Sulfophenylated Segmented Copoly(arylene ether sulfone) Proton Exchange Membranes. Macromolecules 2011, 44, 4901-4910.
-

- 21. Kreuer, K. D. On the Development of Proton Conducting Polymer Membranes for Hydrogen and Methanol Fuel Cells. J. Membr. Sci. 2001, 185, 29-39.
-

- 22. Ouadah, A.; Luo, T.; Gao, S.; Zhu, C. Controlling the Degree of Sulfonation and Its Impact on Hybrid Cross-linked Network Based Polyphosphazene Grafted Butylphenoxy as Proton Exchange Membrane. Int. J. Hydro. Energy 2018, 43, 15466-15480.
-

- 23. Lee, H.-S.; Roy, A.; Lane, O.; McGrath, J. E. Synthesis and Characterization of Poly(arylene ether sulfone)-b-polybenzimid- azole Copolymers for High Temperature Low Humidity Proton Exchange Membrane Fuel Cells. Polymer 2008, 49, 5387-5396.
-

- 24. Ingratta, M.; Jutemar, E. P.; Jannasch, P. Synthesis, Nanostructures and Properties of Sulfonated Poly(phenylene oxide) Bearing Polyfluorostyrene Side Chains as Proton Conducting Membranes. Macromolecules 2011, 44, 2074-2083.
-

- 25. Hara, N.; Ohashi, H.; Ito, T.; Yamaguchi, T. Rapid Proton Conduction through Unfreezable and Bound Water in a Wholly Aromatic Pore-Filling Electrolyte Membrane. J. Phys. Chem. B 2009, 113, 4656-4663.
-

- 26. Kim, S.-K., Polybenzimidazole and Phosphonic Acid Groups-Functionalized Polyhedral Oligomeric Silsesquioxane Composite Electrolyte for High Temperature Proton Exchange Membrane. J. Nanomater. 2016, 2016, 2954147.
-

- 27. Ueda, M.; Toyota, H.; Ouchi, T.; Sugiyama, J.-I.; Yonetake, K.; Masuko, T.; Teramoto, T. Synthesis and Characterization of Aromatic Poly(ether sulfone)s Containing Pendant Sodium Sulfonate Groups. J. Polym. Sci., Part A: Polym. Chem. 1993, 31, 853-858.
-

- 28. Harrison, W. L.; Wang, F.; Mecham, J. B.; Bhanu, V. A.; Hill, M.; Kim, Y. S.; McGrath, J. E. Influence of the Bisphenol Structure on the Direct Synthesis of Sulfonated Poly(arylene ether) Copolymers. I. J. Polym. Sci., Part A: Polym. Chem. 2003, 41, 2264-2276.
-

- 29. Kim, S.-K.; Nguyen, N. A.; Wie, J. J.; Park, H. S. Manipulating the Glass Transition Behavior of Sulfonated Polystyrene by Functionalized Nanoparticle Inclusion. Nanoscale 2015, 7, 8864-8872.
-

- 30. Ko, T.; Kim, K.; Lim, M.-Y.; Nam, S. Y.; Kim, T.-H.; Kim, S.-K.; Lee, J.-C. Sulfonated Poly(arylene ether sulfone) Composite Membranes Having Poly(2,5-benzimidazole)-grafted Graphene Oxide for Fuel Cell Applications. J. Mater. Chem. A 2015, 3, 20595-20606.
-

- 31. Tayouo, R.; David, G.; Améduri, B.; Rozière, J.; Roualdès, S. New Fluorinated Polymers Bearing Pendant Phosphonic Acid Groups. Proton Conducting Membranes for Fuel Cell. Macromolecules 2010, 43, 5269-5276.
-

- 32. Aslan, A.; Bozkurt, A. Nanocomposite Polymer Electrolyte Membranes Based on Poly(vinylphosphonic acid)/sulfated Nano-titania. J. Power Sources 2012, 217, 158-163.
-

- 33. He, G.; Zhao, J.; Hu, S.; Li, L.; Li, Z.; Li, Y.; Li, Z.; Wu, H.; Yang, X.; Jiang, Z. Functionalized Carbon Nanotube via Distillation Precipitation Polymerization and Its Application in Nafion-Based Composite Membranes. ACS Appl. Mater. Interfaces2014, 6, 15291-15301.
-

- 34. Kim, K.; Bae, J.; Lim, M.-Y.; Heo, P.; Choi, S.-W.; Kwon, H.-H.; Lee, J.-C. Enhanced Physical Stability and Chemical Durability of Sulfonated Poly(arylene ether sulfone) Composite Membranes Having Antioxidant Grafted Graphene Oxide for Polymer Electrolyte Membrane Fuel Cell Applications. J. Membr. Sci. 2017, 525, 125-134.
-

- 35. Lee, K. H.; Chu, J. Y.; Mohanraj, V.; Kim, A. R.; Song, M. H.; Yoo, D. J. Enhanced Ion Conductivity of Sulfonated Poly(arylene ether sulfone) Block Copolymers Linked by Aliphatic Chains Constructing Wide-range Ion Cluster for Proton Conducting Electrolytes. Int. J. Hydro. Energy 2020, 45, 29297-29307.
-

- Polymer(Korea) 폴리머
- Frequency : Bimonthly(odd)
ISSN 0379-153X(Print)
ISSN 2234-8077(Online)
Abbr. Polym. Korea - 2023 Impact Factor : 0.4
- Indexed in SCIE
 This Article
This Article
-
2023; 47(1): 1-7
Published online Jan 25, 2023
- 10.7317/pk.2023.47.1.1
- Received on Jul 22, 2022
- Revised on Aug 31, 2022
- Accepted on Oct 4, 2022
 Services
Services
Shared
 Correspondence to
Correspondence to
- Sung-Kon Kim
-
School of Chemical Engineering, Jeonbuk National University, 567 Baekje-Daero, Deokjin-gu, Jeonju-si, Jeollabuk-do 56896, Republic of Korea
- E-mail: skkim@jbnu.ac.kr
- ORCID:
0000-0002-7654-224X










 Copyright(c) The Polymer Society of Korea. All right reserved.
Copyright(c) The Polymer Society of Korea. All right reserved.