- Effect of Thermal Degradation on Physical Properties of Poly(3-hydroxybutyrate-co-4-hydroxybutyrate)
Minki Jo, Tao Zhang, Yunjae Jang*, Minho Jung*, Eunhye Lee*, and Ho-Jong Kang†

Department of Polymer Science and Engineering, Dankook University, 152 Jukjeon-ro, Suji-gu, Yongin-si, Gyeonggi-do 16890, Korea
*CJ Cheiljedang Corp. 55, Gwanggyo-ro 42beon-gil, Yeongtong-gu, Suwon-si, Gyeonggi-do 16495, Korea- 열분해가 Poly(3-hydroxybutyrate-co-4-hydroxybutyrate) 물성에 미치는 영향
단국대학교 고분자공학과, *CJ 제일제당
Reproduction, stored in a retrieval system, or transmitted in any form of any part of this publication is permitted only by written permission from the Polymer Society of Korea.
The effects of thermal degradation in melt processing on physical properties of poly(3-hydroxybutyrate-co-4-hydroxybutyrate)(P(3HB-co-4HB)) and crystalline P(3HB-co-4HB)/non-crystalline P(3HB-co-4HB) mixtures were studied. It was found that thermal degradation occurred at 180 oC or higher and increased with increasing 4HB content. A small amount of thermal degradation reduces melt viscosity and increases the tanδ. As a result, it may cause a problem with melt processing ability. P(3HB-co-4HB) mixtures having similar 4HB content show a small change in rheological properties due to better thermal stability of non-crystalline P(3HB-co-4HB) in the mixtures. In addition, thermal degradation affects the crystallization behavior of P(3HB-co-4HB) in lowering crystallization temperature and decreasing crystallinity. The mixture shows the crystallization behavior similar to that of crystalline P(3HB-co-4HB), which attributed to the relatively better thermal stability of mixtures.
Poly(3-hydroxybutyrate-co-4-hydroxybutyrate)(P(3HB-co-4HB))와 결정성 P(3HB-co-4HB)/비결정성 P(3HB-co-4HB) 혼합물의 용융가공에 의한 열분해가 이들 물성에 미치는 영향을 살펴보았다. P(3HB-co-4HB)와 이들 혼합물은 180 oC 이상의 가공온도에서 4HB 함량이 증가됨에 따라 소량의 열분해가 일어남을 확인하였다. 이러한 적은 양의 열분해는 용융 점도 감소와 tan δ를 증가시켜 P(3HB-co-4HB)의 용융가공 특성이 나빠짐을 알 수 있었다. 반면, 혼합물은 같은 4HB 함량에서 혼합된 비결정성 P(3HB-co-4HB)에 의하여 상대적으로 열분해가 적게 일어나 열분해에 의한 유변 특성 변화가 최소화되어 용융가공 특성 변화가 적음을 확인하였다. 이와 함께 열분해는 P(3HB-co-4HB)의 열적 특성 특히, 결정화 거동에 영향을 미쳐 결정화 온도 증가와 함께 결정화도 감소를 초래한다. 하지만 혼합물은 높은 4HB 함량에도 결정성 P(3HB-co-4HB)와 유사한 결정화 거동을 보이며 이는 상대적으로 높은 혼합물의 열안정성에 의한 결과로 해석할 수 있다.
A small amount of thermal degradation reduces melt viscosity and increases the tan ¥ä. Poly(3-hydroxybutyrate-co-4-hydroxybutyrate) (P(3HB-co-4HB)) mixtures having similar 4-hydroxybutyrate (4HB) content show a small change in rheological properties due to better thermal stability of non-crystalline P(3HB-co-4HB) in the mixtures. Thermal degradation affects the crystallization behavior of P(3HB-co-4HB) and their mixtures in lowering crystallization temperature and decreasing crystallinity.
Keywords: poly(3-hydroxybutyrate-co-4-hydroxybutyrate), thermal degradation, rheological properties, crystallization.
저자(들)는 이해상충이 없음을 선언합니다.
Poly hydroxy alkanoate(PHA)는 다양한 환경에서 생분해성과 생체적합성을 가지며 생분해성 고분자가 갖지 못하는 고분자 성형품이 가져야할 물성을 동시에 유지할 수 있는 aliphatic polyester이다. 특히, 최근 부각되고 있는 고분자 폐기물에 의한 지구환경 오염 문제를 해결할 수 있는 대체 고분자 소재로 인식되어 이에 대한 관심이 커지고 있다.1-3 PHA는 hydroyalkanoic acid를 단량체로 갖는 미생물에 의하여 생성되는 aliphatic polyester로 물성 조절을 위하여 다양한 단량체를 사용하여 공중합체로 만들어지고 있다.4-6 다양한 물성을 갖는 PHA 공중합체를 제조하기 위해서는 단량체와 그 조성비를 조절하는 방법을 들 수 있으나 상업적으로 PHA를 대량 생산하는 경우, 미생물에 의하여 만들어 지는 이들의 제조 특성상 공중합체의 조성비를 다양하게 조절하기가 매우 어렵다. 이를 해결하는 방안으로 미생물이 만든 일정 조성비를 갖는 PHA 공중합체를 이용한 용융 혼합이 대안으로 제시되고 있으나 용융가공 시 발생하는 열분해가 고려되어져야 한다.
생분해성 aliphatic polyester는 미생물 혹은 화학적 가수화 반응에 의하여 광범위한 환경조건에서 분해가 일어나지만 이러한 생분해성으로 인하여 기존 상업적 고분자에 비하여 열에 매우 약하여 열분해를 초래하며7,8 이는 섬유 및 필름 제조를 위한 용융 가공에 문제점으로 인식되고 있다.9,10 P(3HB)는 180 oC 이상의 용융가공에서 열안정성이 매우 취약하여 분자량이 급격이 감소하는 현상을 보여 생분해성 연구와11,12 함께 열분해 연구가13 함께 진행되어 왔다. P(3HB) 열분해는 β-elimination에 의한 random degradation에14,15 의하여 일어나는 것으로 알려져 있다. P(3HB)와 비교하여 사슬에 존재하는 메틸렌기로 주사슬간 거리가 상대적으로 넓은 구조적 차이점에 의하여 사슬 유연성이 증가하여 고무적인 우수한 신율을 가지는 poly(4-hydroxybutyric acid)(P(4HB))도 random degradation에 의하여 열분해가 일어난다. 열분해에 의하여 생성된 -OH 말단기에 의하여 cyclization과 unzipping trans- esterification에 의하여 열안정성이 P(3HB)와 비교하여 개선되는 것으로 알려져 있다.16
최근 P(3HB)의 brittle한 물성 개선을 위하여 poly(3-hydroxybutyrate-co-4-hydroxybutyrate) P(3HB-co-4HB)에 대한 연구가17-19 진행되고 있다. 이들 연구에 따르면 P(3HB-co-4HB)는 3HB와 4HB 사슬 열분해가 β-elimination에 의한 random degradation, cyclization 그리고 transesterification이 함께 일어나는 매우 복잡한 특성을 가지는 것으로 알려져 있다. 이러한 분해 메커니즘은 용융 가공으로 얻어지는 P(3HB-co-4HB)의 섬유와 필름 물성에 영향을 미칠 것으로 예상된다.
본 연구에서는 4HB 함량이 다른 P(3HB-co-4HB)와 이들 혼합물의 열분해에 따른 가공 특성 변화를 살펴보았다. 고분자 용융 가공 온도가 P(3HB-co-4HB) 열분해 특성, 유변 특성, 결정화 거동에 미치는 영향을 중점적으로 확인하여 보았다. 이와 함께 결정성 P(3HB-co-4HB)와 비결정성 P(3HB-co-4HB) 혼합물의 열분해에 의한 물성 변화도 함께 살펴보았다.
재료 및 시편 제조. 본 연구에서는 Figure 1의 화학구조를 갖는 3-hyroxybutylate(3HB)와 4-hyroxybutylate(4HB)로 구성된 random copolymer인 생분해성 P(3HB-co-4HB)(PHA)를 CJ 제일제당에서 공급받아 사용하였다. 이들의 4HB 함량과 분자량 그리고 분자량분포를 Table 1에 나타내었다. 결정성 PHA10과 비결정성 PHA53 혼합물 제조는 internal mixer (Haake; Rheomix600, USA)를 이용하여 열분해를 최소화하기 위하여 140 oC에서 20 rpm으로 10분 동안 용융 혼합하여 혼합물 조성비를 9/1-4/6 범위로 제조하였다. 혼합물과 같은 열이력을 부여하기 위하여 각각의 PHA도 같은 조건으로 용융하여 시료로 함께 사용하였다. 열분해에 따른 유변특성 측정 시편 제조를 위하여 PHA와 이들 혼합물은 compression molding machine(QMESYS: QM900A, Korea)을 이용하여 140 oC에서 2분 동안 preheating한 뒤 압력을 8 MPa까지 올려 2분간 compression molding을 진행한 뒤 수조에 넣어 급랭하여 1T 두께의 필름을 제조하였다.
P(3HB-co-4HB) 물성 측정. PHA와 이들 혼합물의 열분해 특성을 확인하기 위하여 열중량분석기(TA Q50, USA)를 25 oC에서 500 oC까지 가열하여 질량 변화가 일어나는 onset 열분해 온도를 측정하였다. 또한 160, 180, 200 oC에서 20분 동안 등온과정에서의 질량 변화를 함께 살펴보았다. PHA와 PHA 혼합물의 열분해에 따른 점도 변화를 확인하기 위하여 얻어진 필름을 지름 25 mm의 시편으로 제작하여 회전식 점탄성 측정기(TA AR200EX, USA)를 이용하여 oscillation 방식에 의하여 유변 특성을 측정하였다. 전단속도를 10 rad/sec로 고정시키고 %strain을 160 oC에서 3 그리고 180, 200 oC에서 5로 설정하여 시간에 따른 complex viscosity(η*)와 loss tangent(tan δ)의 변화를 확인하였다. 시차열분석기(TA Q20, USA)를 이용하여 PHA와 이들 혼합물의 용융가공 온도가 열적 특성에 미치는 영향을 확인하였다. DSC 1차 승온 과정에서 최대온도(가공온도)로 160, 180, 200 oC까지로 승온하고 이를 다시 냉각한 후 2차 승온하여 이들의 유리전이온도 변화, 결정화 거동과 용융거동 변화를 확인하였다. 이때 승온 및 감온 속도는 각각 20 oC/min였다.

|
Figure 1 Chemical structure of poly(3-hydroxybutylate-co-4- hydroxybutylate). |
|
Table 1 4HB Contents and Molecular Weight of PHA Used in This Study |

*P(3HB-co-4HB) used for mixture preparation. |
Figure 2에 PHA와 이들 혼합물의 4HB 함량 증가에 따른 onset 열분해 온도 변화를 나타내었다. 그림에서 보는 바와 같이 PHA와 이들 혼합물 모두 4HB 함량이 증가됨에 따라 열분해 온도가 증가함을 알 수 있다. 모든 시료는 혼합물 여부와 상관없이 4HB 함량에 따라 열분해 온도가 선형적으로 증가되는 특성을 보이며 이는 4HB 함량 증가에 의하여 PHA의 열안정성이 개선됨을 의미한다.
Iwata 등의 연구에서18 확인된 바와 같이 PHA의 열분해는 random degradation에 의하여 unzipping β elimination 반응을 통해 oligomer형태의 Cr-3HB, Bu-3HB, Cr-4HB, Bu-4HB 등이 형성된다.19 Cr-3HB, Bu-3HB는 crotonic acid 혹은 3-butenoic acid를 형성하여 3HB의 unzipping β elimination반응을 촉진하여 열분해를 증가시킨다. 반면, 4HB에서 분해된 Cr-4HB, Bu-4HB가 갖고 있는 methylene기에 의하여 3HB의 unzipping β elimination반응을 정지시켜 열분해를 감소시킨다. 아울러 -OH 말단기를 갖는 분해된 4HB는 cyclization과 intermolecular transesterification 반응이 진행되어 γ-butyro- lactione이 만들어져 PHA의 열안정성이 개선되는 것으로 알려져 있다.20 이러한 메커니즘에 의하여 본 연구에서 사용된 PHA와 이들 혼합물은 4HB 함량 증가에 의하여 열안전성이 개선됨을 알 수 있다.
가공 온도와 시간과 같은 용융 가공조건이 열안정성에 미치는 영향을 확인하기 위하여 Figure 3에 PHA와 이들 혼합물을 160, 180, 200 oC에서 20분동안 TGA에 등온 체류시켜 thermogram을 얻어 이들의 질량 변화를 4HB 함량에 따라 나타내었다. PHA는 그림에서 보는 바와 같이 가공온도가 증가됨에 따라 열분해에 의하여 4HB 함량 35.6%까지는 최대 3%의 질량 감소가 일어나며 4HB 함량이 53.7%에서는 열분해에 의한 질량 감소가 다시 현저히 작아 짐을 알 수 있다. 이러한 현상은 Figure 2의 4HB 함량 증가에 따른 열안정성 증가와는 매우 다른 결과이다. 용융가공에서 사용하는 가공온도는 Figure 2의 PHA의 최소 onset 열분해 온도 265 oC 보다 현저히 낮고 4HB 함량이 적어 unzipping degradation에 의하여 3HB 분해를 억제하는 4HB의 Cr-4HB, Bu-4HB 분해가 용이하지 않으며 따라서 분해된 4HB 사슬 간의 cyclization과 transesterification에 의한 열안정성 증가도 기대하기 어렵다. 오히려 4HB가 3HB에 비하여 상대적으로 약한 사슬 결합력을 가지고 있어 4HB 함량 증가에 의한 열분해가 증가됨을 보인다. 하지만 4HB 함량이 3HB 함량보다 많아지는 4HB 함량 53.7% 이상에서는 4HB 분해에 의한 Cr-4HB, Bu-4HB 형성될 가능성이 상대적으로 높아 random degradation 감소와 cyclization과 intermolecular transesterification에 의하여 열안정성이 다시 증가되는 것으로 해석할 수 있다.21,22
PHA 혼합물의 경우 PHA와 마찬가지로 낮은 가공 온도에서는 열분해에 의한 질량 감소가 거의 없으나 가공온도가 증가하면 열분해가 증가됨을 보인다. 순수 PHA와 비교하여 180 oC와 200 oC에서의 열분해에 의한 질량 감소가 현저히 적은 것으로 보아 혼합물에서 4HB 함량 증가에 의한 열안정성이 개선됨을 보여준다. 이러한 현상은 PHA 혼합물의 열분해 특성은 혼합물에 포함된 열안정이 우수한 비결정성 PHA53 함량에 의존적이기 때문으로 판단된다.
Figure 4에 Figure 3의 적은 양의 열분해가 complex viscosity와 tan δ에 미치는 영향을 확인하기 위하여 PHA10과 PHA53을 같은 전단속도에서 160-200 oC로 30분간(가공시간) 체류시켜 complex viscosity와 tan δ의 변화를 확인하였다. 160 oC에서는 PHA10은 Figure 3에서 확인된 바와 같이 열분해가 거의 없어 이에 따른 점도 변화가 크지 않으나 180 oC에서는 소량의 질량 감소에도 점도가 현저하게 감소됨을 알 수 있으며 열분해가 가장 많이 일어나는 200 oC에서 점도 감소가 가장 많이 일어남을 알 수 있다. 이러한 점도 감소는 가공시간이 증가함에 따라 더 확연하게 나타남을 알 수 있었다. PHA53의 경우, 180 oC와 200 oC에서 PHA10에 비하여 점도 감소가 개선되며 이는 상대적으로 높은 분자량과 Figure 3에서 확인된 4HB 함량 증가에 따른 열안정성 증가에 기인된 결과이다. 이러한 결과로부터 용융온도 근처에서 가공온도를 증가시키면 PHA는 4HB 함량 증가에 의하여 열분해가 일어나 용융점도를 감소시키는 요인이 되나 4HB 함량이 3HB보다 많아지면 앞에서 언급된 분해 메커니즘에 의하여 열안정성이 개선되어 점도 감소가 작아 짐을 알 수 있다.
Figure 4(b)에 가공온도와 시간에 따른 tan δ의 변화를 나타내었다. 그림에서 보는 바와 같이 가공온도 증가에 의한 complex viscosity 감소는 tan δ를 증가시킴을 알 수 있다. 특히 200 oC 가공에서는 tan δ가 급격히 증가하다 일정 시간 후 감소함을 보인다. tan δ는 melt strength에 반비례함에23 따라 용융가공에 의한 열분해는 complex viscosity 감소와 함께 melt strength를 감소시켜 PHA10의 용융 가공성을 현저하게 떨어뜨림을 알 수 있다. 따라서 PHA의 열분해에 의한 가공성 저하를 최소화하기 위해서는 되도록 저온에서 4HB함량이 많은 비결정성 PHA를 사용하는 것이 좋을 것으로 판단된다. 이상의 결과로부터 200 oC의 용융가공은 열분해에 의한 매우 심한 점도 감소와 이에 따른 tan δ 변화에 따라 용융가공 조건으로 적절하지 않음을 알 수 있다.
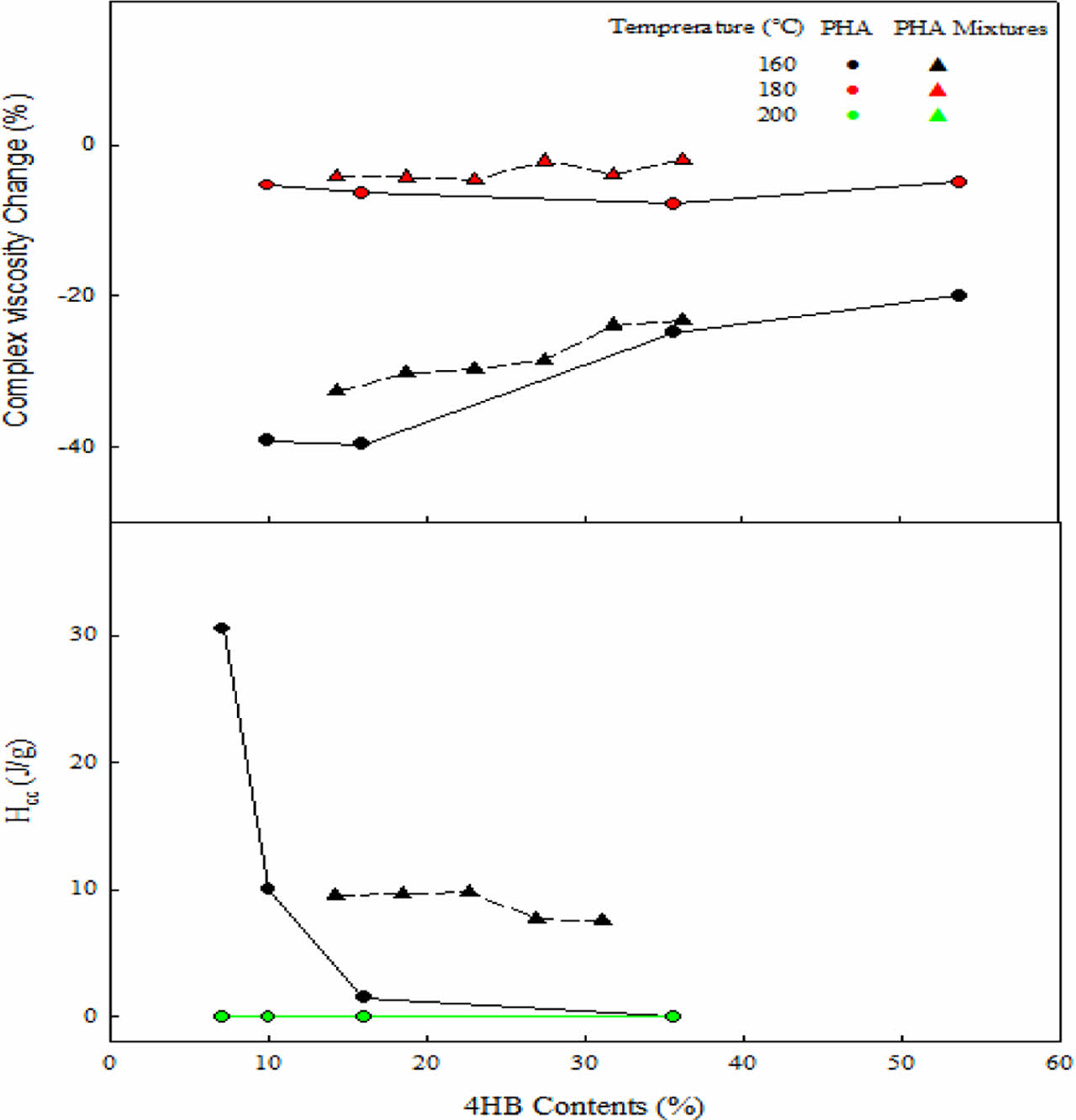
Figure 5(a)에 PHA와 이들 혼합물의 적정 용융 가공 조건인 160, 180 oC에서 4HB 함량에 따른 complex viscosity와 tan δ 변화를 나타내었다. PHA의 경우, 160 oC에서는 4HB 함량에 관계없이 7-10% 정도의 점도 감소를 보인다. 180 oC에서는 4HB 함량이 낮은 PHA10에서 40% 정도의 점도 감소를 보이나 4HB 함량 증가에 의하여 점도 감소가 20%로 현저히 감소됨을 알 수 있다. 즉, 180 oC 가공에서는 열분해에 의한 점도 감소를 초래하나 PHA의 4HB 함량 증가에 의하여 이러한 점도 감소를 최소화할 수 있음을 알 수 있다.
PHA 혼합물의 경우도 유사한 특성을 보이고 있으며 PHA에 비하여 가공 온도에 따른 점도 변화가 상대적으로 적으며 PHA와 마찬가지로 4HB 함량 증가에 따라 점도 감소가 줄어 듬을 알 수 있다. 이는 PHA와는 달리 혼합물에서의 4HB 함량 증가는 열안정성이 PHA10에 비하여 우수한 PHA53 사슬에 포함되어 증가되기 때문이다.
Figure 5(b)에 가공온도가 tan δ에 미치는 영향을 함께 나타내었다. 가공온도 증가에 의하여 loss tangent가 증가하여 가공 특성을 감소시킴을 알 수 있다. 특히, 4HB 함량 증가에도 점도 변화가 거의 없었던 160 oC에서도 tan δ의 변화가 일어나며 180 oC에서는 tan δ의 증가가 최대 10배까지 높아짐을 알 수 있다. 이러한 tan δ의 변화는 4HB 함량이 35.6%까지는 증가되며 4HB 함량 53.7%에서는 다시 감소함을 알 수 있다. tan δ의 증가는 PHA의 melt strength 감소를 의미하며 따라서 PHA의 가공 안정성이 떨어짐을 의미한다. 이러한 결과로부터 PHA는 낮은 온도에서 4HB 함량이 3HB보다 많은 공중합체 조성비에서 우수한 가공 특성을 보일 것으로 판단된다.
혼합물의 경우는 160 oC 가공에서는 4HB 함량 증가에도 tan δ의 변화가 없어 가공성에는 변화가 없음을 알 수 있으며 180 oC에서는 4HB 함량이 증가되면 전 조성비에서 tan δ의 감소 즉, 가공성 증가를 확인할 수 있으며 PHA에 비하여 가공온도에 따른 tan δ의 변화가 현저히 적음을 알 수 있다. 이러한 결과로부터 PHA는 가공 온도 증가와 이에 따른 열분해에 의하여 가공성이 현저히 감소되나 PHA 혼합물의 경우, PHA53 함량 증가에 의하여 열분해를 최소화하여 180 oC 가공온도에서 가공특성을 현저히 개선할 될 수 있을 것으로 판단된다.
Figure 6과 Figure 7에 PHA와 이들 혼합물을 최대 승온 온도(가공온도)를 180 oC와 200 oC로 올린 후 냉각과 2차 승온하여 DSC thermogram을 나타내었다. 그림에서 보는 바와 같이 4HB 함량이 많은 PHA35와 PHA53은 가공온도와 관계없이 냉각과정에서 결정화 관련 피크가 나타나지 않는다. 그 결과, 승온과정에서 용융 피크도 나타나지 않는 것으로 보아 비결정성 PHA임을 알 수 있다. 상대적으로 4HB 함량이 낮은 PHA의 경우 20 oC의 가공 온도 차이에 의하여 DSC의 냉각 thermogram이 현저히 달라짐을 알 수 있다. 그림에서 보는 바와 같이 180 oC까지 가열한 경우, 4HB 함량이 16%까지는 냉각과정에서 결정화에 의한 결정화 엔탈피를 보이는 반면, 가공온도를 200 oC로 증가시키면 모든 공중합체에서 결정화 엔탈피는 사라지며 4HB 함량 10%까지의 공중합체에서 2차 승온과정에서 냉결정화 피크가 나타남을 알 수 있다. 이는 가공온도 증가에 따른 열분해에 의하여 PHA 결정화 거동이 변화됨을 의미한다. DSC 냉각과정에서 결정화 온도가 사라지는 현상은 같은 냉각조건에서 가공온도에 따른 열분해에 의하여 PHA의 결정화가 어려워지는 것을 의미한다. 2차 승온과정에서 나타나는 냉결정화 피크는 열분해에 따라 결정화가 어려워 냉각과정에서 형성된 완전하지 못한 결정들이 DSC의 가열과정에서 받은 열이력에 의하여 보다 완벽한 결정으로 변화되어 생기는 결정화 엔탈피의 변화로 해석할 수 있다.
가공온도에 따른 용융피크의 변화를 살펴보면 4HB 함량이 가장 많은 결정성 PHA16의 200 oC 가공을 제외하고 double melting peak가 나타남을 알 수 있다. Double melting peak는 PHA의 냉각과정에서 random 공중합체인 PHA의 4HB rich phase와 3HB rich phase에 생겨나는 각각의 결정 용융 엔탈피에 기인된다.23,24 즉, 4HB 함량이 증가되거나 200 oC의 가공에서 열분해에 의한 저분자 PHA 함량 증가에 따라 형성된 공중합체의 4HB rich phase에서 불완전한 결정이 형성되고 불완전한 결정이 recrystallization에 의해서 보다 완전한 결성이 형성되기 때문이다. PHA16의 경우 높은 4HB 함량에 의하여 결정화도가 상대적으로 낮으며 가공온도 200 oC의 경우, 열분해로 인하여 결정화가 더욱 더 어려워져 double melting peak의 형성이 어려움을 알 수 있다.
혼합물의 경우, Figure 7에서 보는 바와 같이 180 oC 가공에서는 혼합비에 따라 차이는 있지만 조성비에 관계없이 냉각과정에서 결정화 피크가 모두 나타나는 반면 200 oC에서는 결정화 피크가 모두 사라지고 승온 과정에서의 냉결정화 피크가 4HB 조성비에 상관없이 모두 나타남을 보인다. 혼합물 조성비에 따라 다소 차이는 나지만 이러한 결정화 거동은 혼합물에 포함된 PHA10과 유사함을 보인다. 용융 피크의 경우, 가공온도에 관계없이 double melting peak를 보여 4HB 함량이 많은 PHA53의 조성비가 증가함에 따라, 가공온도가 증가함에 따라 이러한 현상이 두드러짐을 알 수 있다.
Figure 8에 PHA와 이들 혼합물의 가공온도에 따른 유리전이온도의 변화를 나타내었다. 그림에서 보는 바와 같이 상대적으로 유연한 4HB 사슬 함량이 증가됨에 따라 유리전이 온도가 감소됨을 보인다. 비결정성 주사슬의 온도에 따른 움직임을 나타내는 유리전이온도는 PHA의 4HB 함량이 낮아 결정영역이 많은 경우 유리전이온도가 높게 나타나며 4HB 함량 증가에 따라 결정영역이 적어 지면 상대적으로 유연한 4HB 사슬에 의하여 유리전이온도가 낮아짐을 보인다. 하지만 160-200 oC 범위의 가공온도는 유리전이온도에 크게 영향을 미치지 못함을 알 수 있다. 이는 열분해는 Figure 6과 Figure 7에서 확인된 바와 같이 PHA의 결정화 거동에는 매우 민감하게 영향을 미치나 비 결정영역의 사슬 거동인 유리 전이온도에는 크게 영향을 미치지 못함을 알 수 있다.
PHA 혼합물의 경우, 결정성 PHA10과 비결정성 PHA53이 혼합되어 있어 두 개의 유리전이온도를 보인다. 이는 3HB와 4HB로 이루어져 2개의 유전이온도를 갖는 공중합체가 갖는 특성이다. 하지만 4HB 조성비의 증가에 따라 작지만 PHA10에 기인되어는 5 oC 근방의 유리전이온도는 감소되고 PHA53에 해당되는 -25 oC 근방의 유리전이온도는 증가된다. 이는 용융 혼합이 이들 유리전이온도에 다소간의 영향이 존재함을 알 수 있다. 반면, 본 연구에서 사용한 가공온도는 혼합물의 유리전이온도의 변화는 크게 영향을 미치지 않음을 알 수 있다. 본 연구진의 PHA 물성 연구에서23 혼합물의 최대 승온 온도를 250 oC로 하였을 경우, PHA10과 PHA53에 기인되는 유리전이온도는 단일 유리전이온도를 나타내어 비 결정영역의 상분리는 가공온도를 증가시키면 개선될 수 있음을 알 수 있다.
열분해가 PHA 결정화 거동에 미치는 영향을 확인하기 위하여 Figure 9에 PHA와 이들 혼합물의 가공온도에 따른 결정화 온도와 엔탈피의 변화를 나타내었다. PHA는 4HB 함량과 가공온도가 증가됨에 따라 결정화 온도는 감소되며 200 oC 가공에서는 냉각속도 20 oC/min에서 냉각과정에서는 결정화가 전혀 일어나지 않음을 알 수 있다. 이는 random copolymer인 PHA에 4HB 함량 증가는 사슬의 불규칙성을 더 증가시키고 그 결과, 결정화가 어려워짐에 따른 결과로 해석할 수 있다. 가공온도 증가에 따른 결정화 온도 감소는 Figure 3에서 확인된 열분해로 인하여 생긴 저분자 PHA가 결정 형성을 어렵게 함을 의미한다. 결정화 엔탈피의 경우, 결정화 온도와 같은 이유에서 4HB 함량에 증가에 따라 결정 엔탈피는 감소되나 가공온도가 160 oC에서 180 oC로 증가됨에 따라 결정화 엔탈피는 증가됨을 보인다. 열분해에 영향을 적게 받는 160 oC 가공에서의 결정화 엔탈피가 열분해에 의하여 결정화가 어려울 것으로 예측되는 180 oC에 비하여 결정화 엔탈피가 적은 이유는 160 oC 가공에서 냉각과정에서 일어나는 상대적으로 높은 결정화 온도에 따른 결과로 해석 가능하다. 아래 식 (1)의 classical nucleation theory(CNT)에24 의하여 critical size of nucleus(r*, embryo)형성은 용융 온도와 결정화 온도의 차(ΔT=Tm-Tc)로 설명할 수 있다.

여기서 σ는 단위면적당 결정형성 생성 에너지, ΔH는 엔탈피 변화를 나타낸다.
180 oC 가공보다는 160 oC 가공에서의 결정화 온도가 용융 온도에 더 근접됨에 따라 ΔT 가 작아지고 그 결과, embryo가 커짐에 따라 결정 형성이 어려워 결정화 엔탈피가 상대적으로 작아지게 된다. 보다 상세한 가공온도에 따른 결정화거동을 확인하기 위해서는 가공온도가 결정화속도에 미치는 영향에 대한 추가적인 연구가 필요할 것으로 판단된다.
혼합물의 경우, PHA와는 달리 혼합에 의하여 얻어진 모든 4HB 함량 범위에서 결정화가 일어남을 알 수 있다. 이는 PHA와 달리 4HB 사슬이 결정 가능한 PHA10에 존재하여 4HB 함량이 16% 이상에서도 냉각에 의한 결정화가 일어남을 알 수 있다. 4HB 함량에 따른 결정화 온도 및 엔탈피의 감소는 PHA에 비하여 심하지 않음을 알 수 있다. 이러한 현상은 4HB 함량 증가가 공중합체의 randomness에 영향을 미치지 않고 혼합물의 PHA10 domain에 존재하는 PHA53의 co-domain에 의하여 PHA의 결정 형성에 방해를 받음을 알 수 있다. PHA와 마찬가지로, 가공온도 증가에 의한 열분해에 의하여 결정화온도는 감소하며 결정화 엔탈피는 증가함을 보인다. 하지만 4HB 함량에 따른 변화는 4HB 사슬의 유연성이 상대적으로 적을 것으로 예상되는 160 oC에서 확인되지 않고 PHA10과 유사한 결정화 거동을 보이나 사슬의 유연성이 증가된 180 oC에서는 4HB 함량 증가에 따라 결정화온도 및 엔탈피가 감소됨을 알 수 있다.
Figure 10에 PHA와 PHA 혼합물의 가공온도에 따른 용융 온도와 용융 엔탈피의 변화를 나타내었다. 그림에서 보는 바와 같이 가공온도와 4HB 함량에 따라 용용온도와 엔탈피가 달라짐을 알 수 있다. PHA는 random 공중합체로 4B 함량에 따라 3HB rich phase와 4HB rich phase가 존재한다. Figure 10(a)에서 보는 바와 같이 상대적으로 낮은 온도에서 4HB rich phase의 결정 용융에 의한 용융온도(Tm1)가 나타나며 이보다 높은 온도에서 3HB rich phase의 결정 용융에 의한 용융온도(Tm2)가 나타난다. 3HB rich phase의 결정 그리고 4HB phase 결정 모두 가공온도가 증가됨에 따라 그리고 4HB 함량이 증가됨에 따라 감소함을 보인다. 가공온도가 200 oC로 열분해가 많이 일어나며 4HB 함량도 16%로 높은 경우 상대적으로 불완전한 4HB rich phase의 결정이 사라짐을 알 수 있다. 이러한 결과로부터 4HB 함량 증가에 의하여 형성되는 결정이 열역학적 완전성이 감소되며 아울러 가공온도가 증가되면 열분해에 의한 저분자 PHA에 의하여 추가적으로 열역학적 결정 완전성 감소가 일어난다. 그 결과, Figure 10(b)에서 보는 바와 같이 4HB 함량 증가와 가공온도에 증가에 따른 용융 엔탈피 감소를 초래하게 된다. 160 oC 가공의 용융 엔탈피가 다른 가공온도 보다 낮은 이유는 Figure 9에서 확인된 바와 같이 낮은 결정화온도로 인하여 결정화과정에서 결정 형성이 다른 가공온도에 비하여 어렵기 때문으로 판단된다.
혼합물의 경우, PHA10과 같이 가공온도에는 상관없이 4HB rich phase와 3HB phase 모두에서 결정화 일어나며 혼합물의 4HB 함량에 따라 용융온도의 변화가 없으나 용융 엔탈피는 다소 감소함을 보인다. 가공온도가 증가되면 열분해에 의하여 용융온도와 용융 엔탈피의 변화를 보이나 그 변화 정도가 PHA에 비하여 매우 작음을 알 수 있다. PHA 혼합물에서의 결정화는 혼합물에 포함되어 있는 PHA10에 의하여 일어나며 같이 혼합되어 있는 비 결정성 PHA53은 형태학적으로는 PHA10의 결정화에 어려움을 주나 PHA에 포함되어 있는 4HB 사슬보다는 결정화에 미치는 영향이 적음을 알 수 있다. 따라서 혼합물의 용융 현상은 혼합물에 사용된 결정성인 PHA10의 용융거동과 매우 유사함을 알 수 있다. 이러한 결과로부터 PHA 공중합체에 비하여 혼합물은 가공온도에 따른 열분해에 의한 결정화 거동변화는 상대적으로 작음을 알 수 있다.

|
Figure 2 Onset degradation temperature (Td) of PHA and PHA mixtures. |

|
Figure 3 Weight loss of (a) PHA; (b) PHA mixtures by isothermal TGA thermogram. |

|
Figure 4 Effect of thermal degradation on (a) complex viscosity; (b) tan δ of PHA10 and PHA53. |

|
Figure 5 Change in rheological properties of PHA and PHA mixtures after melt processing at various processing temperature for 30 min: (a) complex viscosity; (b) tan δ. |

|
Figure 6 DSC thermograms (cooling and heating) of PHA having different processing temperature: (a) 180 oC; (b) 200 oC. |

|
Figure 7 DSC thermograms (cooling and heating) of PHA mixtures having different processing temperature: (a) 180 oC; (b) 200 oC |

|
Figure 8 Effect of processing temperature on glass transition temperature (Tg) of PHA and PHA mixtures. |

|
Figure 9 Effect of processing temperature on crystallization behavior of PHA and PHA mixtures: (a) cold crystallization temperature (Tc); (b) cold crystallization enthalpy (ΔHc). |

|
Figure 10 Effect of processing temperature on (a) melting temperature (Tm); (b) melting enthalpy (ΔHm) of PHA and PHA mixtures. |
P(3HB-co-4HB)는 180 oC 이상에서 열분해가 일어나며 이러한 열분해는 P(3HB-co-4HB)의 점도 감소와 loss tangent의 증가를 초래하여 용융 가공성을 저하시킴을 알 수 있었다. 4HB의 조성비가 3HB보다 많아지는 조성비에서 P(3HB-co-4HB)는 열분해가 최소화되어 열분해가 유변 특성 변화에 미치는 영향이 작아짐을 확인하였다. 이와는 달리 P(3HB-co-4HB) 혼합물은 같은 4HB 함량에서 P(3HB-co-4HB)보다 열분해가 적게 일어나 4HB 함량 변화가 가공특성에 미치는 영향이 적음을 알 수 있었다.
열분해는 P(3HB-co-4HB)와 이들 혼합물의 열적 특성에 영향 특히, 결정화거동에 영향을 미치며, 열분해에 의하여 결정화온도는 낮아지며 결정화 엔탈피는 높아짐을 알 수 있다. 200 oC의 가공은 본 연구에서 사용한 냉각조건에서 결정화가 완벽하게 일어나지 못하여 승온 과정에서의 냉결정화에 의하여 재 결정화를 보임을 알 수 있다. 혼합물의 경우, 열분해에 의한 가공특성 변화 최소화와 함께 결정화거동 변화도 적어 용융가공 특성을 개선할 수 있을 것으로 판단된다.
- 1. Tsang, Y. F.; Kumar, V.; Samadar, P.; Yang, Y.; Lee, J.; Ok, Y. S.; Jeon, Y. J. Production of Bioplastic through Food Waste Valorization. Environ. Int. 2019, 127, 625-644.
-

- 2. Modi, S.; Koelling, K.; Vodovotz, Y. Assessment of PHB with Varying Hydroxyvalerate Content for Potential Packaging Applications. Eur. Polym. J. 2011, 47, 179-186.
-

- 3. Mohanty, A. K.; Misra, M.; Drzal, L. T. Sustainable Bio-composites from Renewable Resources: Opportunities and Challenges in the Green Materials World. J. Polym. Environ. 2002, 10, 19-26.
-

- 4. Mahishi, L. H.; Tripathia, G.; Rawala, S. K. Poly(3-hydroxy- butyrate) (PHB) Synthesis by Recombinant Escherichia coli Harbouring Streptomyces Aureofaciens PHB Biosynthesis Genes: Effect of Various Carbon and Nitrogen Sources. Microbiol. Res. 2003, 158, 19-27.
-

- 5. Doi, Y.; Mukai, K.; Kasuya, K.; Yamada, K. Biodegradation of Biosynthetic and Chemosynthetic Polyhydroxyalkanoates. J. Polym. Sci. 1994,12, 39-51.
-

- 6. Schubert, P.; Steinbüchel, A.; Schlegel, H. G. Cloning of the Alcaligenes Eutrophus Genes for Synthesis of Poly-beta-hydroxybutyric Acid (PHB) and Synthesis of PHB in Escherichia coli. J. Bacteriol. 1988, 170, 5837-5847.
-

- 7. Hong, S. G.; Hsu, H. W.; Ye, M. T. Thermal Properties and Applications of Low Molecular Weight Polyhydroxybutyrate. J. Therm. Anal. Calorim. 2013, 111, 1243-1250.
-

- 8. Aziz, M. S. A.; Saad, G. R.; Naguib, H. F. Non-isothermal Crystallization Kinetics of Poly(3-hydroxybutyrate) in Copoly(ester-urethane) Nanocomposites Based on Poly(3-hydroxybutyrate) and Cloisite 30B. Thermochim. Acta 2015, 605, 52-62.
-

- 9. Hong, S. G.; Lin, Y. C.; Lin, C. H. Crystallization and Degradation Behaviors of Treated Polyhydroxybutyrates. React. Funct. Polym. 2008, 68, 1516-1523.
-

- 10. Xu, C. L.; Qiu, Z. B. Crystallization Behavior and Thermal Property of Biodegradable Poly(3-hydroxybutyrate)/multi-walled Carbon Nanotubes Nanocomposite. Polym. Adv. Technol. 2011, 22, 538-544.
-

- 11. Kanesawa, Y.; Tanahashi, N.; Doi, Y.; Saito, T. Enzymatic Degradation of Microbial Poly(3-hydroxyalkanoates). Polym. Degrad. Stab. 1994, 45, 179-185.
-

- 12. Kumagai, Y.; Kanesawa, Y.; Doi, Y. Enzymatic Degradation of Microbial Poly(3‐hydroxybutyrate) Films. Die Makromol. Chem. 1992, 193, 53-57.
-

- 13. Kim, K. J.; Doi, Y.; Abe, H. Effects of Residual Metal Compounds and Chain-end Structure on Thermal Degradation of Poly(3-hydroxybutyric acid). Polym. Degrad. Stab. 2006, 91, 769-777.
-

- 14. Abate, R.; Ballistreri, A.; Montaudo, G.; Giuffrida, M.; Impallomeni, G. Separation and Structural Characterization of Cyclic and Open Chain Oligomers Produced in the Partial Pyrolysis of Microbial Poly(hydroxybutyrates). Macromolecules 1995, 28, 7911-7916.
-

- 15. Yun, O. Y.; Min, X.; Li, Y. Properties Analysis of Biodegradable Material P(3HB-co-4HB). Open J. Adv. Mater. Res. 2011, 380, 168-172.
-

- 16. Zhang, J. Q.; Kasuya, K.; Hikima, T.; Takata, M.; Takemura, A.; Iwata, T. Mechanical Properties, Structure Analysis and Enzymatic Degradation of Uniaxially Cold-drawn Films of Poly[(R)-3-hydroxybutyrate-co-4-hydroxybutyrate]. Polym. Degrad. Stab. 2011, 96, 2130-2138.
-

- 17. Chen, X.; Yang, X.; Pan, J.; Wang, L.; Xu, K. Degradation Behaviors of Bioabsorbable P3/4HB Monofilament Suture in vitro and in vivo. J. Biomed. Mater. Res. - Part B Appl. Biomater. 2010, 92, 447-455.
-

- 18. Omura, T.; Goto, T.; Maehara, A.; Kimura, S.; Abe, H.; Iwata, T. Thermal Degradation Behavior of Poly[(R)-3-hydroxybutyrate-co-4-hydroxybutyrate]. Polym. Degrad. Stab. 2021, 183, 109460-109468.
-

- 19. Kunioka, M.; Doi, Y. Thermal Degradation of Microbial Copolyesters: Poly(3-hydroxybutyrate-co-3-hydroxyvalerate) and Poly(3-hydroxybutyrate-co-4-hydroxybutyrate). Macromolecules 1990, 23, 1933-1936.
-

- 20. Kim, K. J.; Doi, Y.; Abe, H.; Martin, D. P. Thermal Degradation Behavior of Poly(4-hydroxybutyric acid). Polym. Degrad. Stab. 2006, 91, 2333-2341.
-

- 21. Wen, X.; Lu, X.; Peng, Q.; Zhu, F.; Zheng, N. Crystallization Behaviors and Morphology of Biodegradablepoly(3-hydroxy- butyrate-co-4-hydroxybutyrate). J. Therm. Anal. Calorim. 2012, 109, 959-966.
-

- 22. Norhafini, H.; Huong, K. H.; Amirul, A. A. High PHA Density Fed-batch Cultivation Strategies for 4HB-rich P(3HB-co-4HB) Copolymer Production by Transformant Cupriavidus Malaysiensis USMAA1020. Int. J. Biol. Macromol. 2019, 125, 1024-1032.
-

- 23. Jo, M.; Jang, Y.; Lee, E.; Shin, S.; Kang, H. J. The Modification of Poly(3-Hydroxybutyrate-co-4-hydroxybutyrate) by Melt Blending. Polymers 2022, 14, 1725-1737.
-

- 24. Krüger, S.; Deubener, J. Lag Time to Crystal Nucleation of Supercooled Lithium Disilicate Melts: A Test of the Classical Nucleation Theory. J. Non Cryst. Solids 2015, 426, 1-6.
-

- Polymer(Korea) 폴리머
- Frequency : Bimonthly(odd)
ISSN 0379-153X(Print)
ISSN 2234-8077(Online)
Abbr. Polym. Korea - 2023 Impact Factor : 0.4
- Indexed in SCIE
 This Article
This Article
-
2022; 46(6): 757-765
Published online Nov 25, 2022
- 10.7317/pk.2022.46.6.757
- Received on Jun 2, 2022
- Revised on Aug 4, 2022
- Accepted on Aug 25, 2022
 Services
Services
Shared
 Correspondence to
Correspondence to
- Ho-Jong Kang
-
Department of Polymer Science and Engineering, Dankook University, 152 Jukjeon-ro, Suji-gu, Yongin-si, Gyeonggi-do 16890, Korea
- E-mail: hjkang@dankook.ac.kr
- ORCID:
0000-0001-8411-3667









 Copyright(c) The Polymer Society of Korea. All right reserved.
Copyright(c) The Polymer Society of Korea. All right reserved.