- Formulation Design of Sustained-release Dosage form of Ticagrelor by Solid Dispersion Using Eudragit RS/RL
Byungkwan Moon*, Younghun Lee*, Seung Jae Kim*, Suyoung Been*, Na Eun Kim*, Seong Won Lee*, Sunjae Park*, Jeong Eun Song*, and Gilson Khang*, **, ***,†

*Department of Bionanotechnology and Bio-Convergence Engineering, Jeonbuk National University, 567 Baekje-daero, Deokjin-gu, Jeonju-si, Jeollabuk-do 54896 Korea
**Department of Polymer Nano Science & Technology, Jeonbuk National University, 567 Baekje-daero, Deokjin-gu, Jeonju-si, Jeollabuk-do 54896 Korea
***Polymer Materials Fusion Research Center, Jeonbuk National University, 567 Baekje-daero,
Deokjin-gu, Jeonju-si, Jeollabuk-do 54896 Korea- Eudragit RS/RL을 이용한 고체분산에 의한 티카그렐러 서방형 제형 설계
문병관* · 이영훈* · 김승재* · 빈수영* · 김나은* · 이성원* · 박선재* · 송정은* · 강길선*, **, ***,†

*전북대학교 바이오나노융합공학과, **전북대학교 고분자나노공학과, ***전북대학교 고분자융합소재연구소
Reproduction, stored in a retrieval system, or transmitted in any form of any part of this publication is permitted only by written permission from the Polymer Society of Korea.
Ticagrelor is a drug that prevents stroke and heart attack in patients with acute coronary syndrome and belongs to the biopharmaceutical classification system IV with low solubility and permeability. Therefore, in order to increase the bioavailability, the drug solubilization process is essential. To this end, a solid dispersion was produced through a wet granulation process by a spray-drying method using hydrophilic and pH-independent polymers Eudragit RL PO and Eudragit RS PO. Crystallinity and saturation were confirmed through X-ray diffractometer and differential scanning calorimetry whether the drug was dispersed in a polymer matrix in an amorphous form, and a chemical change was confirmed through Fourier transform infrared spectroscopy. Finally, it was confirmed that the release control of the drug was well performed through the dissolution test, and it was possible to develop a formulation that reduced the number of doses and improved the patient's compliance with the dose.
티카그렐러는 급성관상동맥증후군 환자의 뇌졸중과 심장마비를 예방하는 약물로서 용해도와 생체막 투과성이 낮은 생물약제학적 분류체계 IV에 속하는 약물이다. 이에 생체이용률을 높이기 위해서는 약물가용화 과정이 필수적이다. 이를 위해 친수성이고 pH 비의존적 고분자 Eudragit RL PO, Eudragit RS PO을 사용해 분무건조법으로 습식과립공정을 통해 고체 분산체를 제조하였다. 약물이 무정형으로 고분자 매트릭스에 분산되었는지 X-ray diffractometer, differential scanning calorimetry를 통해 결정성 및 포접을 확인하였고, Fourier transform infrared spectroscopy을 통해 화학적 변화를 확인하였다. 최종적으로, 용출시험을 통해 약물의 방출제어가 잘 이루어졌는지 확인하여, 복용 회수를 줄이고 환자의 복약 순응도를 높인 제형으로 개발 가능함을 확인하였다.
Ticagrelor is a drug that prevents stroke and heart attack in patients with acute coronary syndrome and belongs to the biopharmaceutical classification system ¥³ with low solubility and permeability. Therefore, in order to increase the bioavailability, the drug solubilization process is essential. To this end, a solid dispersion was produced through a wet granulation process by a spray-drying method using hydrophilic and pH-independent polymers Eudragit RL PO and Eudragit RS PO.
Keywords: ticagrelor, solid dispersion, wet granulation, eudragit, sustained release.
본 연구는 과학기술정보통신부의 재원으로 한국연구재단의 지원(NRF-2021K1A3A1A78097905)을 받아 수행된 국제화기반조성사업의 지원으로 수행되었다.
저자(들)는 이해상충이 없음을 선언합니다.
급성관상동맥증후군(acute coronary syndrome, ACS)은 관상동맥 내에 급성으로 생긴 혈전으로 인해 혈관이 폐쇄되거나 혈전에서 분비되는 혈관 수축성 물질들로 인해 관상동맥 폐쇄가 일어나고 이로 인해 심장에 혈류 공급이 부족해지고 심근경색까지 이르게 되는 질환이다.1
P2Y12는 G-protein-coupled receptor(GPCR)에 속하는 ADP에 대한 화학 수용체로서 혈소판 표면에서 주로 나타나며 혈액응고의 중요한 조절인자로 알려져 있다.2
이러한 P2Y12 차단제(ADP receptor inhibitor)로 클로피도그렐과 티카그렐러 등의 약물이 급성관상동맥증후군의 1차 치료제로 많이 쓰이고 있다.3,4
티카그렐러와 클로피도그렐 두 약물의 생화학적 및 생리학적 효과와 작용기전에 대한 연구에서 티카그렐러는 더 빠르고 강한 혈소판 응집 억제를 보였으며 지속적인 약효 측면에서 더 안정적인 경향을 보였다.5
또한 최근 티카그렐러 단독치료 요법군의 다른 치료에 비해 치명적인 주요출혈을 줄여 궁극적인 총 임상적 이득 NACE (net adverse clinical events) benefit 은 NACB을 얻을 수 있는 연구 결과도 나왔다.6 하지만, 티카그렐러는 생물약제학적 분류체계(Biopharmaceutics Classification System, BCS) IV 등급에 해당하는 약물로 약물의 용해도와 장관 투과도가 낮다. 따라서 티카그렐러 약물의 효율적인 전달 시스템에 관한 연구가 활발히 진행 중이다.7-9
본 연구에서는 용출률을 향상시키고 지속적 약물 방출을 통해 환자의 복용 횟수를 줄이기 위해 분무건조기를 사용하여 티카그렐러와 매트릭스로 사용될 수용성 고분자 Eudragit RL PO(C11H21NO4), Eudragit RS PO(C19H34ClNO6)에 약물을 포접시켜 고체분산체를 제조하였다. Eudragit RL과 RS는 아크릴과 메타크릴산 에스터로 공중합된 고분자로서 물에 대한 투과도가 pH에 영향을 받지 않고 팽윤되지 않는 특성을 가진다.10 아크릴-메타크릴산 에스터 계열 고분자들은 이러한 특성을 지녀 서방형 약물 방출을 목적으로 한 제형에 많이 쓰이고 있다. 분무건조 방법은 용매에 고분자와 약물을 혼합시켜 고온에서 분사시키는 방법으로 이 때 약물이 고분자 매트릭스에 포접하게 된다. 이렇게 포접된 약물은 결정형이 아닌 무결정 상태로 포접되기 때문에 물에 대한 용해도가 증가하며 체내에서 흡수가 용이하다.11 또한 제조한 고체분산체의 흐름성을 개선하기 위해 습식과립공정을 통해 과립물을 형성하였으며 결합제, 붕해제와 같은 부형제를 첨가하여 결합액을 분사한 뒤 건조하여 과립을 제조하였다. 용출 거동을 평가하기 위해 high-performance liquid chromatography(HPLC)가 사용되었으며 용출시험은 United States Pharmacopeia(USP) dissolution apparatus II(paddle method)로 진행하였다.
티카그렐러의 용해도를 개선시킨 기존의 연구들에서 많이 이루어졌지만 제조 과정이 간단하고 지속적 약물 방출을 통해 복약 순응도를 높여 효과적인 급성관상동맥증후군 치료제로 개발이 가능케하고자 실험을 진행하였다.
시약 및 재료. 본 실험에서 사용된 약물인 티카그렐러는 Alembic Pharmaceuticals Ltd.(인도), 고분자인 Eudragit RS PO 와 Eudragit RL PO는 BASF(한국), 붕해제인 sodium starch glycolate(SSG)는 화원약품(한국), 활택제인 magnesium stearate(Mg_st)는 Junsei Chem Co.(일본)을 사용하였다. 결합제인 polyvinyl pyrrolidone K-30(PVP K-30)과 부형제인 microcrystalline cellulose(MCC)는 Sigma-Aldrich에서 각각 구입하여 사용하였다.실험에서 사용된 모든 용매 및 화학약품은 HPLC 등급을 사용하였다.
고체분산체의 제조. Table 1과 같은 방법으로 Eudragit RS PO, RL PO와 포접시킨 고체분산체를 준비하였다. 공용매로는 메탄올을 사용하였으며 분무건조기(Spray Dryer SD-1000, Eyela, 일본)를 통해 고체분산체를 제조하였다. 분무 건조 조건은 Table 2에 나타내었다.
티카그렐러 고체분산체의 유동성을 향상시키기 위하여 과립물을 제조하였다. 티카그렐러를 함유하는 과립의 제조는 약물과 MCC, SSG, PVP K-30을 각각 부형제, 붕해제, 결합제로써 Table 3에 표기한 바와 같이 일정한 비율로 혼합하여 골고루 섞은 뒤 연립액을 분사하여 균일하게 분산시켰다. 연립액으로는 정제수를 사용하였다. 잔류 수분을 제거하기 위하여 약 50 oC의 오븐에서 약 30분간 건조시킨 후 꺼내어 분쇄한 뒤 200 μm 크기의 체에 걸러 균일한 입자를 수득하였다. 얻어진 모든 고체분산체와 과립물은 사용하기 전까지 데시게이터에 보관하였다.
정제의 제조. 정제는 압축 성형 프레스(MH 50Y CAP 50 ton, Japan)를 이용해 1분동안 10 kg/cm2의 압력을 가하여 Table 3의 조성으로 제조하였다. 이후 정제는 시험 전까지 데시케이터에 보관 후 사용하였다.
과립물의 구조학적 특성분석. 티카그렐러와 Eudragit RL과 RS를 각각 혼합하여 제조한 고체분산체가 분무 건조 및 과립 등의 공정 과정에서 화학 변화를 나타냈는지 확인하고 약물과 고분자가 가지고 있는 고유의 성질을 유지하고 있는지 확인하기 위하여 Fourier transform infrared spectroscopy (FTIR, GX, Perkin Elmer, Waltham, Massachusetts, 미국)로 분석을 시행하였다. ATR법을 사용하였으며 측정 범위는 4000-400 cm-1였다.
고체분산체의 형태학적 특성분석. 제조한 고체분산체와 약물의 입자형태를 관찰하여 비교하기 위해 주사전자현미경(scanning electron microscope, SEM, S-3000N, Hitachi Co., Tokyo, 일본)을 사용하였다. 시료관 위에 탄소테이프를 붙이고 시료를 올린 뒤 팔라듐-백금코팅기(SC7640, Quorumech, 영국)를 사용하여 아르곤 가스 하에서 200초간 코팅하여 분석하였다. 시료는 20 kV 전압 조건에서 관찰하였다.
고체분산체의 결정학적 특성분석. 티카그렐러와 Eudragit RL, RS를 각각 포함시켜 제조한 고체분산체의 열적 특성과 결정성을 분석하기 위해 시차주사열량계(differential scanning calorimetry, DSC, Perkin Elmer, 일본)와 X선 회절 분석기(X-ray diffractometer, XRD, MAX 2500, Rigaku, 일본)를 사용하여 분석하였다. DSC는 승온속도 30 oC/min, 온도 범위 0-200 oC에서 온도를 증가시키며 분석하였다. XRD는 간격크기 0.02°, 속도 4°/min, 측정범위 5-60°, 전원 전류 30 mA, 전압 40 kV의 조건에서 분석하였다.
정제의 생체 외 방출거동. 티카그렐러 정제의 용출시험은 USP dissolution apparatus II(paddle method)로 진행하였다. 용출액은 인공장액(pH 6.8), 인공위액(pH 1.2)으로 USP(USP Method A Acid stage, Buffer stage)에 따라 제조 그리고 증류수를 사용하여 진행하였으며 용출시험의 모든 용출구는 티카그렐러 180 mg 해당량이 들어가도록 하였다. 용출기는 DST-610(Labfine Sci Instr, 한국)을 사용하였으며, 회전 수는 100 rpm, 용출액의 온도는 37±0.5 oC, 용출액은 900 mL로 설정하였다. 티카그렐러의 경우 난용성제제로, 각 시험액에 가용화제인 polysorbate 80을 1.0 v/v % 농도로 첨가하여 추가실험을 실시하였다. 붕해시험법 제 1액에서는 5, 10, 15, 30, 45, 60, 90, 120, 240분에, 붕해시험법 제 2액과 증류수에서는 5, 10, 15, 30, 45, 60, 90, 120, 240, 360, 720분에 각각 1 mL의 시료를 취하였으며, 취한 만큼의 완충액 및 정제수를 다시 충진하였다. 시료는 0.45 μm PTFE 필터로 여과한 후 HPLC 분석을 하였다.
티카그렐러 고체분산체의 방출거동은 HPLC 분석기(NS-4000 HPLC System, Futecs, 한국), 오토셈플러(NS-6000 Autosempler, Futecs, 한국), 컬럼 오븐(AT-4000, Futecs, 한국)을 각각 사용하여 분석하였으며 컬럼은 ProntoSIL C18 SH 컬럼(250×4.6 mm, 5 μm, Bischoff Chromatography, 독일)을 사용하였다. HPLC 조건은 유속 1.0 mL/min, 시료주입량 20 μL, 컬럼 온도 35 oC, UV 검출 파장 270 nm 조건에서 샘플 당 12분 동안 분석하였다. 이동상은 acetonitrile: 50 mM ammonium acetate=57:43(v/v %)의 비율로 혼합한 용액을 수산화암모늄을 사용해 pH 8.2로 조정한 후 사용하였다.
|
Table 1 Formulation of Solid Dispersion of Ticagrelor Within Polymer (unit : mg) |

고체분산체의 구조학적 특성분석. 두 종류의 Eudragit의 특성피크는 2940 cm-1, 2906 cm-1(CH2 stretching), 1710 cm-1 (C=O stretching), 1130 cm-1(C-O-C stretching)에서 나타났고 티카그렐러는 1577 cm-1, 1470 cm-1(C=C stretching), 1308 cm-1(C-O stretching), 750 cm-1(C-H bending)에서 각각 특징적인 피크들을 발견할 수 있었다. 이 특징적인 피크들은 고체분산체들에서 또한 찾아볼 수 있었다. 따라서 고체분산체 제조 과정에서 티카그렐러의 변성이 일어나지 않았음을 알 수 있으며 또한 두 종류의 Eudragit 역시 고유의 성질을 잃지 않았으며 이는 화학적 변성이 일어나지 않았음을 알 수 있다. Figure 1
고체분산체의 형태학적 특성분석. 티카그렐러 고체분산체의 형태학적 분석을 위해 SEM을 촬영하여 Figure 3에 나타내었다. SEM을 사용하여 확인한 티카그렐러의 입자모양은 침상의 결정형 원료인 것을 알 수 있다. Figure 3에서 확인할 수 있듯이 분무 건조 과정을 거친 고체분산체의 경우 약물이 기존의 결정형을 잃은 것을 확인할 수 있다.
고체분산체의 결정학적 특성분석. 제조된 티카그렐러 고체분산체의 결정화도는 DSC와 XRD를 사용하여 분석하였다. 고체분산체를 제조하는 과정에서 약물과 고분자가 상호작용하며 결정성을 잃는 것과 그 입자의 크기가 매우 작아짐으로써 용해도가 향상되는 효과를 기대할 수 있다. 분석 결과는 Figure 2와 3에 각각 나타내었다. DSC 분석 결과의 경우, 티카그렐러는 약 140 oC 부근에서 특유의 결정성이 나타났다고 볼 수 있는 흡열 피크가 발견되었으며 고분자인 Eudragit RS PO와 RL PO는 무정형이기 때문에 특정 피크가 나타나지 않음을 확인할 수 있었다.8 고체분산체의 경우에도 마찬가지로 결정형을 띄리라고 판단되는 피크를 발견할 수 없기 때문에 티카그렐러가 결정성을 잃었으며, 고분자에 잘 함유되어 둘러싸여 있는 무정형의 고체분산체가 제조되었다고 판단할 수 있다.12 Figure 4
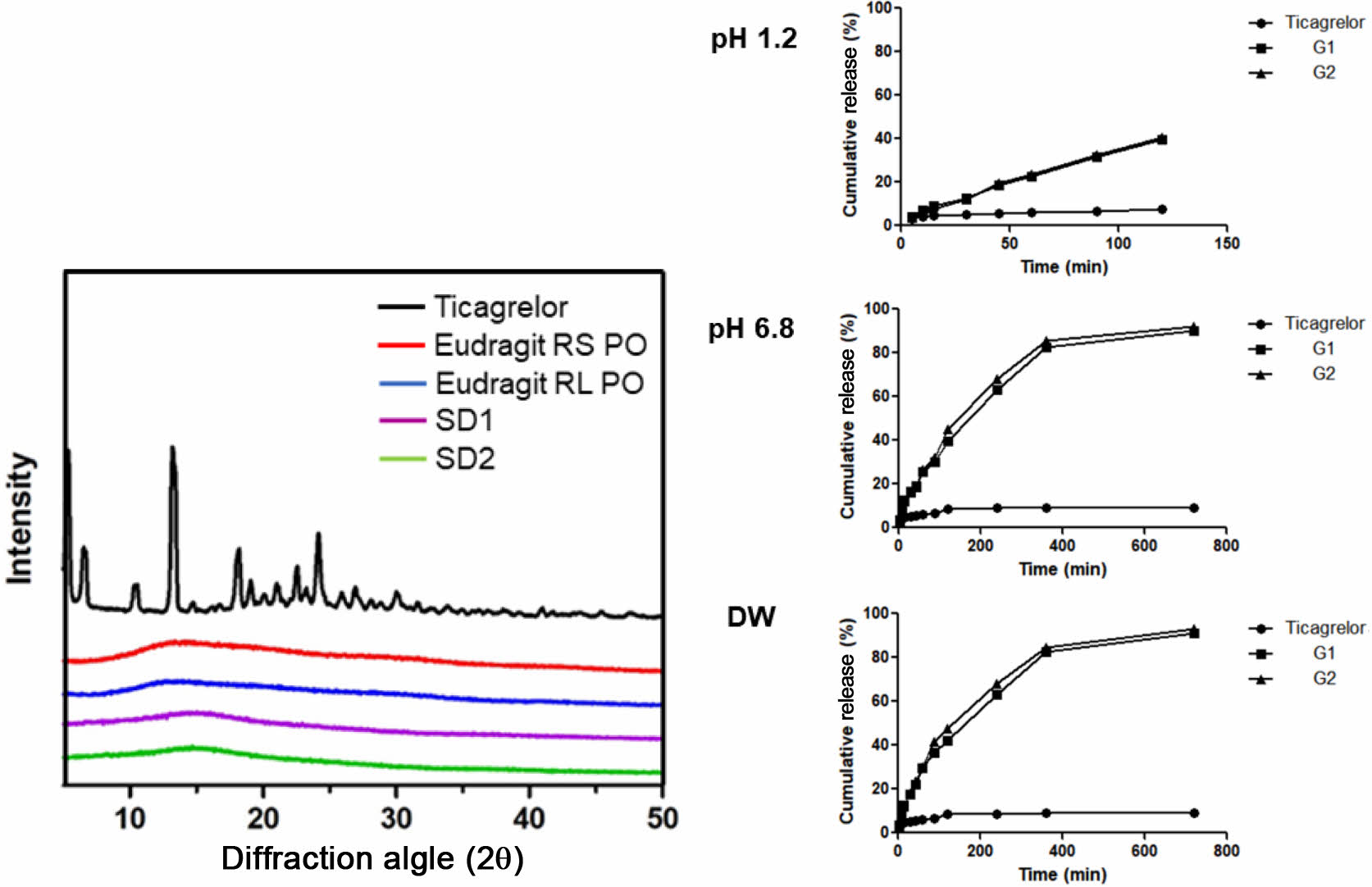
XRD 패턴을 확인해 본 결과 티카그렐러 원료에서 5.6, 6.9, 11.7, 13.5° 부근의 고유의 회절피크가 나타났음을 볼 수 있으며, Eudragit RS PO와 RL PO는 무정형의 패턴을 보임을 알 수 있었다. 티카그렐러 고체분산체의 패턴을 확인해 본 결과 Eudragit과 유사한 패턴을 보이지만 티카그렐러 특유의 회절피크가 보이지 않는 것으로 보아, 무정형의 티카그렐러 고체분산체가 제조되었음을 알 수 있다.13
정제의 생체외 방출거동. HPLC를 통해 용출률을 분석하였으며 분석 결과는 Figure 5를 통해 나타내었다. 용출은 붕해시험 제1액인 pH 1.2에서 2시간, 붕해시험 제2액인 pH 6.8과 정제수에서 각각 12시간 동안 용출 거동을 확인해본 결과 난용성인 티카그렐러 에서는 모두 10% 미만으로 거의 용출되지 않은 반면 분무 건조 공정을 거친 티카그렐러 고체분산체에서는 두 개의 군 모두 최종적으로 90% 이상의 양호한 용출률을 보였다. 또한 이 고체분산체는 서방성 기제로 주로 사용되는 고분자인 Eudragit RL PO 와 RS PO를 포함하였기 때문에 1시간에서 20%, 3시간에서 50%, 8시간에서 90% 이상의 방출률을 보이며 지연방출이 되었음을 확인할 수 있었다. 여기서 Eudragit RL PO가 RS PO 보다 용출률이 높다는 것을 확인할 수 있었는데 이것은 Eudragit RL은 RS 보다 친수성 4차 암모늄 그룹을 더 많이 가지고 있기 때문이라 사료된다.14 또한 pH 1.2와 pH 6.8, 정제수에서 약물이 거의 비슷하게 방출되었음을 확인할 수 있는데 이는 Eudragit RS PO와 RL PO가 pH에 비의존적인 고분자이기 때문임을 시사한다.

|
Figure 1 FTIR spectra of ticagrelor, Eudragit RS PO, Eudragit RL PO, SD 1, and SD 2. |

|
Figure 3 DSC thermogram of ticagrelor, Eudragit RS PO, Eudragit RL PO, and solid dispersion. |

|
Figure 2 SEM image of (a) pure ticagrelor particle; (b) SD 1; (c) SD 2. |

|
Figure 4 XRD patterns of ticagrelor, Eudragit RS PO, Eudragit RL PO, and solid dispersion. |

|
Figure 5 Dissolution behavior of ticagrelor and G1, G2 in (a) pH 1.2; (b) pH 6.8; (c) DW. |
본 연구에서는 티카그렐러의 낮은 생체이용률과 용해도를 개선하고, 1일 2회 복용을 1일 1회복용으로 단순화하여 환자의 복약순응도 및 복용편의성 향상에 도움을 줄 수 있는 서방형 제형을 설계하였다. 제형의 가용화를 위해 분무 건조 방법을 채택하여 사용하였고, 서방형 기제로 주로 사용되는 고분자인 Eudragit RS PO와 RL PO를 포접시켜 고체분산체를 제조하였으며 흐름성 개선을 위해 MCC, PVP K-30, SSG와 혼합하여 연립액을 분사한 뒤 습식과립공정을 거쳐 과립을 만들었다. 이후 Mg_st를 혼합하여 타정이 용이하도록 하였다. 또한 XRD와 DSC, SEM 등의 실험을 통해 고체분산체가 결정성을 잃었으며 약물이 무정형으로 고분자에 잘 포접되었음을 확인할 수 있었다. FTIR 분석을 통해 고체분산체의 제조 과정에서 티카그렐러의 화학적 구조 변성이 일어나지 않았음을 확인하였다. 마지막으로 HPLC를 통해 제형의 용출 거동을 확인하였다. 그 결과 고분자를 함유한 티카그렐러가 12시간 동안 서서히 방출되고 있음을 확인할 수 있었으며 용해도 또한 증가하였음을 알 수 있었다. 따라서 습식과립법을 통해 공정과정이 간단할 뿐만 아니라 티카그렐러의 용해도를 개선시키고 기존 제제에 비해 약물의 방출속도를 제어한 치료제로 개발할 수 있음을 확인하였다.
- 1. Makki, N.; Brennan, T. M.; Girotra, S. Acute Coronary Syndrome. J. Intensive Care Med. 2015, 30, 186-200.
-

- 2. O’Connor, S. A.; Amour, J.; Mercadier, A.; Martin, R.; Kerneis, M.; Abtan, J.; Brugier, D.; Silvain, J.; Barthelemy, O.; Leprince, P.; Montalescot, G.; Colley, J. P. Efficacy of Ex vivo Autologous and In vivo Platelet Transfusion in the Reversal of P2Y12 Inhibition by Clopidogrel, Prasugrel, and Ticagrelor: The APTITUDE Study. Circ. Cardiovasc. Interv. 2015, 8, e002786.
-

- 3. Franchi, F.; Angiolillo, D. J. Novel Antiplatelet Agents in Acute Coronary Syndrome. Nature Reviews Cardiology 2015, 12, 30-47.
-

- 4. Abbate, R.; Cioni, G.; Ricci, I.; Miranda, M.; Gori, A. M. Thrombosis and Acute Coronary Syndrome. Thromb. Res. 2012, 129, 235-240.
-

- 5. Hao, L., et al., Preparation and In vivo/In vitro Characterization of Ticagrelor PLGA Sustained-release Microspheres for Injection. Des. Monomers Polym. 2021, 24, 305-319.
-

- 6. Kim, B. K.; Hong, S. J.; Cho, Y. H.; Yun, K. H.; Kim, Y. H.; Suh, Y.; Cho, J. Y.; Her, A. Y.; Cho, S.; Jeon, D. W.; Yoo, S. Y.; Cho, D. K.; Hong, B. K.; Kwon, H.; Ahn, C. M.; Shin, D. H.; Nam, C. M.; Kim, J. S.; Ko, Y. G.; Choi, D.; Hong, M. K.; Jang, Y. Effect of Ticagrelor Monotherapy vs Ticagrelor with Aspirin on Major Bleeding and Cardiovascular Events in Patients with Acute Coronary Syndrome: The TICO Randomized Clinical Trial. Jama 2020, 323, 2407-2416.
-

- 7. Kim, S. J.; Lee, H. K.; Na, Y. G.; Bang, K. H.; Lee, H. J.; Wang, M.; Huh, H. W.; Cho, C. W. A Novel Composition of Ticagrelor by Solid Dispersion Technique for Increasing Solubility and Intestinal Permeability. Int. J. Pharm. 2019, 555, 11-18.
-

- 8. Chen, K.; Xia, T.; Shao, D.; Zhou, G.; Shen, J.; Yang, Z. Solubility Measurement and Mathematical Correlation of Ticagrelor in Different Pure Solvents. J. Chem. Eng. Data 2020, 65, 3560-3565.
-

- 9. Na, Y. G.; Byeon, J. J.; Wang, M.; Huh, H. W.; Son, G. H.; Jeon, S. H.; Bang, K. H.; Kim, S. J.; Lee, H. J.; Lee, H. K.; Cho, C. W. Strategic Approach to Developing a Self-microemulsifying Drug Delivery System to Enhance Antiplatelet Activity and Bioavailability of Ticagrelor. Int. J. Nanomedicine 2019, 14, 1193.
-

- 10. Y, J. Y.; Ku, J.; Lee, S. Y.; Kim, B. S.; Kim, M. S.; Lee, B.; Khang, G. S.; Lee, H. B. The Effect of Drug Release from Osmotic Pellet Related to the Various Ratio of Eudragit(R) RL and RS. Polym. Korea 2007, 31, 329-334.
-

- 11. Hancock, B. C.; Parks, M. What is the True Solubility Advantage for Amorphous Pharmaceuticals? Pharm. Res. 2000, 17, 397-404.
-

- 12. Gumieniczek, A.; Berecka-Rycerz, A.; Mroczek, T.; Wojtanowski, K. Determination of Chemical Stability of Two Oral Antidiabetics, Metformin and Repaglinide in the Solid State and Solutions Using LC-UV, LC-MS, and FTIR Methods. Molecules 2019, 24, 4430.
-

- 13. Inam, M.; Wu, J.; Shen, J.; Phan, C. U.; Tang, G.; Hu, X. Preparation and Characterization of Novel Pharmaceutical Co-crystals: Ticagrelor with Nicotinamide. Crystals 2018, 8, 336.
-

- 14. Fan, Z. Q.; Yu, H.; Cai, Y. Q. Determination of Alkyl Ammonium Ionic Liquid Cations by Hydrophilic Interaction Liquid Chromatography and its Application in Analysis of Environmental Water. Anal. Methods 2018, 10, 2812-2820.
-

- Polymer(Korea) 폴리머
- Frequency : Bimonthly(odd)
ISSN 0379-153X(Print)
ISSN 2234-8077(Online)
Abbr. Polym. Korea - 2023 Impact Factor : 0.4
- Indexed in SCIE
 This Article
This Article
-
2022; 46(6): 752-756
Published online Nov 25, 2022
- 10.7317/pk.2022.46.6.752
- Received on May 30, 2022
- Revised on Jul 18, 2022
- Accepted on Sep 13, 2022
 Services
Services
Shared
 Correspondence to
Correspondence to
- Gilson Khang
-
*Department of Bionanotechnology and Bio-Convergence Engineering, Jeonbuk National University, 567 Baekje-daero, Deokjin-gu, Jeonju-si, Jeollabuk-do 54896 Korea
**Department of Polymer Nano Science & Technology, Jeonbuk National University, 567 Baekje-daero, Deokjin-gu, Jeonju-si, Jeollabuk-do 54896 Korea
***Polymer Materials Fusion Research Center, Jeonbuk National University, 567 Baekje-daero,
Deokjin-gu, Jeonju-si, Jeollabuk-do 54896 Korea - E-mail: gskhang@jbnu.ac.kr
- ORCID:
0000-0002-6452-5653











 Copyright(c) The Polymer Society of Korea. All right reserved.
Copyright(c) The Polymer Society of Korea. All right reserved.