- Non-isothermal Crystallization of Poly(3-hydroxybutyrate-co-4-hydroxybutyrate)
Soomi Kwon, Tao Zhang, Yunjae Jang*, Minho Jung*, Eunhye Lee*, and Ho-Jong Kang†

Department of Polymer Science and Engineering, Dankook University, 152 Jukjeon-ro, Suji-gu, Yongin-si, Gyeonggi-do 16890, Korea
*CJ Cheiljedang Corp. 55, Gwanggyo-ro 42beon-gil, Yeongtong-gu, Suwon-si, Gyeonggi-do 16495, Korea- Poly(3-hydroxybutyrate-co-4-hydroxybutyrate) 비등온 결정화 거동
단국대학교 고분자공학과, *CJ 제일제당
Reproduction, stored in a retrieval system, or transmitted in any form of any part of this publication is permitted only by written permission from the Polymer Society of Korea.
The non-isothermal crystallization behavior of poly(3-hydroxybutyrate-co-4-hydroxybutyrate)(P(3HB-co-4HB)) was studied. It was found that the non-isothermal crystallization behavior of P(3HB-co-4HB) was affected even with a small change in the melt processing temperature of 10-20 oC. It can be understood as the effect of low molecular weight (3HB-co-4HB) formed by the thermal degradation because of inherent low thermal stability of biodegradable P(3HB-co-4HB) in melt processing. The crystallization temperature and enthalpy decreased with increasing melt processing temperature. In addition, it can be seen that the perfectness of crystal formed in the non-isothermal crystallization of random copolymer also varies depending on the processing temperature. P(3HB-co-4HB) crystals formed under the rapid solidification were made in the 3HB rich phase regardless of the melt processing temperature. Crystals formed under the slow solidification were made both in the 3HB and 4HB rich phases and increasing melt processing temperature makes it difficult to form crystals in the 4HB rich phase. Modified Avrami equation and Avrami-Ozawa equation were fitted well for the non-isothermal crystallization of P(3HB-co-4HB). It was confirmed that the cooling rate and melt processing temperature affect the crystallization rate and the shape of the crystal of P(3HB-co-4HB).
Poly(3-hydroxybutyrate-co-4-hydroxybutyrate)(P(3HB-co-4HB))의 용융 가공온도에 따른 비등온 결정화 거동 변화를 살펴보았다. 10-20 oC의 작은 용융 가공온도 변화에도 P(3HB-co-4HB)의 비등온 결정화 거동이 달라짐을 확인하였다. 이는 용융 가공에서 생분해성 P(3HB-co-4HB)의 원천적으로 낮은 열안정성에 따른 열분해에 의하여 발현된 저분자 P(3HB-co-4HB)의 영향으로 해석할 수 있다. 용융 가공온도 증가에 의한 열분해로 인하여 결정화 온도와 엔탈피 감소를 확인할 수 있었다. 이와 함께 비등온 결정화에서 형성된 공중합체 결정의 완전성도 용융 가공온도에 따라 달라짐을 알 수 있다. 급랭 고상화 조건에서 형성된 P(3HB-co-4HB) 결정은 용융 가공온도와 관계없이 랜덤 공중합체의 3HB rich phase에서 주로 형성되는 반면, 서냉 고상화 조건에서는 3HB rich phase와 4HB rich phase에서 동시에 결정이 형성되며 용융 가공온도가 증가될수록 4HB rich phase에서 결정화가 어려움을 확인하였다. Modified Avrami 식과 Avrami-Ozawa 식은 P(3HB-co-4HB)의 비등온 결정화 거동 해석에 잘 맞으며 냉각속도와 용융 가공온도는 P(3HB-co-4HB)의 결정화 속도와 결정 형태에 영향을 미침을 알 수 있었다.
Non-isothermal crystallization behavior of poly(3-hydroxybutyrate-co-4-hydroxybutyrate) (P(3HB-co-4HB)) was affected even with a small change in the melt t processing temperature of 10-20 oC. The crystallization temperature and enthalpy decreased with increasing melt processing temperature. It can be understood as the effect of low molecular weight (3HB-co-4HB) formed by the thermal degradation because of inherent low thermal stability of biodegradable P(3HB-co-4HB) in melt processing.
Keywords: poly(3-hydroxybutyrate-co-4-hydroxybutyrate), thermal degradation, non-isothermal crystallization, perfectness of crystal.
저자(들)는 이해상충이 없음을 선언합니다.
생분해성 친환경 고분자로 최근 관심의 대상이 되고 있는 poly(3-hydroxybutyrate-co-4-hydroxybutyrate)(P(3HB-co-4HB))는 poly(3-hydroxybutyric acid)(P(3HB)) 사슬에 4HB 사슬이 포함된 미생물에 의하여 만들어지는 random 공중합체이다.1,2 P(3HB-co-4HB) 공중합체 개발이 추진된 배경은 먼저 개발된 P(3HB)의 brittle한 특성 개선을 위함이다.3 P(3HB)는 사슬 구조의 stereoregularity에 의하여 고결정성을 가지고 있으나 기핵 형성이 쉽지않아 P(3HB)에 형성된 구정의 크기가 매우 커지고 구정 성장이 완료되면 구정이 서로 impinging 하면서 형성된 계면이 많아져 물성이 brittle하다.4 또한 낮은 유리전이온도와 느린 결정화 속도로 인하여 상온에서 지속적으로 결정화가 일어나 최종 제품의 안정성에 문제를 초래한다.5,6 P(3HB)에 상대적으로 사슬이 유연한 4HB 사슬을 10% 이하로 포함시키면 4HB 사슬이 crystal defect로 작용하여 결정화도와 결정화 속도를 조절할 수 있기 때문에7 P(3HB)의 brittle한 특성을 개선할 수 있다.
P(3HB-co-4HB)의 결정화거동을 조절하기 위하여 생분해성 고분자인 polylactic acid(PLA)와 블렌딩하여 의하여 이들의 비등온 결정화 거동 연구가8 진행되었으며 silica와 같은 nanoparticle을9 첨가하여 결정화 거동을 살펴본 연구도10 있다. 이와 함께 P(3HB-co-4HB)의 느린 결정화 속도에 따른 post crystallization을 최소화하기 위하여 boron nitride, talc, hydroxyapatite, zinc stearate와 같은 기핵제를 혼합하여 이들의 등온과 비등온 결정화거동을 확인하였다.11,12 P(3HB-co-4HB) 생분해성을 유지하기 위하여 uracil을 친환경 생체적합성 기핵제로 사용하여 이들의 결정화 속도를 조절하는 연구도13 확인되고 있다. 하지만 용융 가공에서 가공조건이 P(3HB-co-4HB)의 비등온 결정화 거동에 미치는 영향에 대한 연구는 전무한 실정이다.
고분자 용융 가공에서는 가해지는 열이력과 힘에 의하여 배향 혹은 결정과 같은 거시구조를 갖는 성형체가 만들어진다.14 결정성 고분자에서 결정화는 등온 결정화와 비등온 결정화로 진행될 수 있다.15 등온 결정화는 고분자의 결정화 거동을 확인할 수 있는 가장 이상적인 방법으로 알려져 있으며 macro crystallization에 적용되는 모델로 시간에 따른 구정이 형성될 수 있는 확률 계산으로 결정화 거동을 확인하는 Avrami model이16 널리 알려져 있다. 하지만 실제 섬유 및 필름 가공과 같은 고분자 용융 가공에서는 다이에서 형성된 섬유 혹은 필름은 냉각과정을 거치면서 비등온 결정화가 일어나게 된다. 냉각과정에서 냉각속도를 조절하여 결정화를 조절할 수 있음에 따라 사용 제품의 결정화도를 조절하기 위하여 비등온 결정화 거동은 용융 가공에서 필수적으로 알아야 할 기본 정보이다. 가장 많이 사용되는 비등온 결정화 model에는 Jeziorny의 modified Avrami model,17 Ozawa model,18 Avrami-Ozawa model,19 Flynn-Wall-Ozawa model20 등이 있다.
본 연구에서는 용용 가공조건 특히, 용융 가공온도가 P(3HB-co-4HB)의 비등온 결정화거동에 미치는 영향을 살펴보기 위하여 modified Avrami model과 Avrami-Ozawa model의 비등온 결정화 모델을 적용하여 이들의 결정화 거동을 해석하고자 하였다.
이론적 배경. 등온 결정화 모델로 많이 사용되는 Avrami model은16 등온 시간에 따른 상대 결정화도의 변화 Xc(t)를 다음과 같이 나타낼 수 있다.

여기서 k는 기핵 및 결정 성장 속도를 나타내며 n 성장 구정의 모양을 나타내는 Avrami constant이다. Avrami constant를 구하기 위해서는 식 (1)을 두 번 로그를 취하여 식 (2)로 나타내고 ln[ln(1-χc(t)]와 lnt plot의 절편과 기울기로써 이들을 각각 구할 수 있다.
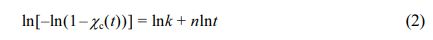
Jeziorny에17 의하여 변형된 modified Avrami model은 비등온 결정화를 해석할 수 있는 model로 식 (1)의 시간의 함수인 Xc(t) 대신 온도의 함수인 Xc(T)를 사용하여 식 (3)으로 나타내며 이때 Avrami constant k는 냉각속도(Ф)를 이용하여 식 (4)로 나타낼 수 있다. 식 (5)를 사용하여 결정화속도를 나타내는 crystallization half time을 계산할 수 있으며 식 (6)으로부터 온도와 냉각속도를 이용하여 등온 결정화와 마찬가지로 시간에 따른 결정화도의 변화를 확인할 수 있다.
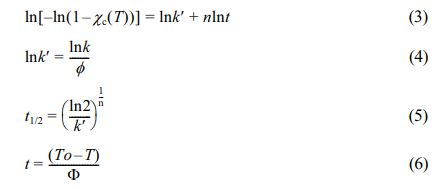
비등온 결정화 거동을 해석에 많이 적용되는 식으로 Ozawa model을18 들 수 있다. Ozawa model을 비등온 결정화를 무한하게 작은 등온 결정화로 가정하였으며 Evans에21 의하여 다음 식으로 표시되었다.

여기서 k'' 와 m은 Ozawa exponent이고 k'' 는 가열 혹은 냉각 함수이다. Avrami 식과 마찬가지로 두 번 로그를 취하여 식 (8)을 얻고 ln[ln(1-χc(T)]와 Ф plot의 절편과 기울기로써 이들을 각각 구할 수 있다. m은 핵과 결정 성장의 정량적 정보를 얻을 수 있으며 k'' 는 결정화 속도를 나타낸다.
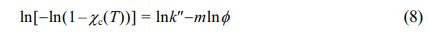
위의 Ozawa 식을 비등온 결정화에 더 잘 적합하도록 Mo는19 Avrami와 Ozawa를 복합적으로 사용하여 다음과 같은 식 (9)를 유도하여 사용하였다.

여기서 F(T)와 α는 lnФ와 lnt plot의 절편과 기울기로 각각 구할 수 있으며 F(T)는 [k''(T)/k]1/m을 나타내며 α는 Avrami 식과 Ozawa 지수의 비(n/m)를, F(T)는 결정화 어려움의 정도를 나타낸다.
재료.본 연구에서는 Figure 1과 같은 구조를 갖는 4HB 함량이 2.1%이며 분자량이 200000 g/mol인 첨가제가 들어가지 않은 실험용 P(3HB-co-4HB)를 CJ 제일제당(Korea)으로부터 제공받아 사용하였다.
분석. 제공받은 P(3HB-co-4HB)의 열안정성을 확인하기 위하여 thermal gravity analyzer(TGA, TA Q50, USA)를 이용하여 180-200 oC에서 20분간 등온으로 유지한 후 질량 변화를 측정하여 가공온도에 따른 열안정성 변화를 무게 감소로 확인하였다.
Differential scanning calorimeter(DSC, TA Q20, USA)를 이용하여 이들의 비등온 결정화 거동을 살펴보았다. 시료는 20 oC/min로 -50 oC에서 용융 가공온도인 180-200 oC까지 가열하여 10-50 oC/min로 냉각하여 결정화 온도(Tc)와 엔탈피(ΔHc)의 변화를 측정하였다. 용융 온도와 용융 엔탈피의 변화를 살펴보기 위하여 이를 다시 -50 oC에서 200 oC로 2차 가열하여 용융 온도(Tm)와 엔탈피의 변화(ΔHm)를 측정하였다. 각 냉각속도로부터 얻어진 결정화 엔탈피로부터 온도에 따른 상대결정화도 변화를 χc(T), 시간에 따른 상대결정화도 변화를 χc(t)로 나타내었다. 식 (3), (7), (8)을 적용하여 modified Avrami model과 Avrami-Ozawa model에서 각각의 결정화 상수를 구하여 이들의 용융 가공온도에 따른 변화를 확인하였다.

|
Figure 1 Chemical structure of poly(3-hydroxybutylate-co-4- hydroxybutylate). |
Figure 2는 180-200 oC로 DSC 승온 최대온도(용융 가공온도)를 올린 후 이를 10-50 oC/min로 냉각하여 얻은 DSC thermogram이다. 그림에서 보는 바와 같이 용융 가공온도에 따라 결정화 온도 및 엔탈피 변화가 일어남을 알 수 있다. 상대적으로 낮은 용융 가공온도인 180 oC에서는 냉각 조건에 따라 결정화 엔탈피 변화가 일어나는 반면, 용융 가공온도를 증가시키면 결정화 피크가 줄어들며 200 oC 용융 가공온도에서는 냉각속도와 관계없이 결정화 엔탈피가 모두 사라짐을 알 수 있다. 또한 용융 가공온도와 냉각속도에 따라 결정화 온도도 함께 변화됨을 알 수 있다. 이러한 결과는 용융 가공시 용융 가공온도가 P(3HB-co-4HB)의 비등온 결정화에 영향을 미침을 의미한다.
Figure 3에 TGA를 이용하여 용융 가공에 의한 열분해를 확인하기 위하여 20분간 각 가공온도에서 P(3HB-co-4HB)를 체류시켜 이들의 질량변화를 나타내었다. 그림에서 보는 바와 같이 용융 가공온도가 증가함에 따라 최대 1.1% 이내의 소량의 열분해가 일어남을 알 수 있다. 본 연구에서 사용한 P(3HB-co-4HB)는 생분해성 고분자로 생분해가 갖는 우수한 분해 특성과 함께 열분해가 일반 고분자에 비하여 잘 일어나는 것으로 알려져 있다.22 P(3HB-co-4HB)는 P(3HB)에 비하여 4HB 사슬 첨가에 의하여 열분해가 개선된다는 보고가23 있으나 생분해성 고분자가 갖는 intrinsic 특성에 의하여 일반 고분자와 비교하여 매우 낮은 열적 특성을 갖는다. P(3HB-co-4HB)는 β-elimination에 의한 random degradation에 의하여 3HB 사슬과 4HB 사슬에서 분해가 일어나며 이에 따라 저분자량의 oligomer가 발생하는 것으로 알려져 있다.24 따라서 융용 가공에서 Figure 3과 같은 소량의 열분해로 인해 저분자 P(3HB-co-4HB)가 생성되며 이로 인하여 P(3HB-co-4HB)의 결정화가 방해를 받을 수 있다. 10-20 oC의 아주 작은 용융 가공온도 변화에도 결정화 거동이 변화되며 냉각속도가 빠른 경우, 변화가 더 많이 일어남을 알 수 있다. 이러한 결과로부터 생분해성 P(3HB-co-4HB)의 열분해 최소화를 위하여 낮은 온도로 용융 가공할 경우, 용융 가공온도가 P(3HB-co-4HB)의 흐름특성에 미치는 영향과 함께 결정과 같은 거시구조를 형성하는 결정화 거동에도 영향을 미침에 따라 이에 대한 연구가 필요함을 알 수 있다.
Figure 4에 Figure 2로부터 용융 가공온도에 따른 결정화 온도와 결정화 엔탈피의 변화를 함께 나타내었다. 그림에서 보는 바와 같이 냉각속도를 증가시키면 결정화 온도는 감소되며 아울러 결정화 엔탈피 또한 감소함을 알 수 있다. 이는 P(3HB-co-4HB)에 형성된 기핵이 결정으로 성장하기 위해서는 배아(embryo) 형성을 위한 최소한의 에너지가 필요하나 냉각속도가 빨라지면 이러한 에너지를 얻지 못하여 결정 성장이 늦게 일어나며 이에 따라 얻어지는 결정 양도 상대적으로 적어 결정화 엔탈피가 감소된다. 즉, 용융 가공에서 급랭 고상화 조건은 결정화 온도와 결정화도의 감소를 초래함을 알 수 있다.
Figure 4의 용융 가공온도에 따른 결정화온도와 엔탈피 변화로부터 냉각속도와 함께 용융 가공온도에 의하여 P(3HB-co-4HB)의 비등온 결정화에 큰 영향을 미침을 알 수 있다. 용융 가공온도가 증가될수록 결정화 온도는 더 낮아지며 결정화 엔탈피 또한 줄어드는 것으로 보아 용융 가공온도 증가가 결정화를 어렵게 함을 알 수 있다. 용융 가공온도의 결정화에 대한 영향은 냉각속도가 느릴수록 더 잘 나타나며 용융 가공온도 200 oC에서는 냉각속도 30 oC/min 이상에서 결정화가 전혀 일어나지 못함을 알 수 있다. 주목할 만한 사항은 10-20 oC의 용융 가공온도 차이에 의하여 P(3HB-co-4HB) 결정화 거동이 현저하게 변한다는 것이다. 이는 일반 고분자에서는 잘 확인되지 않는 현상이다. P(3HB-co-4HB)가 개발된 이유는 P(3HB)의 느린 결정화에 따른 커다란 구정 형성에 따른 brittle한 특성의 개선과 함께 느린 결정화 거동에 따른 post crystallization을25 개선하기 위함이다. 따라서 용융 가공온도에 따른 이러한 결정화 거동은 용융 가공 후 얻어지는 P(3HB-co-4HB)의 최종 물성에 지대한 영향을 미칠 것으로 예상되며 따라서 용융 가공온도에 따른 P(3HB-co-4HB)의 비등온 결정화 거동에 대한 연구가 필요함을 알 수 있다.
Figure 5는 각기 다른 용융 가공온도에서 냉각속도를 변화시켜 결정화가 일어난 P(3HB-co-4HB)를 2차 승온시킨 DSC thermogram이다. Figure 5에서 보는 바와 같이 용융 가공온도와 냉각속도에 따라 냉결정화 및 결정의 용융 거동이 현저하게 달라짐을 보인다. 가공온도를 증가시키면 2차 승온과정에서 냉결정화가 일어나며 특히, 이러한 냉결정화는 냉각속도가 빠를수록 더 낮은 용융 가공온도에서 발현됨을 알 수 있다. 이와 함께 생성 결정의 용융 피크는 double 피크로 나타나는 것을 확인할 수 있다.
냉결정화 엔탈피는 비등온 냉각과정에서 완전하게 결정이 일어나지 못했던 결정들이 DSC에 의한 승온 열이력에 의하여 보다 열역학적으로 완전한 결정으로 변화되는 현상이다. 그림에서 보는 바와 같이 용융 가공온도를 증가시키면 열분해에 의하여 결정 형성에 어려움이 있고 특히, 냉각속도가 빠른 경우 불완전한 결정이 더 많이 발현되며 그 결과, 이들이 2차 승온 과정에서 보다 완전한 결정으로 재결정화가 다시 일어남을 알 수 있다.
Double 용융 피크는 본 연구에서 사용한 P(3HB-co-4HB)가 random copolymer이기 때문에 일어나는 현상이다.26 3HB 사슬과 함께 P(3HB-co-4HB)의 사슬을 구성을 하고 있는 2.1%의 4HB 사슬이 random하게 3HB 사슬 내에 존재하기 때문에 P(3HB-co-4HB)에는 4HB rich phase와 3HB rich phase가 필연적으로 존재하게 된다. 따라서 각각 phase에서 형성된 결정들은 그 열역학적 완전성이 달라지게 되며 그 결과, 두개의 용융 피크를 보이게 된다. 4HB rich phase에서 형성된 결정은 사슬내의 4HB가 결정 형성을 제한하여 열역학적으로 완전성이 낮은 결정이 얻어짐에 따라 다소 낮은 온도에서 용융 피크(Tm1)를 보이는 반면, 4HB 사슬이 상대적으로 적은 3HB rich phase에서 얻어지는 결정은 4HB rich phase에서 형성된 결정보다 안정하여 보다 높은 온도(Tm2)에서 용융 피크를 보이게 된다. Double 용융 피크를 보이는 또 다른 이유로 DSC 승온 과정에서 냉결정화로 생성된 결정들의 재용융에 의해서도 이러한 용융 피크의 변화가 일어날 수 있다. 4HB rich phase에서 형성된 결정이 DSC 승온과정에서 보다 더 열역학적으로 완전하게 결정화되면 용융과정에서 3HB rich phase에서 얻어지는 결정과 유사한 완전성을 가져 높은 용융온도에서 용융될 수 있다.
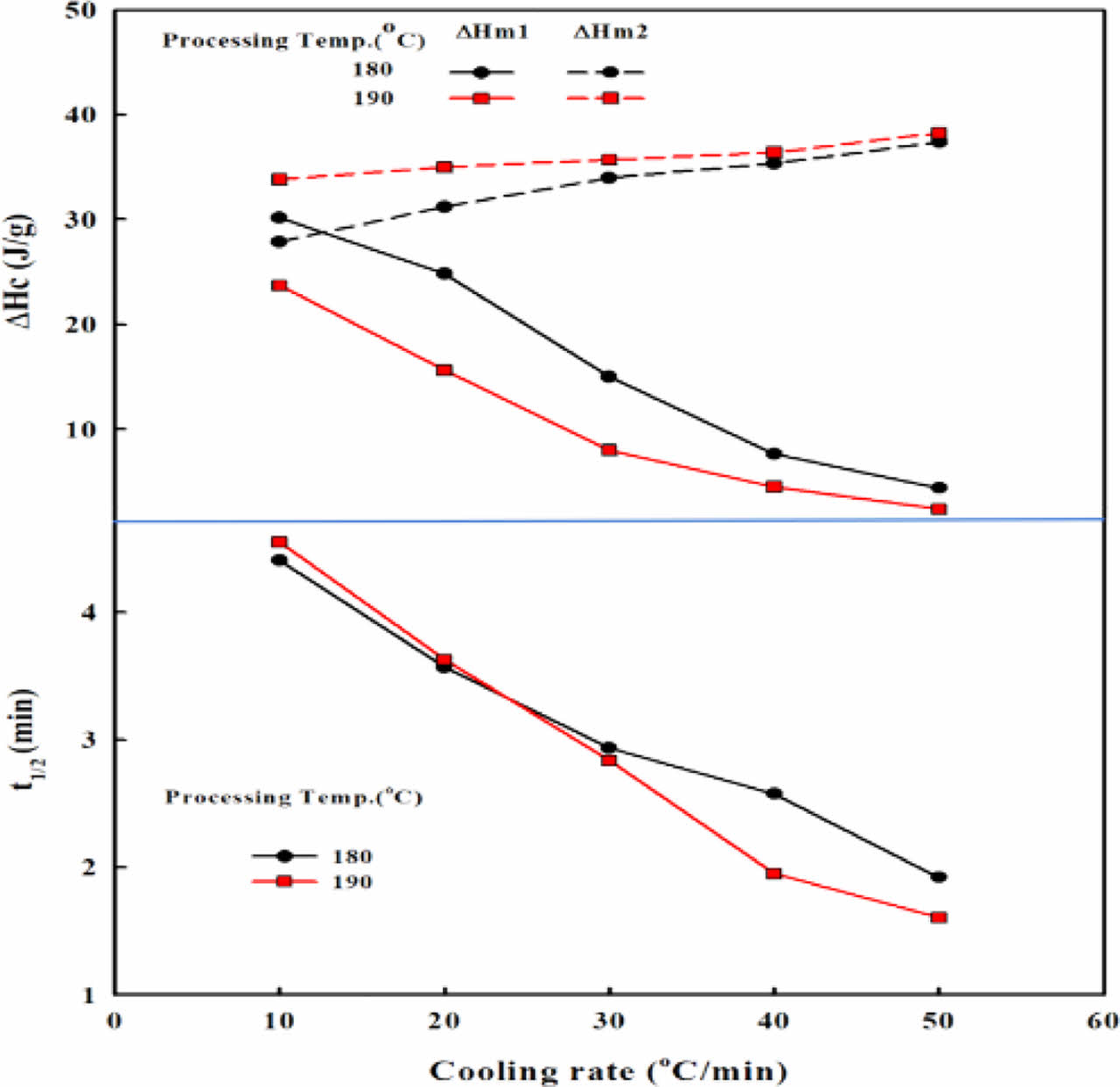
Figure 6에 Figure 5에서 얻어진 용융 피크로부터 4HB rich phase에서 형성되는 결정의 용융 온도(Tm1)와 엔탈피의 변화(∆Hm1) 그리고 3HB rich phase에서 형성된 결정의 용융 온도(Tm2)와 엔탈피의 변화(∆Hm2)를 나타내었다. 그림에서 보는 바와 같이 4HB rich phase에서 형성되는 결정들은 160 oC 근방에서 형성되며 3HB rich phase에서 형성된 결정들은 170 oC 근방에서 형성되는 것으로 보아 4HB 사슬이 상대적으로 적은 3HB rich phase에서 형성된 결정들이 3HB 사슬의 규칙적인 stereoregularity로 인하여 열역학적 완전성이 높음을 알 수 있다.
용융 가공온도가 결정의 용융온도에 미치는 영향을 살펴보면 용융 가공온도는 3HB rich phase의 결정보다는 상대적으로 불완전한 4HB rich phase의 결정에 더 영향을 미침을 알 수 있다. 용융 가공온도가 증가함에 따라 4HB rich phase의 결정의 용융온도(Tm2)는 감소함을 보이며 냉각속도가 증가됨에 따라 용융 가공온도에 의한 용융온도의 영향은 작아짐을 알 수 있다. 3HB rich phase의 결정도 같은 경향을 보이나 용융 가공온도의 영향이 작음을 보인다. 높은 용융 가공온도에서는 Figure 3에서 확인된 바와 같이 저분자 P(3HB-co-4HB)에 의하여 결정화가 제한되어 결정의 불완전성이 커진다. 하지만 냉각속도가 증가되면 냉각속도에 의한 불완전한 결정 형성 영향이 더 커져 열분해에 의한 영향이 보이지 않는 것으로 사료된다.
Figure 6(b)에 각각 결정의 용융 엔탈피 변화를 나타내었다. Figure 5에서 확인된 바와 같이 P(3HB-co-4HB)의 double 용융 피크는 용융온도의 차이가 10 oC 이내임에 따라 각각의 엔탈피의 중첩이 일어남에 따라 이를 분리하기 어려우나 double 피크의 변곡점으로부터 각각의 엔탈피를 확인하여 이를 Figure 6(b)에 나타내었다. 그림에서 보는 바와 같이 180 oC 용융 가공온도에서는 3HB rich phase에서 형성된 결정이 4 HB rich phase에서 형성된 결정보다 많아지나 용융 가공온도가 증가될수록 4HB에 기인되는 결정의 양이 현저히 줄어듦을 알 수 있다. 냉각속도가 결정 형성에 미치는 영향을 살펴보면 냉각속도가 증가됨에 따라 4HB rich phase의 결정 형성이 어려워지는 반면 3HB rich phase의 결정 형성은 더 많아짐을 알 수 있다. 냉각속도가 50 oC/min 즉, 급랭 조건의 경우에 형성되는 결정은 용융 가공온도와 상관없이 대부분 3HB rich phase에서 형성된 결정임을 알 수 있다.
이러한 현상은 4HB rich phase에서 형성되는 결정이 3HB rich phase에서 형성되는 결정에 비하여 결정 형성이 어렵다는 것을 의미한다. 따라서 용융 가공온도 증가에 의한 열분해와 냉각속도 증가와 같은 결정화를 방해하는 요인들이 결정화가 상대적으로 어려운 4HB rich phase 결정 형성에 더 많은 영향을 미치는 것을 알 수 있다. Figure 6(c)에 3HB rich phase와 4HB rich phase에 의하여 형성된 결정의 합을 나타내었다. 두개의 용융 피크가 중첩됨에 따라 중첩된 부분의 결정화 엔탈피를 구하고 이중 반을 Figure 6(b)의 각각의 결정화 엔탈피에 더하여 총 결정화를 나타내었다. 그림에서 보는 바와 같이 냉각속도 증가에 따른 상대 결정화도가 낮아지며 동시에 용융 가공온도의 증가에 의해서도 P(3HB-co-4HB)의 상대 결정화도가 낮아짐을 알 수 있다. 하지만 Figure 6(b)에서 높은 용융 가공온도와 빠른 냉각속도에서 생성된 결정들은 상대적으로 안정적인 3HB rich phase에서의 결정으로 이루어졌음을 알 수 있어 결정의 형성 영역은 용융 가공온도에 따른 상대 결정화도의 변화와 함께 성형품의 최종 물성을 좌우하는 요인이 될 것으로 판단된다.
식 (6)에 의하여 각 냉각속도로부터 상대 결정화도를 시간에 따라 구하여 Figure 7에 시간에 따른 상대 결정화도 Xc(T)의 변화를 나타내었다. 200 oC 용융 가공에서는 본 연구에서 사용한 냉각속도 전 구간에서 비등온 결정화 엔탈피를 얻을 수 없어 180와 190 oC 용융 가공 온도에서 이들의 변화를 확인하였다. 냉각속도가 증가함에 따라 Xc(T)가 빨리 100%에 도달하는 것으로 보아 결정화 속도가 증가함을 알 수 있다. P(3HB-co-4HB)의 결정화는 전형적인 sigmoidal 결정화 거동을 보이며 결정화 초반의 기핵 형성에 따른 비선형적인 느린 결정화 거동과 함께 결정화 후반에서는 secondary crystallization에 의한 느린 비선형적인 결정화 거동을 보인다.
Figure 8에 식 (3)의 Jeziorny의 변형된 modified Avrami model을 사용하여 ln[(-ln(1-X(T))] vs. lnt plot을 나타내었다. 이때 기핵 형성과 secondary crystallization에 기인되는 비선형 구간을 제외한 primary crystallization의 선형적인 구간 만을 사용하였다. 각 용융 가공온도에서 냉각속도와 시간의 관계가 선형적(correlation coefficient(R2): 0.9963-0.9985)으로 보임에 따라 Jeziorny가 유도한 식 (3)이 P(3HB-co-4HB) 비등온 결정화에 잘 맞는 것을 알 수 있다.
Figure 8에서 이들의 절편과 기울기로 k'와 modified Avrami model의 상수 n을 구하고 식 (5)에 의하여 crystallization half time을 계산하여 Figure 9에 함께 나타내었다. 그림에서 보는 바와 같이 냉각속도가 증가됨에 따라 k'값이 증가하는 것으로 보아 결정화 속도가 빨라짐을 알 수 있다. 즉, Figure 6(b)의 결과에서 확인된 것과 같이 급랭조건에서는 4HB rich phase의 결정 형성이 감소되면서 형성되는 3HB rich phase의 결정은 빠른 시간 내 결정화가 완료됨을 알 수 있다.
용융 가공온도가 결정화 속도에 미치는 영향을 보면 냉각속도 30 oC/min까지는 용융 가공온도는 결정화속도 k'값에는 영향이 없는 것으로 보인다. 상대적으로 서냉 조건에서는 Figure 6에서 확인된 바와 같이 3HB phase와 4HB phase 영역에서 동시에 형성되어 용융 가공온도는 결정의 열역학적 완전성에는 영향을 미치나 결정화 속도에는 크게 영향을 미치지 않음을 의미한다. 하지만 3HB rich phase에서 형성된 결정이 상대적으로 많은 30 oC/min 이상의 급랭 조건에서는 용융 가공온도 증가에 의하여 결정화 속도가 증가된다. 이러한 결과로부터 P(3HB-co-4HB)를 높은 용융 가공온도에서 급랭 조건으로 냉각시키면 상대적으로 안정된 3HB rich phase 결정이 빠르게 형성됨을 알 수 있다.
Figure 9(b)에 결정의 모양을 나타내는 n 값을 냉각속도 및 용융 가공온도에 따라 나타내었다. 그림에서 보는 바와 같이 n 값은 2.7-3.1 범위를 가짐에 따라 형성된 결정은 3차원적 구조를 가지고 있음을 알 수 있다. 냉각 속도가 증가됨에 따라 n값이 다소 감소하는 것으로 보아 급랭조건에서 형성된 3HB rich phase 영역에서 생긴 결정이 서냉에 의하여 3HB와 4HB rich phase에서 생긴 결정보다 열역학적으로는 더 안정하지만 Figure 9(a)에서 확인된 바와 같이 빠른 결정화 속도에 의하여 형태학적으로는 3차원적 구조적 형성이 다소 미흡하나 그 차이는 크지 않음을 알 수 있다. 용융 가공온도는 n 값에 크게 영향을 미치지 않는 것으로 보아 열분해에 의하여 생성된 저분자 P(3HB-co-4HB)에 의하여 P(3HB-co-4HB) 결정화, 특히, 4HB rich phase영역에서의 결정 형성은 어려워지나 결정의 3차원적 모양에는 큰 차이가 없음을 알 수 있다. Figure 9(c)에 구해진 k' 와 n값을 사용하여 이들의 crystallization half time을 나타내었다. 냉각속도가 증가됨에 따라 결정화 속도가 빨라짐을 보이며 용융 가공온도가 crystallization half time에 미치는 영향은 Figure 9(a)의 k'의 결과와 마찬가지로 냉각속도 30 oC/min 이상에서는 높은 용융 가공온도에서 3HB phase에서 형성되는 결정의 결정화 속도는 빨라짐을 알 수 있다.
Figure 10에 Avrami와 Ozawa model을 복합적으로 사용한 Mo 식 (9)를 나타내었다. 그림에서 보는 바와 같이 각 가공온도에서 냉각속도와 시간의 곡선이 선형적(correlation coefficient(R2): 0.9970-0.9988)으로 보임에 따라 Mo가18 유도한 식 (9)가 P(3HB-co-4HB) 비등온 결정화에 잘 맞는 것을 알 수 있다. Figure 11에 Figure 10의 절편과 기울기로부터 F(T)와 α를 구하여 나타내었다. F(T)는 각 상대 결정화도에 도달하기 위한 냉각속도, 결정화의 어려움 정도를 의미하며 α는 Avrami 상수 n과 Ozawa 상수 m의 비(n/m)를 나타낸다.
Figure 11(a)에서 보는 바와 같이 F(T) 값이 상대 결정화도와 관계없이 거의 일정한 것으로 보아 각 상대 결정화도에 도달하기 위한 결정화의 어려움의 정도 즉, 결정화 속도가 각 상대 결정화가 증가하는 과정에서 일정함을 알 수 있다. 180 oC 용용 가공에서의 F(T) 값이 높은 것으로 보아 낮은 용융 가공온도에서 결정화 속도가 느린 것을 알 수 있으며 이러한 결과는 Figure 9의 modified Avrami model과 잘 일치한다. Figure 11(b)의 α값은 상대 결정화도가 증가됨에 따라 감소됨을 보이며 결정화 온도가 증가됨에 따라 감소됨을 알 수 있다. 이는 각 결정화 정도와 용융 가공온도에서 등온과 비등온 결정화의 형태가 달라짐을 의미한다. Figure 6에서 확인한 바와 같이 P(3HB-co-4HB)는 각 냉각속도에 따라 4HB rich phase와 3HB rich phase에서 생겨나는 결정의 완전성이 다르며 이를 좌우하는 용융 가공온도 및 결정화 정도에 따라 결정의 형태가 등온 결정화와 비등온 결정화에서 달라짐을 의미한다.

|
Figure 2 DSC cooling thermograms of P(3HB-co-4HB) with various melt processing temperature: (a) 180 oC; (b) 190 oC; (c) 200 oC. |

|
Figure 3 TGA thermograms of P(3HB-co-4HB) with various melt processing temperature. |

|
Figure 4 Crystallization behaviors of P(3HB-co-4HB): (a) crystallization temperature; (b) crystallization enthalpy |

|
Figure 5 DSC 2nd heating thermograms of P(3HB-co-4HB) with various melt processing temperature: (a) 180 oC; (b) 190 oC; (c) 200 oC. |

|
Figure 6 Effect of cooling rate on melting behavior of P(3HB-co4HB) with different 4HB contents: (a) melting temperature; (b) melting enthalpy; (c) total melting enthalpy |

|
Figure 7 Relative crystallinity of P(3HB-co-4HB) as a function of time with various processing temperature: (a) 180 oC; (b) 190 oC. |

|
Figure 8 Modified Avrami plots of P(3HB-co-4HB) with various melt processing temperature: (a) 180 oC; (b) 190 oC. |

|
Figure 9 Non-isothermal crystallization kinetic parameters of P(3HB-co-4HB) based on modified Avrami model: (a) k'; (b) n; (c) t1/2. |

|
Figure 10 Avrami-Ozawa plots of P(3HB-co-4HB) with various processing temperature: (a) 180 oC; (b) 190 oC. |

|
Figure 11 Non-isothermal crystallization kinetic parameters of P(3HB-co-4HB) based on Avrami-Ozawa model: (a) F(T); (b) α. |
본 연구에서는 용융 가공온도가 P(3HB-co-4HB)의 비등온 결정화에 미치는 영향을 살펴보아 다음과 같은 결론을 얻을 수 있었다. 용융 가공온도의 변화는 P(3HB-co-4HB) 비등온 결정화에 영향을 미쳐 결정화 온도는 낮아지며 결정화 엔탈피도 감소됨을 알 수 있다. 이러한 결정화 거동의 변화는 열분해에 의하여 발현되는 저분자 P(3HB-co-4HB)에 따른 것으로 해석할 수 있다.
용융 가공 온도는 형성되는 결정의 완전성에도 영향을 미치며 특히, 서냉 조건에서는 낮은 가공온도에서 3HB rich phase와 4HB rich phase 결정이 동시에 형성되며 용융 가공온도가 증가되면 4HB rich phase의 결정 형성을 어려워짐을 알 수 있다.
서냉 조건에서는 용융 가공온도가 결정화 속도에 미치는 영향이 없는 반면, 급랭 조건에서 형성된 3HB rich phase 결정은 결정화 속도가 상대적으로 빠르며 이때 용융 가공온도 증가에 의하여 결정화 속도가 감소됨을 알 수 있다. 하지만 용융 가공 온도는 결정 형태에는 크게 영향을 미치지 않음을 알 수 있었다.
Modified Avrami 식과 Avrami-Ozawa 식은 P(3HB-co-4HB)의 비등온 결정화 거동에 잘 맞으며 냉각속도와 용융 가공온도가 결정화속도 및 구정 형태에 영향을 미침을 알 수 있었다.
- 1. Chanprateep, S.; Buasri, K.; Muangwong, A.; Utiswannakul, U. Biosynthesis and Biocompatibility of Biodegradable Poly(3-hydroxybutyrate-co-4-hydroxybutyrate). Polym. Degrad. Stab. 2010, 95, 2003-2012.
-

- 2. Ramachandran, H.; Amirul, A. A. Evaluation of Unrefined Glycerine Pitch as an Efficient Renewable Carbon Resource for the Biosynthesis of Novel Yellow-pigmented P(3HB-co-4HB) Copolymer Towards Green Technology. Biotechnol. Bioprocess Eng. 2013, 18, 1250-1257.
-

- 3. Guerra-Blanco, P.; Cortes, O.; Poznyak, T.; Chairez, I.; García-Peñ, E. I. Polyhydroxyalkanoates (PHA) Production by Photo- heterotrophic Microbial Consortia: Effect of Culture Conditions Over Microbial Population and Biopolymer Yield and Composition. Eur. Polym. J. 2018, 98, 94-104.
-

- 4. Conti, D. S.; Pezzin, S. H.; Ferreira, L. A.; Coelho, L. A. F. Mechanical and Morphological Properties of Poly(3-hydroxy- butyrate)/Poly(3-hydroxybutyrate-co-3-hydroxyvalerate) Blends. Macromol. Symp. 2006, 245-246, 491-500.
-

- 5. Wellen, R. M. R.; Rabello, M. S.; Araufo Jr., I. C.; Fechine, G. J. M.; Canedo, E. Melting and Crystallization of Poly(3-hydroxy- butyrate): Effect of Heating/Cooling Rates on Phase Transformation. Polímeros 2015, 25, 296-304.
-

- 6. Gopi, S.; Kontopoulou, M.; Ramsay, B. A.; Ramsay, A. J. Manipulating the Structure of Medium-chain-length Polyhydroxy- alkanoate (MCL-PHA) to Enhance Thermal Properties and Crystallization Kinetics. Int. J. Biol. Macromol. 2018, 119, 1248-1255.
-

- 7. Lu, X. P.; Wen, X.; Yang, D. Isothermal Crystallization Kinetics and Morphology of Biodegradable Poly(3-hydroxybutyrate-co-4-hydroxybutyrate). J. Mater. Sci. 2011, 46, 1281-1288.
-

- 8. Li, H. Y.; Lu, X. P.; Yang, H.; Hu, J. W. Non-isothermal Crystallization of P(3HB-co-4HB)/PLA Blends. J. Therm. Anal. Calorim. 2015, 122, 817-829.
-

- 9. Volova, T. G.; Shumilova, A. A.; Nikolaeva, E. D.; Kirichenko, A. K.; Shishatskaya, E. I. Biotechnological Wound Dressings Based on Bacterial Cellulose and Degradable Copolymer P(3HB/4HB). Int. J. Biol. Macromol. 2019, 131, 230-240.
-

- 10. Cai, Z. J.; Hou, C. W.; Yang, G. Poly(3-hydroxubutyrate-co-4-hydroxubutyrate)/Bacterial Cellulose Composite Porous Scaffold: Preparation, Characterization and Biocompatibility Evaluation. Carbohydr. Polym. 2012, 87, 1073-1080.
-

- 11. García-Quiles, L.; Cuello, A. F.; Castell, P. Sustainable Materials with Enhanced Mechanical Properties Based on Industrial Polyhydroxyalkanoates Reinforced with Organomodified Sepiolite and Montmorillonite. Polymers 2019, 11, 696-714.
-

- 12. Qian, J.; Zhu, L. Y.; Zhang, J. W.; Whitehouse, R. S. Comparison of Different Nucleating Agents on Crystallization of Poly(3-hydroxybutyrate-co-3-hydroxyvalerates). J. Polym. Sci. B: Polym. Phys. 2007,45, 1564-1577.
-

- 13. Che, X. M.; Ye, H. M.; Chen, G. Q. Effects of Uracil on Crystallization and Rheological Property of Poly(R-3-hydroxy- butyrate-co-4-hydroxybutyrate). Composites A: Appl. Sci. Manuf. 2018, 109, 141-150.
-

- 14. White, J. L. Structure Development in Polymer Processing. Pure Appl. Chem. 1983, 55, 765-776.
-

- 15. Mandelkern, L. Crystallization of Polymers: Volume 2, Kinetics and Mechanisms, 2nd Edition Cambridge University Pressm 2004.
- 16. Avrami, M. Kinetics of Phase Change. I General Theory. J. Chem. Phys. 1938, 7, 1103-1112.
-

- 17. Jeziorny A. Parameters Characterizing the Kinetics of the Non-isothermal Crystallization of Poly(ethylene terephthalate) Determined by DSC. Polymer 1987, 19, 1142-1144.
-

- 18. Ozawa, T. Kinetics of Non-isothermal Crystallization. Polymer 1971, 12, 150-158.
-

- 19. Liu T. X.; Mo, Z. S.; Wang, S. G.; Zhang, H. F. Nonisothermal Melt and Cold Crystallization Kinetics of Poly(aryl ether ether ketone ketone). Polym. Eng. Sci. 1997, 37, 568-575.
-

- 20. Flynn, J. H.; Wall, L. A. A Quick, Direct Method for the Determination of Activation Energy from Thermogravimetric Data. J. Polym. Sci. Part B: Polym. Lett. 1966, 4, 323-328.
-

- 21. Evans, U. R. The Laws of Expanding Circles and Spheres in Relations to the Lateral Growth of Surface Films and the Grain-size of Metals. Trans. Faraday Soc. 1945, 41, 365-374.
-

- 22. Kunioka, M.; Doi, Y. Thermal Degradation of Microbial Copolyesters: Poly(3-hydroxybutyrate-co-3-hydroxyvalerate) and Poly(3-hydroxybutyrate-co-4-hydroxybutyrate). Macromolecules 1990, 23, 1933-1936.
-

- 23. Kim, K. J.; Doi, Y.; Abe, H.; Martin, D. P. Thermal Degradation Behavior of Poly(4-hydroxybutyric acid). Polym. Degrad. Stab. 2006, 91, 2333-2341.
-

- 24. Omura, T.; Goto, T.; Maehara, A.; Kimura, S.; Abe, H.; Iwata, T. Thermal Degradation Behavior of Poly[(R)-3-hydroxybutyrate-co-4-hydroxybutyrate]. Polym. Degrad. Stab. 2021, 183, 109460-109468.
-

- 25. Bian, Y. J.; Han, L. J.; Han, C. Y.; Lin, H. J.; Zhang, H. L.; Biana, J. J.; Dong, L. S. Intriguing Crystallization Behavior and Rheological Properties of Radical-based Crosslinked Biodegradable Poly(3-hydroxybutyrate-co-4-hydroxybutyrate). CrystEngComm 2014, 16, 2702-2714.
-

- 26. Xu, P. X.; Zhang, C.; Qi, G. P.; Yang, W. J.; Ma, P. M. Morphology and Crystallization Kinetics of Regime Transition for Biosynthesized Polyhydroxyalkanoate. J. Polym. Res. 2022,29, 140-145.
-

- Polymer(Korea) 폴리머
- Frequency : Bimonthly(odd)
ISSN 0379-153X(Print)
ISSN 2234-8077(Online)
Abbr. Polym. Korea - 2023 Impact Factor : 0.4
- Indexed in SCIE
 This Article
This Article
-
2022; 46(5): 661-670
Published online Sep 25, 2022
- 10.7317/pk.2022.46.5.661
- Received on May 28, 2022
- Revised on Jun 29, 2022
- Accepted on Jun 30, 2022
 Services
Services
Shared
 Correspondence to
Correspondence to
- Ho-Jong Kang
-
Department of Polymer Science and Engineering, Dankook University, 152 Jukjeon-ro, Suji-gu, Yongin-si, Gyeonggi-do 16890, Korea
- E-mail: hjkang@dankook.ac.kr
- ORCID:
0000-0001-8411-3667









 Copyright(c) The Polymer Society of Korea. All right reserved.
Copyright(c) The Polymer Society of Korea. All right reserved.