- Study on Colloidal Stability of Gold Nanoparticles Modified with Sugar Molecules
*Department of Optometry, Seoul National University of Science and Technology, 138 Gongneung gil, Nowon-gu, Seoul 01811, Korea
**Convergence Institute of Biomedical Eng. & Biomaterials, Seoul National University of Science and Technology, 138 Gongneung gil, Nowon-gu, Seoul 01811, Korea- 당 분자를 이용한 금 나노입자의 콜로이드 안정성 연구
*서울과학기술대학교 안경광학과
**서울과학기술대학교 의공학-바이오소재(융합협동 프로그램)Reproduction, stored in a retrieval system, or transmitted in any form of any part of this publication is permitted only by written permission from the Polymer Society of Korea.
Surface modified gold nanoparticles can be applied in various fields with increased chemical resistance. In this study, gold nanoparticles were treated with sugar molecules to improve chemical stability. Glucose known as a reducing sugar, sucrose or trehalose, which is non-reducing sugars, was added to a dispersion of gold nanoparticles synthesized with citrate as a reducing agent. The color and absorbance of the dispersion were evaluated for colloidal stability. As a result, there was no significant difference in the size, shape, and optical properties of gold nanoparticles depending on the type of sugar. After the addition of PBS, dispersion stability was evaluated and the aggregation reaction over time was analyzed. It was found, the gold nanoparticles coated with the non-reducing sugar were more stable than those with the reducing sugar. Higher molecular weight sugar prevented the particle agglomeration. Therefore, it is expected that gold nanoparticles coated with non-reducing sugar can be applied stably in high ionic condition.
금 나노입자는 표면개질을 통해 내화학성을 높여 활용분야를 넓힐 수 있다. 본 연구는 당을 이용하여 화학적 환원법으로 제조된 금 나노입자의 표면 안정성을 개선하고자 하였다. 환원제로 Citrate를 사용하여 합성한 금 나노입자 분산액에 환원당인 glucose, 비환원당인 sucrose와 trehalose를 첨가한 후, 분산액의 색상 및 흡광도로 콜로이드 안정성을 평가하였다. 그 결과 금 나노입자의 크기와 형태 및 광학적 특성은 당의 종류 및 코팅 유무에 따른 유의한 차이는 보이지 않았다. PBS를 첨가한 후 분산 안정성을 평가하고, 시간에 따른 응집반응을 분석한 결과 환원당에 비해 비환원당으로 코팅된 금 나노입자가 더 안정적이었으며, 분자량이 높을수록 응집 저항성이 높게 나타났다. 따라서 비환원당으로 코팅된 금 나노입자는 이온농도가 높은 환경에서 금 나노입자를 안정적으로 적용할 수 있을 것으로 기대한다.
Gold nanoparticles (GNPs) prepared by chemical reduction were surface-modified using sugars with different molecular weights for colloidal stability. Analysis of resistance to aggregation showed that the surface stability of GNPs simply coated with a higher molecular weight and non-reducing sugar was significantly improved.
Keywords: gold nanoparticle, colloidal stability, sugar molecules, surface modification, aggregation reaction.
본 연구는 서울과학기술대학교 교내연구비로 수행되었습니다.
저자들은 이해상충이 없음을 선언합니다.
금 나노입자는 고유한 광학적, 전자기적 특성을 가지고 있어 의료, 환경, 산업 및 에너지 등 다양한 분야에서 활용되고 있다. 특히 금 나노입자는 생체적합성이 우수하고, 다양한 크기와 모양으로 제조할 수 있으며, 여러 표면 작용기를 도입할 수 있어 바이오 연구를 위한 대표적인 플랫폼으로 주목받고 있다.1-5 그러나 여러 장점에도 불구하고, 금 나노입자는 내화학성 및 장기간 보관에 따른 안정성이 떨어지므로 생체 내 적용에 한계가 있고, 활용범위 또한 제한된다.6 이에 따라 금 나노입자의 표면개질을 통해 안정성을 향상시키고자 하는 연구가 활발히 진행되고 있다.7,8
금 나노입자의 표면개질은 콜로이드 입자를 안정화할 뿐 아니라 금 나노입자의 효용성을 높일 수 있으므로 적용 분야에 따라 다양한 형태로 이루어지고 있다.9-13 일반적으로 많이 사용되는 방법은 표면에 싸이올기(-SH)를 가지고 있는 고분자를 환원제로 사용하거나, 합성된 금 나노입자의 표면에 정전기적 인력을 이용하여 고분자 물질을 적층하는 방법 등이 있다. Fuller 등에 의하면 고분자 전해질의 단층 및 다층 코팅은 금 나노입자의 표면에 DNA, 항체 및 단백질 리간드를 형성하여 체내에서 비선택적인 표면 흡착을 방지하고 표적효율을 높일 수 있어, 약물전달, 유전자치료, 영상진단 등에 금 나노입자를 활용할 수 있도록 돕는다고 알려져 있다.9 Liu 등은 금 나노입자의 표면을 양쪽성 이온으로 둘러쌈으로써 높은 염도와 단백질 흡착에 저항성이 높고, 종양 표적에 유리한 입자를 합성하기도 하였다.10 최근에는 Aldewachi 등이 시트레이트(citrate)로 환원된 금 나노입자의 안정성을 개선하기 위하여 펩티드 혼합물을 첨가하고, 금 나노입자의 표면에 펩티드 층이 형성됨으로써 고농도의 이온 환경에서도 형태를 유지할 수 있다고 보고하였다.11 한편, 금 나노입자를 고분자 매트릭스에 결합함으로써 그 응용범위를 넓힐 수 있는데,14-16 Miranda 등은 citrate로 환원된 금 나노입자를 polyethylene glycol diacrylate(PEGDA) 하이드로겔에 결합하여 웨어러블 바이오센서에 적용 가능한 생체적합성이 우수한 나노 입자를 설계하였다.14
금 나노입자를 제조하는 방법은 다양하지만, 균일한 입자를 생성하기 위해서는 Turkevich-Frens 방법이 많이 사용되고 있다.17,18 Turkevich-Frens 법은 수용액상에서 소량의 금 입자를 빠르게 환원시킬 수 있고, 금 이온의 농도와 시트르산의 농도 비율을 조정하여 나노입자의 크기와 모양을 제어하기에 용이하다.19,20 금 나노입자의 합성과정에서 citrate와 같은 화학물질을 대신하여 당을 환원제로 이용할 수도 있다. 당은 독성이 없고 환경 친화적이며, 자연계에서 쉽게 얻을 수 있다는 장점이 있다. 일반적으로 환원제로 작용할 수 있는 당은 헤미아세탈을 이루고 있는 알데히드기(-CHO)나 케톤기 (-CO-)를 가지고 있어야 하며, 헤미아세탈을 가지고 있는 당을 환원당이라 한다.
본 연구는 화학적 환원법으로 제조된 금 나노입자의 콜로이드 안정성을 개선하고자 하였다. 합성된 금 나노입자 분산액에 분자량이 다른 당을 첨가하였고, 당으로 코팅된 금 나노입자의 광학적 특성 변화를 관찰하고 응집에 대한 저항성을 분석하였다.
재료. 본 연구의 시약은 Sigma Aldrich사에서 제조된 Gold(III) chloride trihydrate(HAuCl4)≥99.9%, Sodium citrate dihydrate, D-(+)-Glucose, Sucrose, D-(+)-Trehalose dihydrate를 사용하였다. 사용된 Glucose, Sucrose, Trehalose의 분자량은 각각 180.16, 342.30, 378.33 g/mol이다.
금 나노입자의 합성. 금 나노입자는 수용액 상에서 시트르산을 환원제로 사용하는 Turkevich-Frens 법으로 합성되었다.18 증류수 30 mL를 90 oC로 가열한 후, 10 mM HAuCl4 2 mL를 첨가하고, 온도를 유지하며 RPM 1000으로 10분 동안 교반하였다. 이 용액에 38.8 mM sodium citrate를 6 mL를 첨가한 후, 온도를 유지하며 15분 동안 교반하였다. 이 때, 용액의 색상이 붉은색으로 변함에 따라 금 나노입자의 생성을 확인할 수 있다. 합성된 금 나노입자 분산액은 반응하지 않고 남아있는 이온들을 제거하기 위해 반투과성막에 담아 증류수에 1시간 정도 침지시킨 후 사용하였다.
분자량이 다른 당을 이용한 금 나노입자의 코팅. 금 나노입자 분산액이 9 mL씩 담긴 4개의 삼각 플라스크에 증류수와 100 mM의 glucose, sucrose, trehalose를 각각 1 mL씩 첨가하였다. RPM 1000으로 50 oC에서 30분간 교반하였고, 실온에서 식힌 후 색상과 흡광도의 변화를 측정하였다.
분산도 평가. 금 나노입자의 이온에 대한 안정성을 평가하기 위하여 인산완충식염수(phosphate buffered saline, PBS)를 사용하였다. NaCl의 농도가 0-54.8 mM이 되도록 금 나노입자 분산액에 PBS를 첨가한 후, 상온에 두고 변화를 관찰하였다. 이 중 가장 높은 농도(54.8 mM)의 NaCl를 첨가한 분산액은 1시간 동안 추적 관찰하여 색상과 흡광도의 변화를 측정하였다.
입자의 물성분석. 용액의 색상은 스마트폰(Note 20, Samsung, Korea)으로 촬영하였고, 나노입자의 크기와 분포도는 동적광산란계(Zetasizer, Malvern, UK)와 투과전자현미경(Cs-STEM, Neo Arm, Jeol, Japan)으로 촬영하였고, 나노입자의 크기와 분포도는 동적광산란계(DLS)와 투과전자현미경(TEM)을 이용하였다. 표면 플라즈몬 공명(SPR) 파장대는 자외선-가시광선 분광광도계(Nano-MD, Scinco, Korea)를 이용하여 측정하였다.
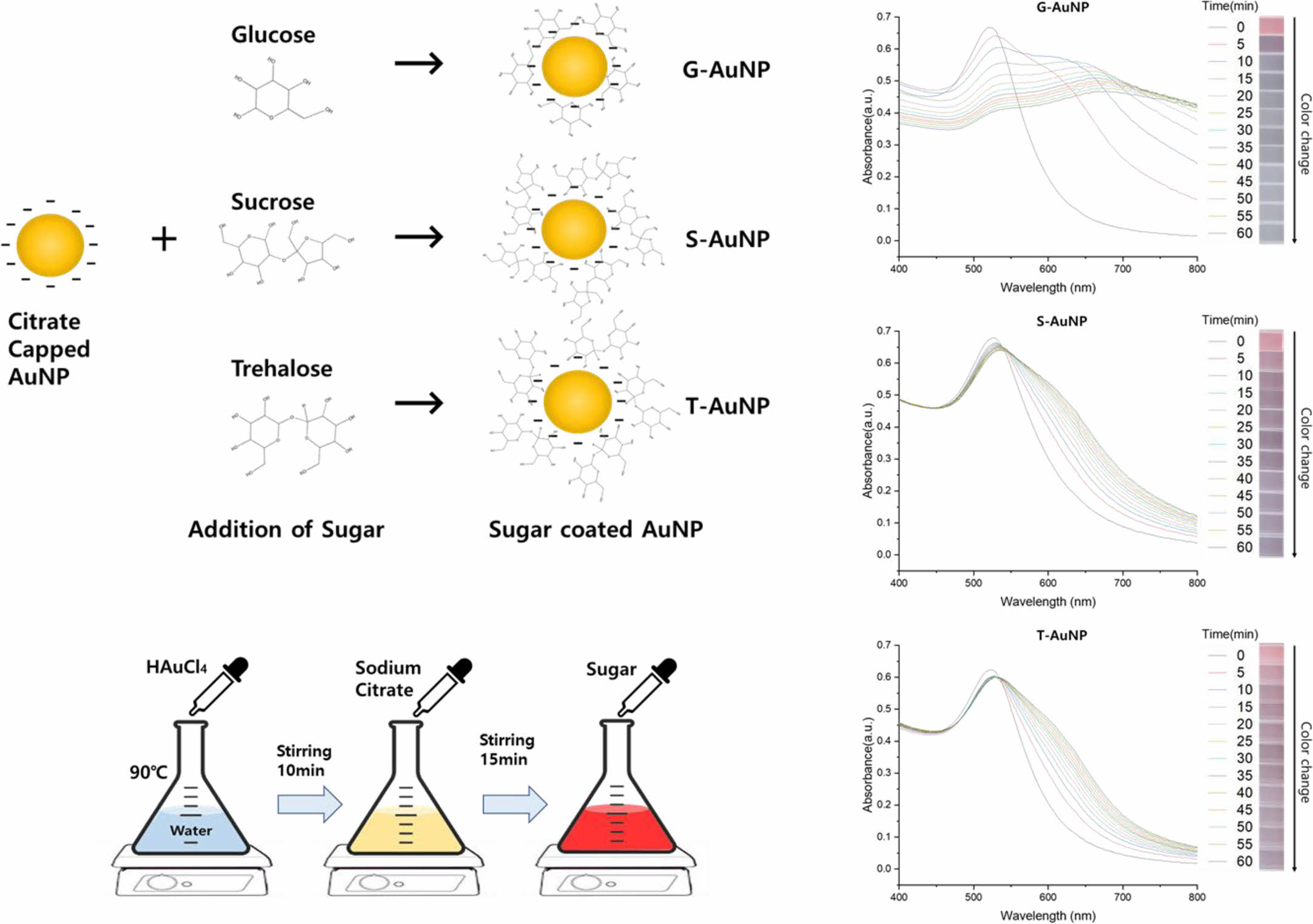
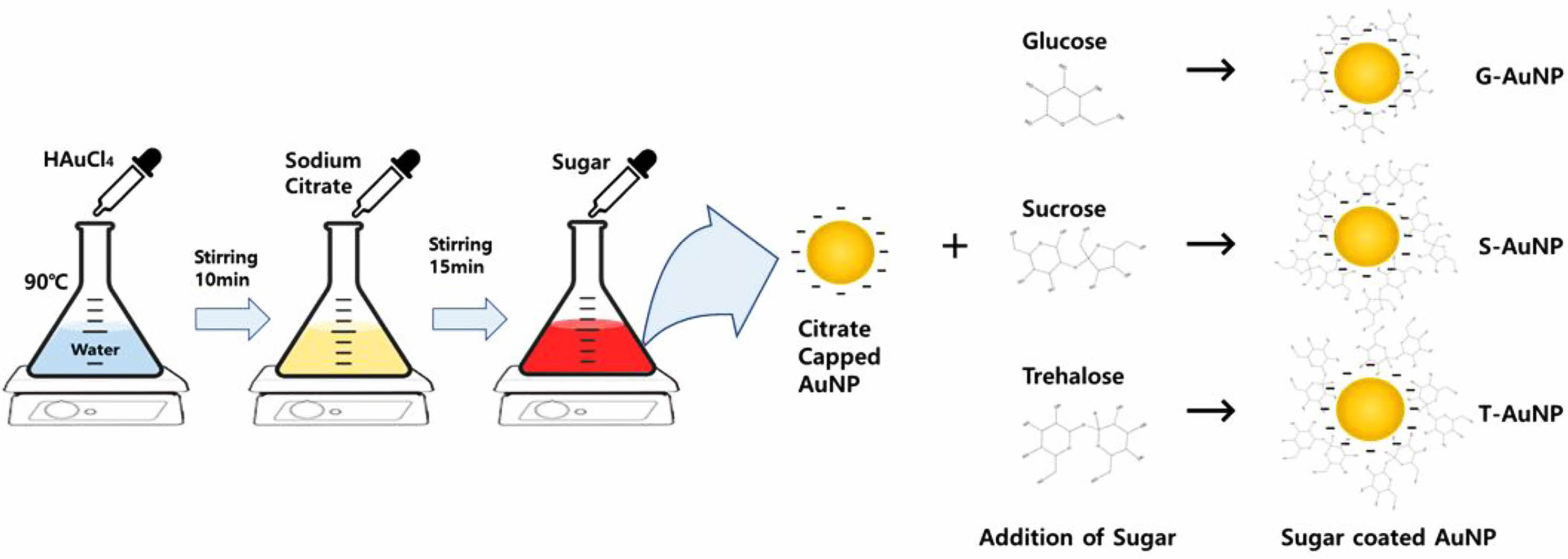
금 나노입자의 제조는 Turkevich-Frens 법을 사용하였고, 금 나노입자의 표면개질을 위해 환원당인 glucose와 비환원당인 sucrose와 trehalose를 사용하였다(Figure 1).
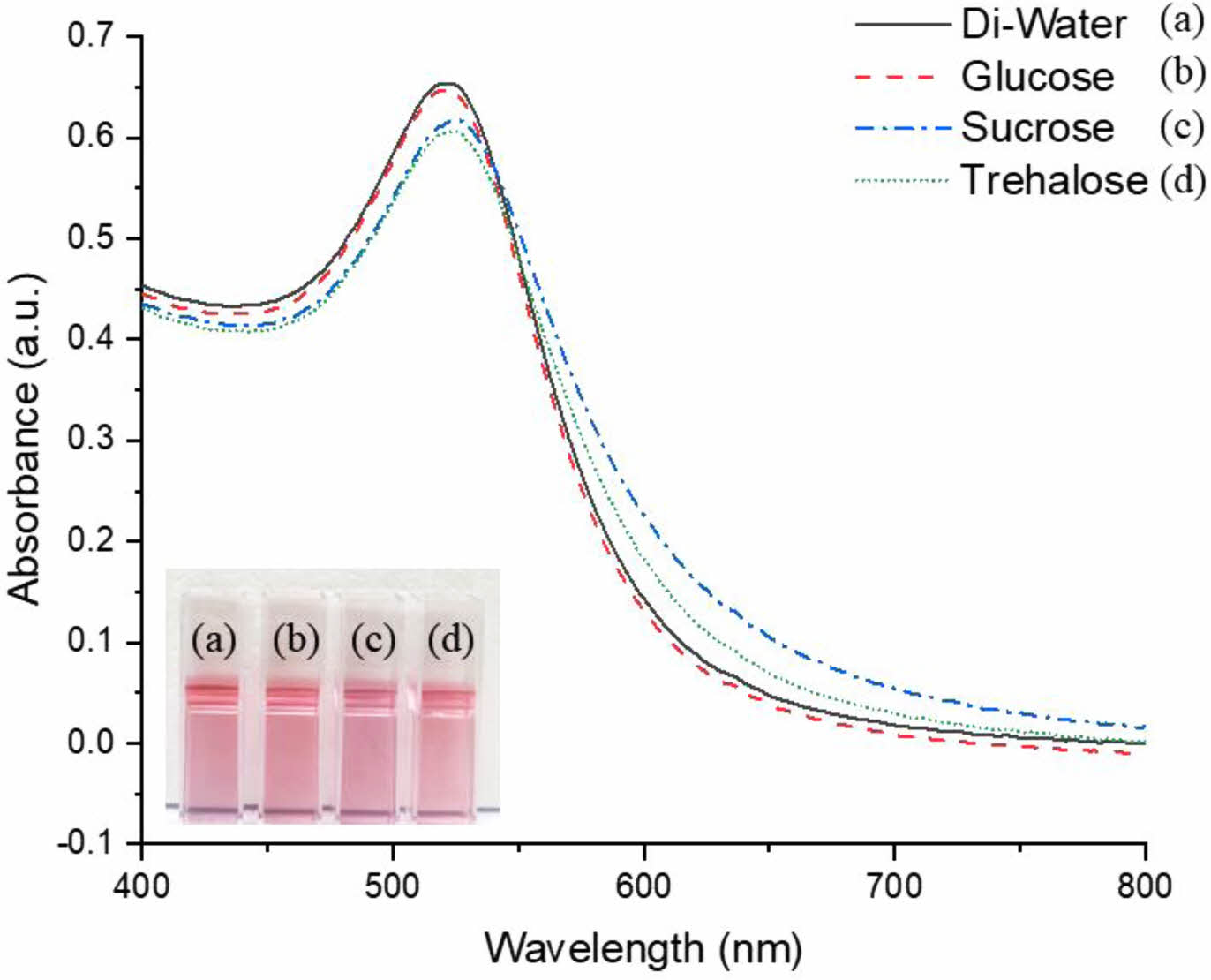
금 나노입자의 광학적 특성. 당을 첨가한 금 나노입자 분산액의 색상과 흡광도를 Figure 2에 나타내었다. 용액의 색상은 붉은색이었고, 가시광선 영역에서의 최대흡수파장은 520 nm 부근에서 측정되었다. 이것은 일반적으로 금 나노입자에서 나타나는 광학적 특성이며,21-23 본 연구에서도 당의 첨가 여부 및 종류에 상관없이 금 나노입자 분산액의 색상과 흡광도는 유사하게 나타났다. 다만 sucrose와 trehalose를 첨가하였을 때, 최대흡수파장이 약 3 nm 정도 적색편이 되고 흡광도가 다소 낮게 측정되었다. 이러한 현상은 입자의 크기나 모양이 변함에 따라 금 나노입자의 전위가 소폭 변하였음을 의미하지만,23 근소한 차이로 당의 첨가 여부가 금 나노입자의 광학적 특성에 미치는 영향은 미미한 것으로 여겨진다.
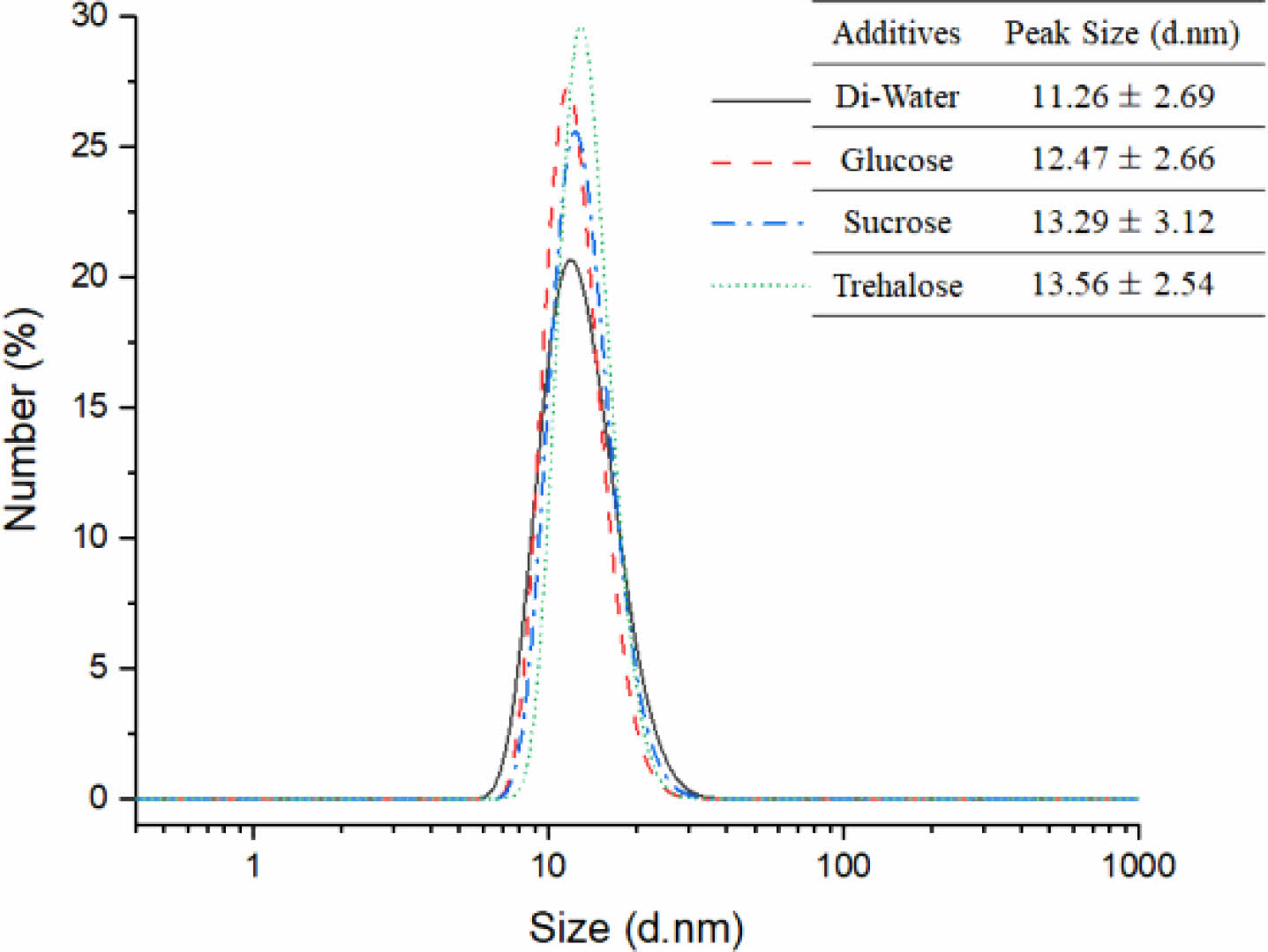
금 나노입자의 크기 및 형태. DLS로 측정한 금 나노입자의 분산 분포를 Figure 3에 수평균 분산도로 나타내었다. 가장 많은 수를 차지하는 입자들의 평균 크기는 10-15 nm 내외로 당의 종류와 관계없이 비슷한 크기로 측정되었다.
Figure 4은 TEM으로 입자를 관찰한 것으로 (a)-(d)는 차례대로 금 나노입자 분산액에 증류수, glucose, sucrose, 그리고 trehalose를 첨가한 것이다. 균일한 구형의 입자를 관찰할 수 있으며, 입자의 크기는 DLS로 측정한 크기와 유사하다. Figure 4의 오른쪽 이미지는 carbon lacey grid에 걸쳐져 있는 개별 입자를 좀 더 정밀하게 촬영한 것으로 금 나노입자의 주위를 둘러싸고 있는 유기물층을 관찰할 수 있다. 이러한 코어-쉘 구조는 금속 표면에 보호막을 형성하여 분산 안정성을 높이는 데에 중요한 역할을 한다.24-26 본 연구에서는 당으로 입자 표면을 코팅하여 쉘 형성을 강화하고자 하였고, TEM 이미지에서 근소한 차이이지만 유기물 층의 두께가 증가한 것을 확인할 수 있었다.
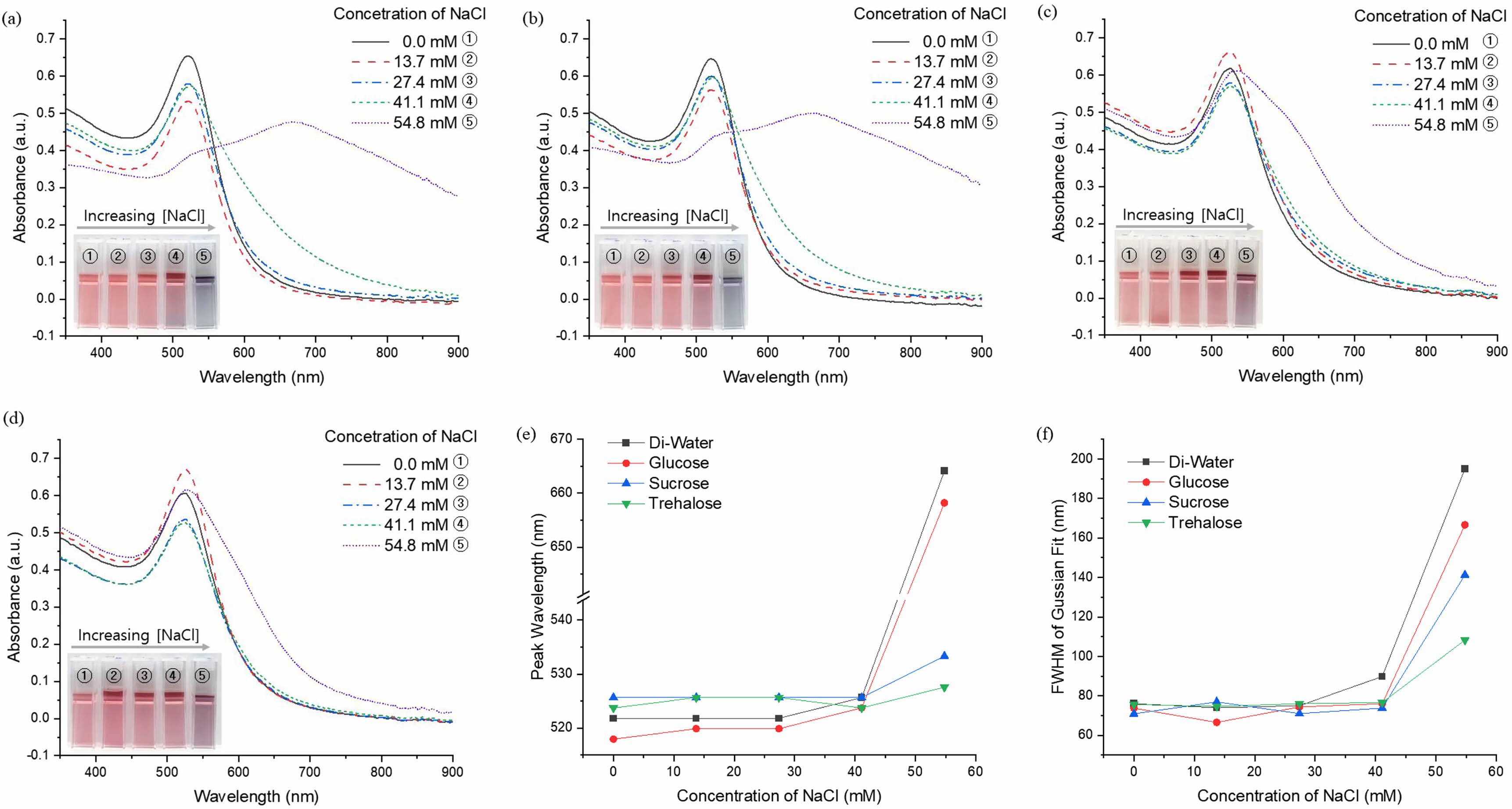
이온 안정성 평가. 당이 함유된 금 나노입자 분산액에 PBS를 첨가한 후, 상온에 두고 변화를 관찰하였다. 시간이 지남에 따라 분산액의 색상은 붉은색에서 보라색으로 변하였고, NaCl의 농도가 높을수록 색 변화는 더 많이 일어났다. 1시간 동안 반응시킨 후에, 분산액의 색상과 흡광도를 측정하여 Figure 5에 나타내었다. 흡광도를 측정한 결과, NaCl의 농도가 증가할수록 최대흡수파장은 적색으로 이동하고, 가우시안 함수로 피팅한 스펙트럼의 반치전폭(full width at half maximum, FWHM)은 넓어졌다. 이러한 현상은 고농도의 이온 환경에서 금 나노입자를 둘러싸고 있는 전하가 약해지고 입자가 응집되어 나타나는 현상으로, 입자의 크기와 분산이 증가하였음을 의미한다.27 특히 NaCl의 농도가 50 mM 이상일 때는 환원당을 포함하는 나노입자는 급격한 변화를 보였는데, sucrose와 trehalose를 첨가하였을 때는 입자의 변화가 상대적으로 작았다(Figure 5(e), 5(f)).
상온에서 1일이 지난 후, 분산액의 색상은 전반적으로 붉은색이 감해지거나 보라색으로 변하였다. 금 나노입자의 색상은 입자의 크기를 나타내는 대표적인 지표로 입자의 크기가 증가할수록 붉은색에서 보라색으로 변화한다. 분산액의 색상이 변화한 것은 응집으로 금 나노입자의 크기가 증가하였고, 이온 환경에서 콜로이드 안정성이 저하되었음을 나타낸다.6 NaCl의 농도가 54.8 mM일 때는 trehalose를 첨가한 것을 제외한 나머지 분산액에서 침전물이 관찰되었다. 이로써 본 연구에서 콜로이드 안정성을 위해 첨가한 당 중에서는 trehalose가 가장 효과적인 것으로 판단된다(Figure 6).
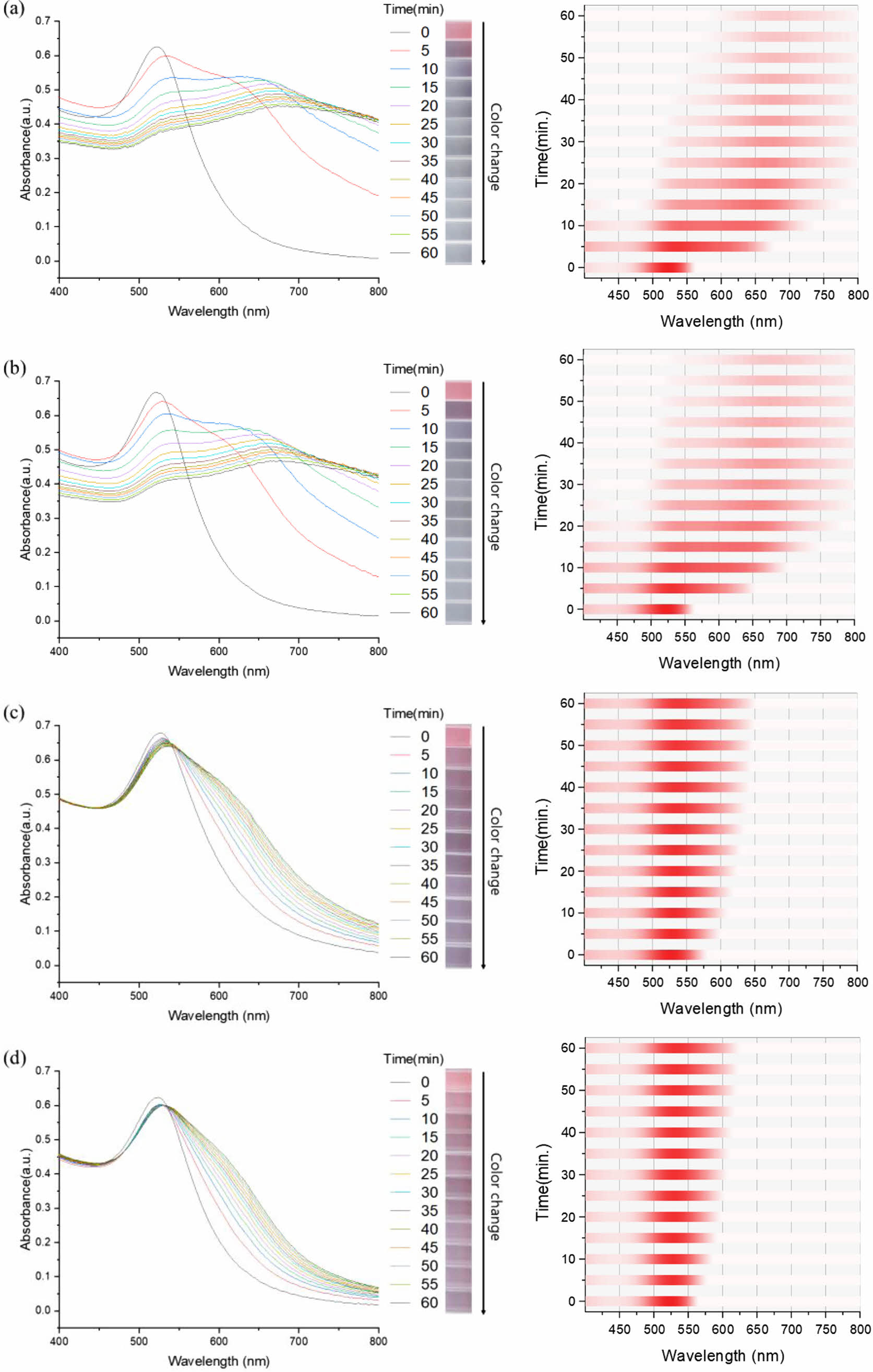
응집 저항성 평가. 고농도(54.8 mM)의 NaCl를 첨가한 후, 금 나노입자 분산액의 색상과 흡광도의 변화를 1시간 동안 추적 관찰하였다(Figure 7). 시간이 지남에 따라 나타나는 흡광도의 변화를 보면, 최대흡수파장은 적색 이동하였고, 흡광도 스펙트럼은 폭이 넓어지면서 전체적으로 낮아졌다. 이는 화학적 환원법으로 합성된 금 나노입자가 고이온의 환경에서 쉽게 산화되어 응집이 일어남을 시사한다.28 Citrate 환원법으로 합성된 금 나노입자 분산액은 입자의 표면을 둘러싸고 있는 citrate 이온의 정전기적 반발력에 의해 안정화되는데, 주변에 이온이 증가하면 citrate 이온이 해리되면서 금 나노입자의 응집을 유발하게 되는 것으로 알려져 있다.6 본 연구에서도 당을 첨가하지 않은 것과 glucose를 첨가한 금 나노입자 분산액에서 색상과 흡광도의 변화가 뚜렷하게 나타났다(Figure 7(a), 7(b)). 이에 반해 sucrose와 trehalose를 첨가한 분산액은 색상 지속력이 우수하였고, 최대흡수파장이 약간 이동하였으나 전체적으로 흡광도 스펙트럼을 안정적으로 유지하였다(Figure 7(c), 7(d)). 이것은 앞서 언급한 것처럼 당이 금 나노입자의 표면에 흡착되어 보호막을 형성함으로써 입자가 응집되는 것을 방어하는 기능을 하는 것으로 판단된다.
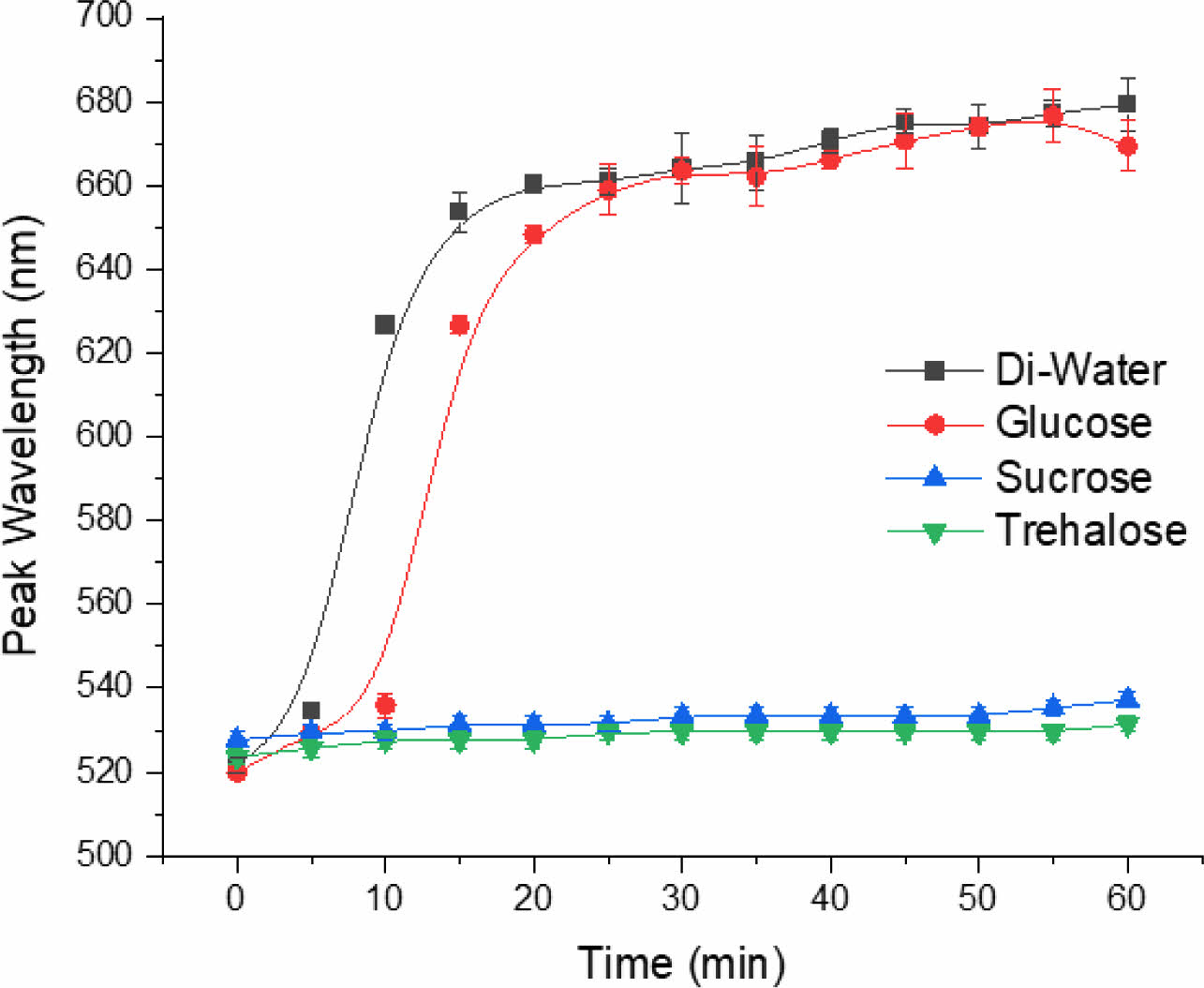
Figure 7의 오른쪽 그림은 시간에 따른 흡광도의 변화를 색으로 나타낸 것으로, 응집반응은 반응 초기에 빠르게 일어나고 시간이 지날수록 변화의 속도가 느려지는 것으로 보인다. Figure 8에 나타낸 최대흡수파장의 변화도 비슷한 양상을 보이고 있으며, 증류수와 glucose를 첨가한 분산액에서 반응초기에 파장이 가파르게 이동하는 것을 확인할 수 있다.
본 연구에서 glucose가 금 나노입자의 분산안정성에 미치는 효과는 미미한 것으로 나타났다. 기존 연구들에 의하면, glucose는 알데히드기를 가지고 있는 환원당으로 나노입자의 친환경 합성에 널리 쓰이고 있다.23 이러한 환원력 때문에 금 나노입자 분산액에 첨가한 glucose는 기존에 금 나노입자를 둘러싸고 있는 citrate 이온과 일정부분 경합하여 금 나노입자의 코팅 효과가 거의 나타나지 않은 것으로 보인다. 이에 반해 sucrose와 trehalose는 비환원당으로 citrate의 환원력을 저해하지 않으면서, 기존 입자의 표면에 반데르발스 힘에 의해 흡착되는 것으로 여겨진다. Zhou 등의 연구에 따르면 적층된 유기물 쉘은 금 나노입자의 표면 전위의 변화를 가져오고, 금속 표면의 보호 및 방패 역할을 함으로써 응집에 대한 저항성을 높인다고 하였다.24 본 연구에서도 비환원당으로 코팅된 금 나노입자는 이온농도가 높은 환경에서 안정적인 분산상태를 유지하는 것으로 확인되었다.
|
Figure 1 Scheme of sugar-coated gold nanoparticles preparation. |
|
Figure 2 UV-Vis spectra of gold nanoparticles coated by sugars with different molecular weights: (a) di-water; (b) glucose; (c) sucrose; (d) trehalose. |
|
Figure 3 Size distribution of gold nanoparticles coated with different sugars by dynamic light scattering |

|
Figure 4 TEM images of sugar-coated gold particles supported on a carbon lacey grid: (a) di-water; (b) glucose; (c) sucrose; (d) trehalose |
|
Figure 5 UV-Vis spectral variation of sugar-coated gold nanoparticles according to various concentration of NaCl in PBS: (a) di-water; (b) glucose; (c) sucrose; (d) trehalose; (e) shift of the peak wavelength; (f) expansion of FWHM. |

|
Figure 6 Color variation of sugar-coated gold nanoparticles according to various concentration of NaCl in PBS after 1 day: (a) di-water; (b) glucose; (c) sucrose; (d) trehalose. |
|
Figure 7 Kinetics of sugar-coated gold nanoparticle aggregation at 54.8 mM NaCl in PBS for 1 hour: (a) di-water; (b) glucose; (c) sucrose; (d) trehalose. |
|
Figure 8 Absorption peak shift of UV-Vis spectra of sugar-coated gold nanoparticles over the reaction time. |
본 연구는 Trukevich-Frens 법으로 10 nm 내외의 균일한 금 나노입자를 합성하였고, 금 나노입자의 표면안정성을 높이기 위하여 분자량이 서로 다른 당을 이용하였다. 당으로 코팅된 금 나노입자의 색상은 붉은색을 띠었고, 최대흡수파장은 520 nm 부근으로 당의 종류에 따른 차이는 거의 없었다. 입자의 형태는 구형이었고, 금 나노입자 주위를 둘러싸고 있는 유기물층이 있음을 확인할 수 있었다. PBS를 첨가하여 안정성을 평가한 결과, 비환원당으로 코팅된 금 나노입자가 이온농도가 높은 환경에서 더 안정적인 것으로 나타났다. 본 연구에서 비환원당을 첨가하는 것만으로 간단하게 표면개질을 할 수 있었으며, 금 나노입자의 콜로이드 안정성이 향상되었음을 확인하였다.
- 1. Shah, M.; Badwaik, V.; Kherde, Y.; Waghwani, H. K.; Modi, T.; Aguilar, Z. P.; Rodgers, H.; Hamilton, W.; Marutharaj, T.; Webb, C.; Lawrenz, M. B.; Dakshinamurthy, R. Gold Nanoparticles: Various Methods of Synthesis and Antibacterial Applications. Front Biosci. 2014, 19, 1320-1344.
-

- 2. Wang, C.; Yu, C. Detection of Chemical Pollutants in Water Using Gold Nanoparticles as Sensors: A Review. Rev. Anal. Chem. 2013, 32, 1-14.
-

- 3. Jain, P. K.; Lee, K. S.; El-Sayed, I. H.; El-Sayed, M. A. Calculated Absorption and Scattering Properties of Gold Nanoparticles of Different Size, Shape, and Composition: Applications in Biological Imaging and Biomedicine. J. Phys. Chem. B 2006, 110, 7238-7248.
-

- 4. Mariño-López, A.; Sousa-Castillo, A.; Carbó-Argibay, E.; Otero-Espinar, F.; Alvarez-Puebla, R. A.; Pérez-Lorenzo, M.; Correa-Duarte, M. A. Laser-protective Soft Contact Lenses: Keeping an Eye on the Eye Through Plasmonics. Appl. Mater. Today 2019, 15, 1-5.
-

- 5. Elahi, N.; Kamali, M.; Baghersad, M. H. Recent Biomedical Applications of Gold Nanoparticles: A Review. Talanta 2018, 184, 537-556.
-

- 6. Cho, T.; Hackley, V. Assessing the Chemical and Colloidal Stability of Functionalized Gold Nanoparticles, Special Publication (NIST SP) [Online]; National Institute of Standards and Technology: Gaithersburg, 2018. https://doi.org/10.6028/NIST.SP.1200-26 (accessed Jun 28, 2021).
-

- 7. Alex, S.; Tiwari, A. Functionalized Gold Nanoparticles: Synthesis, Properties and Applications-a Review. J. Nanosci. Nanotechnol. 2015, 15, 1869-1894.
-

- 8. Liu, S.; Lämmerhofer, M. Functionalized Gold Nanoparticles for Sample Preparation: A Review. Electrophoresis 2019, 40, 2438-2461.
-

- 9. Fuller, M. A.; Köper, I. Biomedical Applications of Polyelectrolyte Coated Spherical Gold Nanoparticles. Nano Converg. 2019, 6, 11.
-

- 10. Liu, X.; Jin, Q.; Ji, Y.; Ji, J. Minimizing Nonspecific Phagocytic Uptake of Biocompatible Gold Nanoparticles with Mixed Charged Zwitterionic Surface Modification. J. Mater. Chem. 2012, 22, 1916-1927.
-

- 11. Aldewachi, H.; Woodroofe, N.; Gardiner, P. Study of the Stability of Functionalized Gold Nanoparticles for the Colorimetric Detection of Dipeptidyl Peptidase IV. Appl. Sci. 2018, 8, 2589.
-

- 12. Kim, S. Y.; Yoo, M. S.; Jung, S. R.; Paek, K. Y.; Kim, B. J. J.; Bang, J. Controlling the Location of Thermally Stable Au Nanoparticles with Tailored Surface Property Within Block Copolymer Templates. Polym. Korea 2011, 35, 238-243.
- 13. Kim, E. J.; Yeum, J. H.; Ghim, H. D.; Lee, S. G.; Lee, G. H.; Lee, H. J.; Han S. I.; Choi, J. H. Ultrasmall Polyethyleneimine-gold Nanoparticles with High Stability. Polym. Korea 2011, 35, 161-165.
- 14. Miranda, B.; Moretta, R.; De Martino, S.; Dardano, P.; Rea, I.; Forestiere, C.; De Stefano, L. A PEGDA Hydrogel Nanocomposite to Improve Gold Nanoparticles Stability for Novel Plasmonic Sensing Platforms. J. Appl. Phys. 2021, 129, 033101.
-

- 15. Baipaywad, P.; Park, Y. E.; Kim, Y.; Park, H. Effect of PNIPAM Formulation on Fabrication of Nanogels Containing Gold Nanoparticles. Polym. Korea 2016, 40, 547-552.
-

- 16. Kim, Y. H.; Kim, B. Preparation of Poly(ethylene glycol) Hydrogel Particles Containing Gold Nanoparticles by In Situ Polymerization. Polym. Korea 2020, 44, 784-789.
-

- 17. De Souza, C. D.; Nogueira, B. R.; Rostelato, M. E. C. Review of the Methodologies Used in the Synthesis Gold Nanoparticles by Chemical Reduction. J. Alloys Compd. 2019, 798, 714-740.
-

- 18. Dong, J.; Carpinone, P. L.; Pyrgiotakis, G.; Demokritou, P.; Moudgil, B. M. Synthesis of Precision Gold Nanoparticles Using Turkevich Method. KONA 2020, 37, 224-232.
-

- 19. Kimling, J.; Maier, M.; Okenve, B.; Kotaidis, V.; Ballot, H.; Plech, A. Turkevich Method for Gold Nanoparticle Synthesis Revisited. J. Phys. Chem. B 2006, 110, 15700-15707.
-

- 20. Polte, J. Fundamental Growth Principles of Colloidal Metal Nanoparticles–A New Perspective. Cryst. Eng. Comm. 2015, 17, 6809-6830.
-

- 21. Scampicchio, M.; Fuenmayor, C. A.; Mannino, S. Sugar Determination via the Homogeneous Reduction of Au Salts: A Novel Optical Measurement. Talanta 2009, 79, 211-215.
-

- 22. Qi, Z. M.; Zhou, H. S.; Matsuda, N.; Honma, I.; Shimada, K.; Takatsu, A.; Kato, K. Characterization of Gold Nanoparticles Synthesized Using Sucrose by Seeding Formation in the Solid Phase and Seeding Growth in Aqueous Solution. J. Phys. Chem. B 2004, 108, 7006-7011.
-

- 23. Imbraguglio, D.; Giovannozzi, A. M.; Rossi, A. M. Nanometrology. In Metrology and Physical Constants; Bava, E., Kuhne, M., Rossi, A. M., Eds.; IOS Press: Bologna, 2013; pp. 193-220.
- 24. Zhou, J.; Ralston, J.; Sedev, R.; Beattie, D. A. Functionalized Gold Nanoparticles: Synthesis, Structure and Colloid Stability. J. Colloid Interface Sci. 2009, 331, 251-262.
-

- 25. Kim, T.; Kang, H.; Jeong, S.; Kang, D. J.; Lee, C.; Lee, C. H.; Seo, M. K.; Lee, J. Y.; Kim, B. J. Au@ Polymer Core–shell Nanoparticles for Simultaneously Enhancing Efficiency and Ambient Stability of Organic Optoelectronic Devices. ACS Appl. Mater. Interfaces 2014, 6, 16956-16965.
-

- 26. Uchimiya, M.; Pignatello, J. J.; White, J. C.; Hu, S. L.; Ferreira, P. J. Surface Interactions Between Gold Nanoparticles and Biochar. Sci. Rep. 2017, 7, 5027.
-

- 27. Kim, T.; Lee, C. H.; Joo, S. W.; Lee, K. Kinetics of Gold Nanoparticle Aggregation: Experiments and Modeling. J. Colloid Interface Sci. 2008, 318, 238-243.
-

- Polymer(Korea) 폴리머
- Frequency : Bimonthly(odd)
ISSN 0379-153X(Print)
ISSN 2234-8077(Online)
Abbr. Polym. Korea - 2023 Impact Factor : 0.4
- Indexed in SCIE
 This Article
This Article
-
2022; 46(1): 68-73
Published online Jan 25, 2022
- 10.7317/pk.2022.46.1.68
- Received on Sep 8, 2021
- Revised on Oct 6, 2021
- Accepted on Oct 7, 2021
 Services
Services
Shared
 Correspondence to
Correspondence to
- Hyeran Noh
-
*Department of Optometry, Seoul National University of Science and Technology, 138 Gongneung gil, Nowon-gu, Seoul 01811, Korea
**Convergence Institute of Biomedical Eng. & Biomaterials, Seoul National University of Science and Technology, 138 Gongneung gil, Nowon-gu, Seoul 01811, Korea - E-mail: hrnoh@seoultech.ac.kr
- ORCID:
0000-0003-4667-6754










 Copyright(c) The Polymer Society of Korea. All right reserved.
Copyright(c) The Polymer Society of Korea. All right reserved.