- Preparation and Characterization of Polyurethane Using Cardanol-Based Bio-Polyol Obtained from One-Pot Synthetic Method
Department of Chemical Engineering, Kyonggi University, 154-42, Gwanggyosan-ro, Yeongtong-gu, Suwon 16227, Korea
- 한 단계 합성 방법을 통한 카다놀 기반 바이오 폴리올 합성 및 이를 이용한 폴리우레탄의 제조 및 특성
경기대학교 화학공학과
Reproduction, stored in a retrieval system, or transmitted in any form of any part of this publication is permitted only by written permission from the Polymer Society of Korea.
In this study, a cardanol based bio-polyol (CBP) was prepared via one-pot synthesis method. The synthesis of CBP was proceeded via Mannich reaction using cardanol, formaldehyde, and ethanolamine. The chemical structure of CBP was confirmed via 1H NMR and FTIR. Then, bio-polyurethane (CBPU) was prepared using CBP and hexamethylene diisocyanate (HDI). For the comparison experiments, polyethylene glycol (PEG), petroleum-based polyol, was applied to prepare a polyurethane (PEGU) as a control sample. From analyses results for TGA, UTM, chemical resistance test, and antibacterial test for CBPU and PEGU, it was found that CBPU showed higher tensile strength, chemical resistance, and antibacterial properties against E. coli compared to PEGU.
본 연구에서는 한 단계의 합성 방법을 통해 카다놀 기반 바이오 폴리올(CBP)을 합성하였다. CBP는 카다놀, 포름알데히드 수용액, 에탄올아민을 사용한 Mannich reaction을 통해 제조하였으며, 1H NMR과 FTIR 분석을 통해 CBP가 성공적으로 합성되었음을 확인하였다. CBP와 헥사메틸렌 디이소시아네이트(HDI)를 우레탄 반응하여 바이오 폴리우레탄(CBPU)을 제조하였으며, 폴리에틸렌글리콜(PEG)을 사용하여 제조한 석유계 폴리우레탄(PEGU)을 대조군으로 사용하여 TGA, UTM, 내화학성, 항균성에 대한 분석을 수행하였다. 이러한 분석 결과 CBPU는 CBP 고유의 화학적 분자 구조 차이를 바탕으로 대조군 PEGU와 비교하여 E. coli에 대한 높은 항균성과 우수한 내화학성 및 높은 인장강도를 가지고 있음을 확인하였다.
Bio-polyol (CBP) was prepared by one-pot synthesis method using cardanol, ethanolamine, and formaldehyde. Bio-polyurethane (CBPU) prepared with CBP and diisocyanate (HDI) was found to have relatively high mechanical strength, thermal stability, chemical resistance, and antibacterial properties due to the influence of molecular structure for CBP in CBPU.
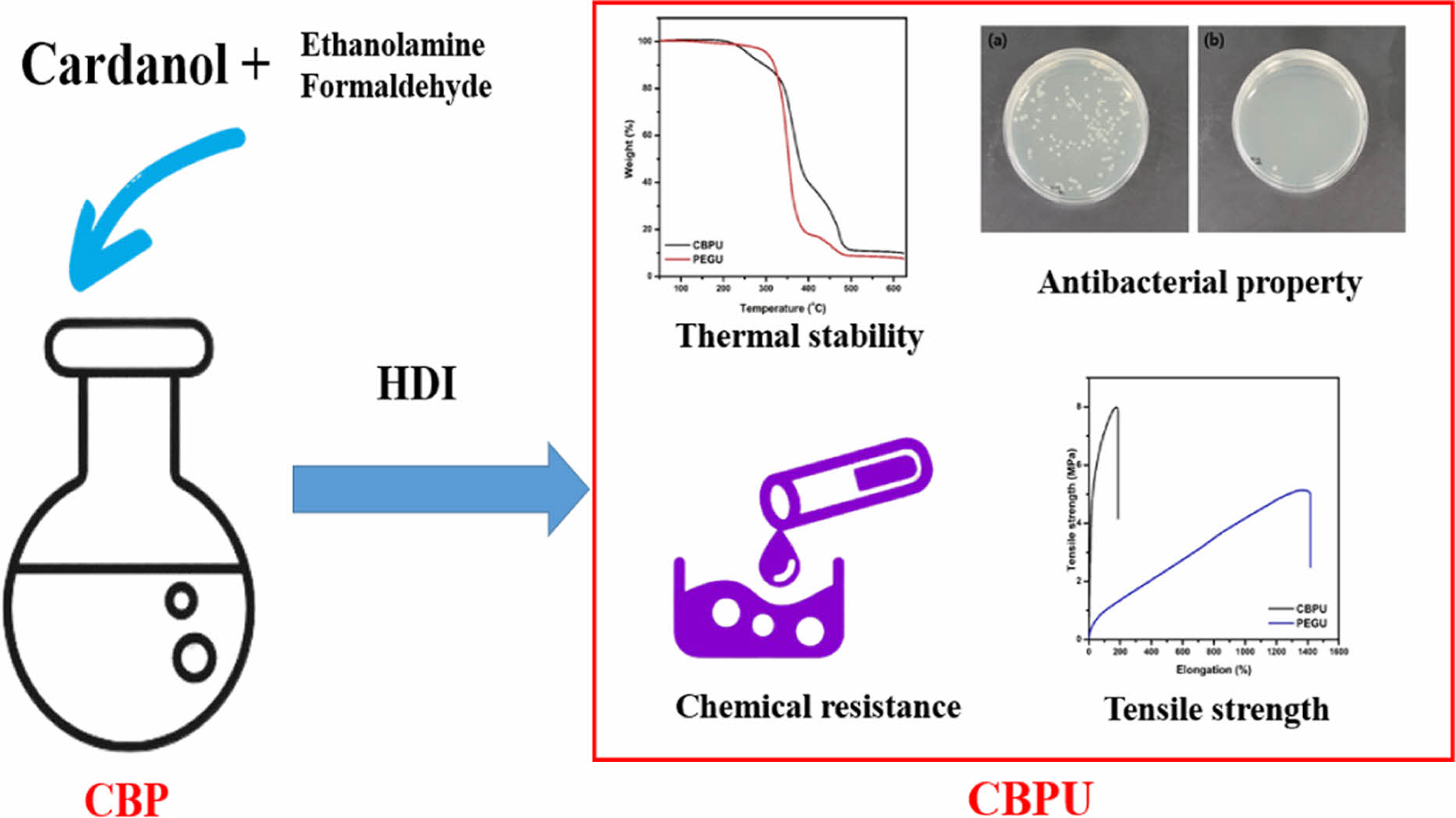
Keywords: cardanol, polyurethane, bio-polyol, antibacterial property, mechanical property.
본 연구는 2021학년도 경기대학교 대학원 연구원장학생 장학금 지원에 의하여 수행되었음.
폴리우레탄은 분자 내에 다가 수산기를 지닌 폴리올과 이소시아네이트의 반응을 통해 제조되는 고분자로 우수한 기계적 물성과 및 용이한 가공성 등의 많은 장점을 바탕으로 전자, 가구, 의류, 자동차 내장재, 코팅 등의 다양한 산업 분야에서 널리 사용되고 있다.1,2 하지만, 폴리우레탄의 주원료 물질인 폴리올과 이소시아네이트가 대부분 석유 화학 산업에서 얻어지는 특성상 한정 자원인 원유의 가격에 따라 폴리우레탄의 생산 단가가 불안정한 변동을 하게 되는 문제점을 가지고 있다. 이에 따른 폴리올과 이소시아네이트의 생산 단가 의존성 및 생산 과정에서 발생하는 이산화탄소 발생 문제는 폴리우레탄 산업이 당면해 있는 중요한 문제점 중의 한가지이다. 이에 따라 폴리우레탄의 주재료 중 하나인 폴리올을 친환경 바이오 폴리올(bio-polyol)로 대체하기 위한 노력은 환경적인 측면에서 폴리우레탄 산업의 지속 가능성을 향상시키는 것에 대한 의미가 있으며, 특히 바이오 매스 및 재생 가능한 원료로부터 바이오 폴리올을 개발하는 것은 석유산업에 대한 폴리우레탄 산업의 의존성을 낮출 수 있다는 점에서 큰 관심을 받고 있다.3
현재까지 대두유, 팜유, 면실유, 사탕수수, 옥수수 등의 식물성 유지 기반 바이오 매스를 이용한 바이오 폴리올 합성에 대한 연구는 폭넓게 진행되었다.4,5 하지만, 이러한 식용 바이오 매스는 식량자원을 직접적으로 사용한다는 점과 이에 따른 애그플레이션 현상을 야기할 수 있는 문제점을 지니고 있다. 따라서, 친환경적인 장점을 유지하면서 식량자원을 사용한다는 문제점을 해결하기 위한 대안으로 식용 자원이 아닌 농업 폐기물 등을 재활용하여 바이오 폴리올을 생산하기 위한 노력이 지속적으로 진행되었다.6
최근 석유 화학 물질을 대체할 수 있는 비식용 바이오 매스로써, 캐슈넛 껍질액(cashew nut shell liquid)이 주목받고 있다.7 캐슈넛 껍질액은 카다놀, 카돌, 아나카딕산 및 2-메틸카돌의 혼합물로 캐슈산업의 부산물로부터 얻어지며 연간 300000-360000 톤이 생산된다.8 캐슈넛 껍질액의 간단한 증류과정을 통해 얻어지는 카다놀(cardanol)은 페놀 유도체의 메타 위치에 15개의 불포화 탄화수소 사슬을 지니며 유기 용매에 대한 용해도가 높기 때문에 다양한 화학적 개질이 가능하다.9
이러한 카다놀의 장점을 바탕으로 카다놀 기반 바이오 폴리올에 대한 다양한 연구가 진행되었으며, 합성 방법은 화학적 구조상 카다놀의 개질 위치를 바탕으로 다음과 같이 크게 두 가지 방법으로 나뉜다. 첫번째 방법은 카다놀의 불포화 탄화수소 사슬을 개질하여 폴리올을 합성하는 방법이다. 이 방법은 일반적으로 불포화 탄화수소 사슬의 에폭시화 반응을 통해 진행된다. 우선, 포름산, 과산화수소, 메타-클로로퍼 옥시 벤조산 등과 같은 물질을 이용한 에폭시화(epoxidation) 반응을 통해 카다놀의 불포화 탄화수소 사슬을 에폭시로 변환시킨다. 이렇게 에폭시화 반응을 통해 얻어지는 에폭시 카다놀의 개환(ring-opening)반응을 통해 폴리올을 합성한다.10-12 그러나, 우리는 이전 연구에서 카다놀 기반 바이오 폴리우레탄 제조시 카다놀에 포함되어 있는 불포화 탄화수소 사슬이 폴리우레탄의 항균성에 중요한 영향을 미치는 것을 확인하였다.10 카다놀을 개질할 때 제조되는 분자 구조에 따라 항균성이 상이하게 나타나기 때문에 위와 같이 불포화 탄화수소 사슬을 개질하는 방법으로 얻은 폴리올을 이용하여 제조된 바이오 폴리우레탄은 항균성을 지니지 못할 것으로 예상된다. 카다놀을 이용하여 폴리올을 제조하는 두번째 방법은 카다놀의 페놀기를 개질하는 방법이다. 이 방법 역시 불포화 탄화수소 사슬을 개질하는 방법과 비슷하게 일반적으로 두 단계의 합성 과정을 통해서 진행된다. 우선, 카다놀의 페놀기를 에피클로로히드린, 1,4-다이브로모뷰테인 등과 같은 할로겐 물질이 포함된 물질과의 할로겐화 치환반응을 통해 개질하며10,13,14 이후, 치환된 카다놀과 수산기를 포함하는 분자 구조를 지닌 물질과의 추가 반응을 통해 바이오 폴리올을 제조한다.11,15 이처럼 일반적으로 두 단계 이상으로 진행되는 바이오 폴리올의 합성과정을 한 단계로 간소화한다면, 경제적인 측면에서 폴리우레탄 산업분야에 대한 바이오 폴리올의 적용이 더욱 용이할 것으로 예상된다.
Mannich reaction은 아민기와 포름알데히드를 이용하여 벤젠고리의 친전자성 치환반응을 유도하는 한 단계 개질 방법으로, 일반적인 치환반응과 비교하였을 때 촉매가 사용되지 않는다는 특징을 갖고 있다.16 본 연구에서는 카다놀, 에탄올아민, 포름알데히드를 이용한 Mannich reaction을 통하여, 한단계 반응을 이용한 카다놀 기반 바이오 폴리올(CBP)을 합성하는 것에 성공하였다. CBP는 2개의 수산기를 포함하고 있기 때문에 폴리올로의 적용이 가능하며, CBP와 헥사메틸 디이소시아네이트(HDI)을 이용하여 바이오 폴리우레탄(CBPU)을 제조하였다. 실험의 대조군으로 사용하기 위해 석유계 폴리올로 많이 사용되는 폴리에틸렌글리콜(PEG)을17 이용하여 석유계 폴리우레탄(PEGU)을 제조하였다. 이를 바탕으로 본 연구에서는 CBPU의 열적, 기계적, 화학적 특성과 항균성을 석유계 폴리우레탄과 비교 및 고찰하였다.
재료. 본 연구에서 사용한 카다놀은 Biochempia(Korea)사에서 원료를 제공받아 사용하였으며, CBP 합성에 사용되는 37% 포름알데히드 수용액, 에탄올아민 그리고 CBPU 제조에 사용되는 디부틸주석 디라우레이트(DBTDL), 헥사메틸렌 디이소시아네이트(HDI) 은 Sigma Aldrich(Korea)사에서 구매하였다. 대조군을 제조하기 위한 폴리에틸렌글리콜(PEG Mn=400, for synthesis), 용매로 사용한 tetrahydrofuran(THF), acetonitrile, ethyl acetate(EA), dichloromethane(MC)는 대정화금(주)에서 구매하였다. 항균성 측정을 위한 Escherichia coli(E. coli, ATCC 8739)는 American Type Culture Collection (ATCC) (Korea)에서 구매하였다. 모든 원료는 별도의 처리없이 사용하였다.
카다놀 기반 바이오 폴리올(CBP) 합성.카다놀 기반 바이오 폴리올인 CBP를 합성하기 위해 카다놀(30.2 g, 0.1 mol), 37% 포름알데히드 수용액(8.1 g, 0.1 mol) 그리고 에탄올아민(6.1 g, 0.1 mol)을 둥근 바닥 플라스크에 투입하고 80 oC에서 환류 상태로 1시간 동안 교반하였다. 이후 온도를 120 oC까지 승온 하여, 환류 냉각관을 제거하고 30분 동안 교반 하였다. 반응 완료 후, EA, MC 및 염수를 사용하여 1차 정제를 진행하고, acetonitrile을 사용한 침전 방법으로 2차 정제를 진행하였다. 이를 통해 초기 카다놀의 무게 대비 48.7%의 수율로 액상의 CBP를 얻었다.
CBP 기반의 바이오 폴리우레탄(CBPU) 제조.CBP 기반의 바이오 폴리우레탄(CBPU)은 다음과 같은 방법으로 제조하였다. THF 25 mL에 용해시킨 CBP 10 g과 DBTDL 0.1 g(1 wt%)을 둥근 바닥 플라스크에 투입한 뒤 상온에서 교반 하였다. 이후 CBP의 hydroxyl value 값을 기반으로 이소시아네이트의 비율을 NCO/OH=1.4로 계산하여 HDI를 천천히 한 방울씩 첨가하여 30분간 교반하였다. 교반이 끝난 후 100 mm ×100 mm×3 mm 테프론 몰드 위에 교반액을 캐스팅하였다. 캐스팅액을 상온에서 24시간 동안 건조한 후, 80 oC의 오븐에서 건조하여 필름 내부에 존재하는 잔여 용매를 완전히 제거하였다. 대조군으로 제조한 PEGU는 석유계 폴리올인 PEG를 사용하여 위와 동일한 방법으로 제조하였다.
CBP 및 CBPU 특성 평가 및 분석. CBP의 분자 구조는 1H NMR(HD 400, Bruker, Germany)을 이용하여 분석하였으며, 분석 용매로는 chloroform-d(CDCl3)를 사용하였다. 푸리에 변환 적외선(FTIR) 분광기 분석(ALPHA-P, Bruker, Germany)은 ATR 모드에서 500-4000 cm-1 분자 결합의 변화를 통해 CBP의 합성 및 CBPU의 제조를 확인하였다.
CBP의 hydroxyl value를 측정하기 위해 무수초산-피리딘 방법을18 사용하였다. Hydroxyl value는 폴리올 1 g에 존재하는 수산기에 해당하는 KOH의 mg 수로 식 (1)으로 나타낼 수 있다. 폴리올의 당량을 분자량과 수산기로 변환시키면 식 (2)에 나타난 바와 같다. 따라서, 폴리올의 분자량과 수산기의 수를 알고 있으면, 이론상 hydroxyl value를 계산할 수 있다.

CBPU 및 PEGU의 열분해온도는 열 중량 분석기(TGA 4000, PerkinElmer, USA)를 이용하여 분석하였다. TGA 분석은 50 oC부터 600 oC의 온도 범위에서 승온 속도 10 oC/min로 측정하였다.
CBPU와 PEGU의 항균 특성은 Escherichia coli(E. coli, ATCC 8738)에 대한 필름 밀착법(film adhesion method)으로 측정하였다. 세균 현탁액을 제조하기 위해 E. coli를 37 oC에서 18시간 동안 배양하였다. 이후, 백금이를 이용하여 콜로니를 포집하여 30 mL의 영양 배지에 넣고 37 oC에서 18시간 동안 흔들며 배양하였다. 0.9 wt% NaCl 용액으로 2회 세척한 후 0.9 wt% 용액에 재 분산시켜 1×107 CFU/mL를 농도로 산출하였다. CBPU 필름의 살균 활성을 평가하기 위해 필름(2 cm×2 cm)을 세균 현탁액에 침지한 후, 24시간 동안 25 oC의 진탕 배양기에서 200 rpm으로 회전하였다. 용액의 연속 희석 후, 0.1 mL의 1×104 CF 희석액을 한천 배지에 펼쳤다. Spreading Agar 배지를 37 oC에서 18시간 동안 배양하고 살아남은 콜로니 수를 세어 측정하였다. 대조군 샘플로써 PEGU 필름에서 생존한 콜로니의 수를 측정하였다. 항균 활성은 식 (3)을 통해 계산하였다.
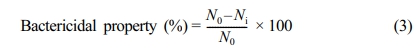
N0: Bacterial CFU of blank
N1: Bacterial CFU of tested sample
기계적 특성을 측정하기 위해 상온에서 cross-head 속도 50 mm/min으로 만능시험기(QM100S, Qmesys, Korea)를 통해 측정하였다. 측정 필름의 크기는 15 mm×10 mm로 동일한 아령형으로 진행하였다. 내화학성을 평가하기 위해 20 mm ×20 mm×10 mm의 샘플을 준비하였다. 준비한 샘플을 pH 2 용액과 pH 10 용액에 각각 24시간 동안 침지하였다. 24시간 뒤 시료를 닦고, 2일간 건조한 후 무게 변화를 측정하였다. 총 3번의 시험을 통해 평균값을 도출하였으며, 중량 감소 실험은 식 (4)를 통해 계산하였다.
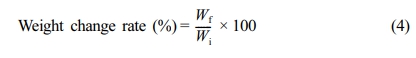
Wi: The weight of the initial sample (g)
Wf: The weight of the final sample (g)
CBP와 CBPU의 제조 및 분석. 본 연구에서 사용한 CBP 및 CBPU의 합성 과정은 Scheme 1에 도식하였다. 수산기를 포함하는 페날카민 유도체인 CBP는 별도의 용매와 촉매를 사용하지 않고 카다놀, 에탄올아민, 포름알데히드를 이용한 Mannich reaction을 통해 하나의 반응기 내에서 합성되었다. CBP의 합성은 1차 아민 물질인 에탄올아민과 포름알데히드가 빠른 속도로 반응하여 포름알데히드-아민 유도체가 형성되며 시작되었을 것이다.19 이후 생성된 포름알데히드-아민 유도체는 잔여하는 카다놀과 상대적으로 느린 반응 속도로 반응하여 Mannich bridge가 형성되는 과정을 통해 CBP의 합성이 완료되었을 것으로 예상된다. 이 과정에서 미반응 포름알데히드와 에탄올아민은 CBP의 부반응을 빠르게 진행시킨다.20,21 따라서, 이러한 부반응을 억제하기 위해 CBP 합성을 위한 Mannich reaction 진행시 카다놀, 포름알데히드, 에탄올아민은 각각 1:1:1의 몰 비율을 사용하였다.
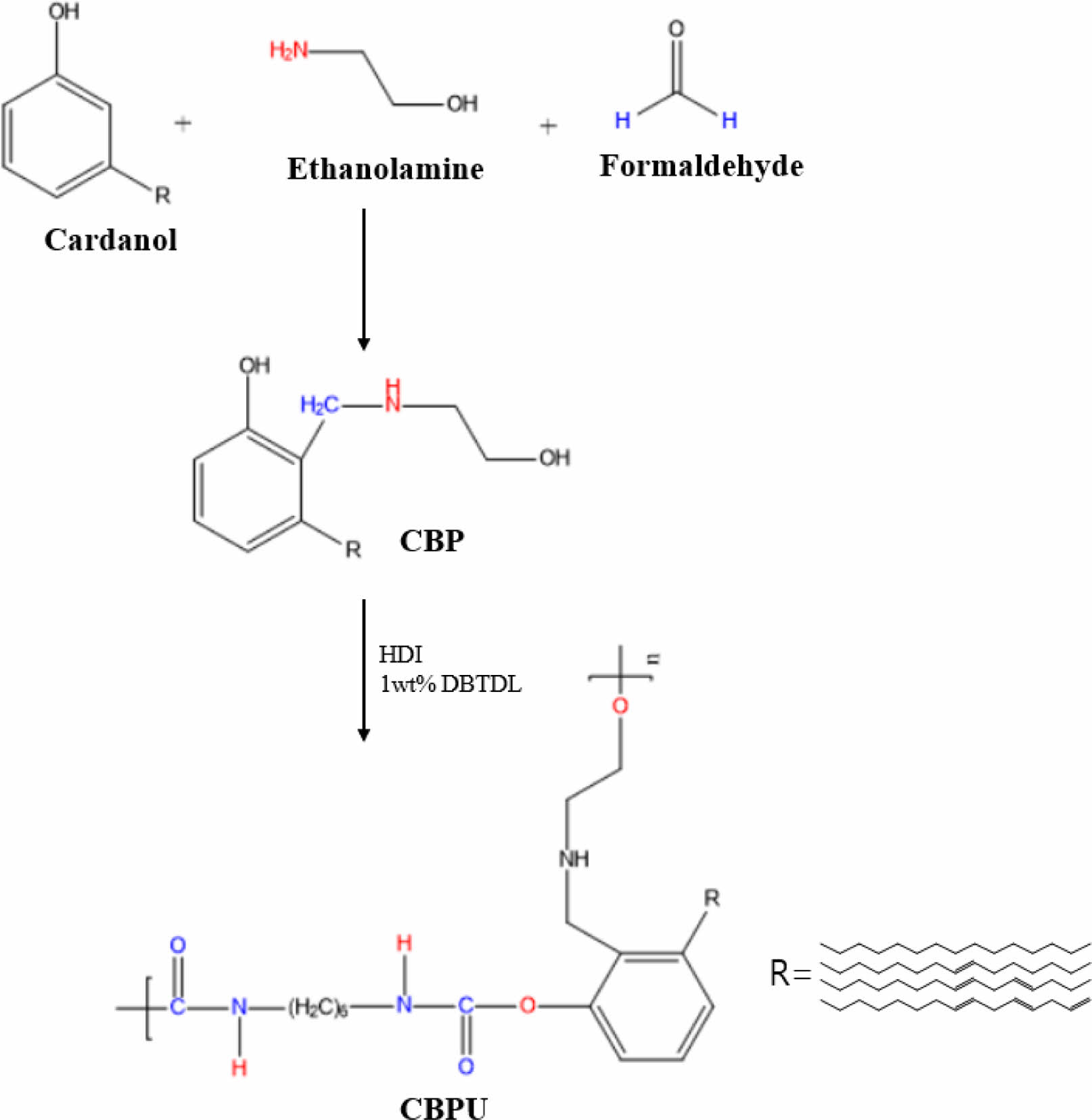
Scheme 1. Schematic diagram of synthetic procedure for CBP and CBPU.
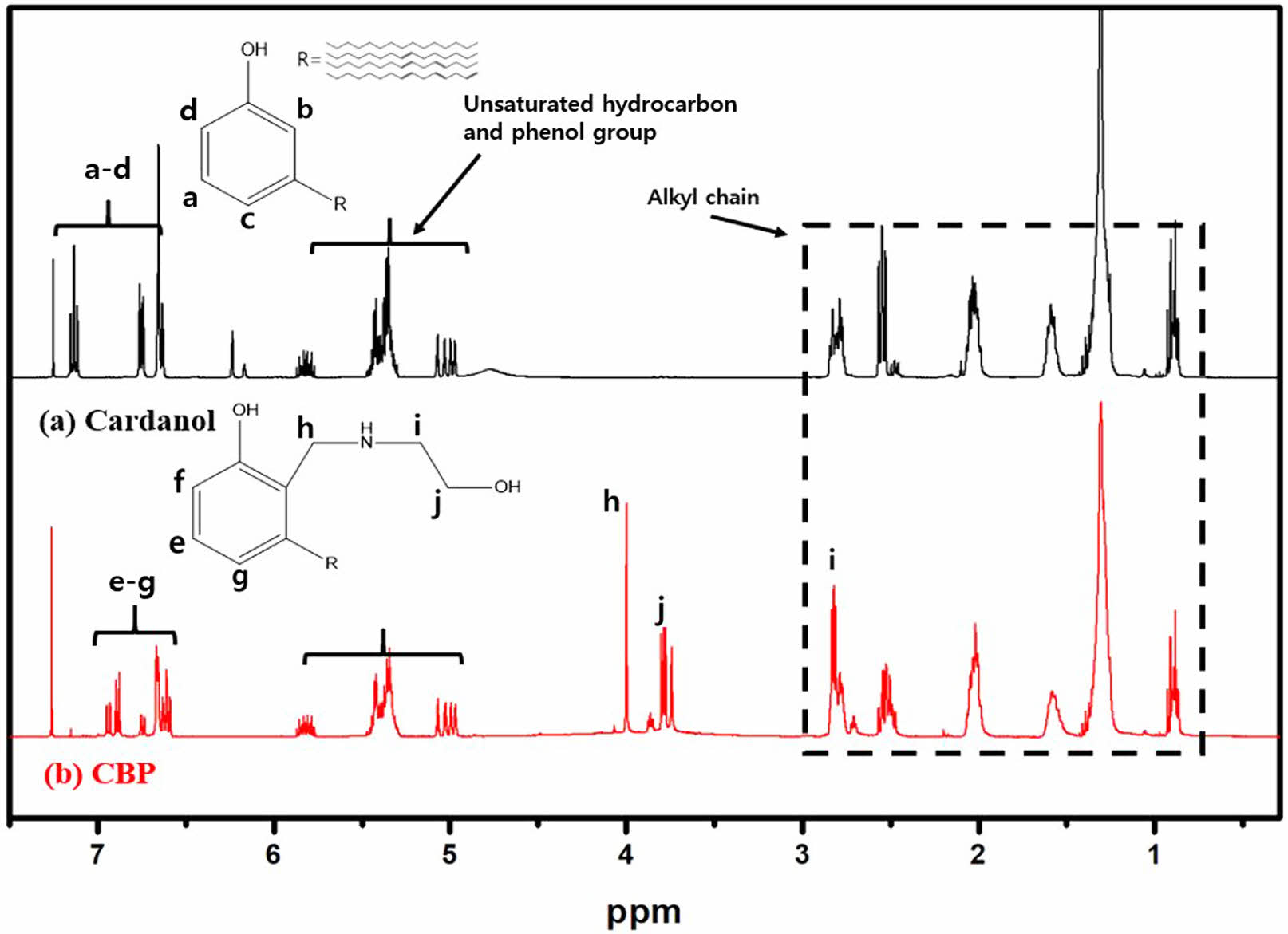
정제 후 얻어진 CBP의 화학적 구조는 1H NMR과 FTIR 분석을 통해 확인하였다. Figure 1(a)의 1H NMR을 통한 분석 결과 카다놀의 방향족 고리의 수소에 대한 특성 피크가 6.5-7.2 ppm에서 관찰되며, 5.3-5.6 ppm에서 불포화 탄화수소 사슬 및 페놀기의 피크를 확인하였다. 또한, 0.7-3.0 ppm에서 카다놀의 불포화 탄화수소 사슬의 피크를 확인하였다.21,22 CBP의 경우 2.5 및 3.5 ppm에서 나타나는 에탄올 아민의 특징 피크가 반응 후, 전자 밀도 감소에 의한 화학적 이동이 발생하여 각각 2.8 및 3.8 ppm에서 확인되었다(Figure 1(b)). 추가적으로 Mannich bridge(Ar-CH2-NH)에 해당하는 피크는 4.0 ppm에서16 관찰되며, 위의 분석을 통해 CBP가 성공적으로 합성되었음을 확인하였다.
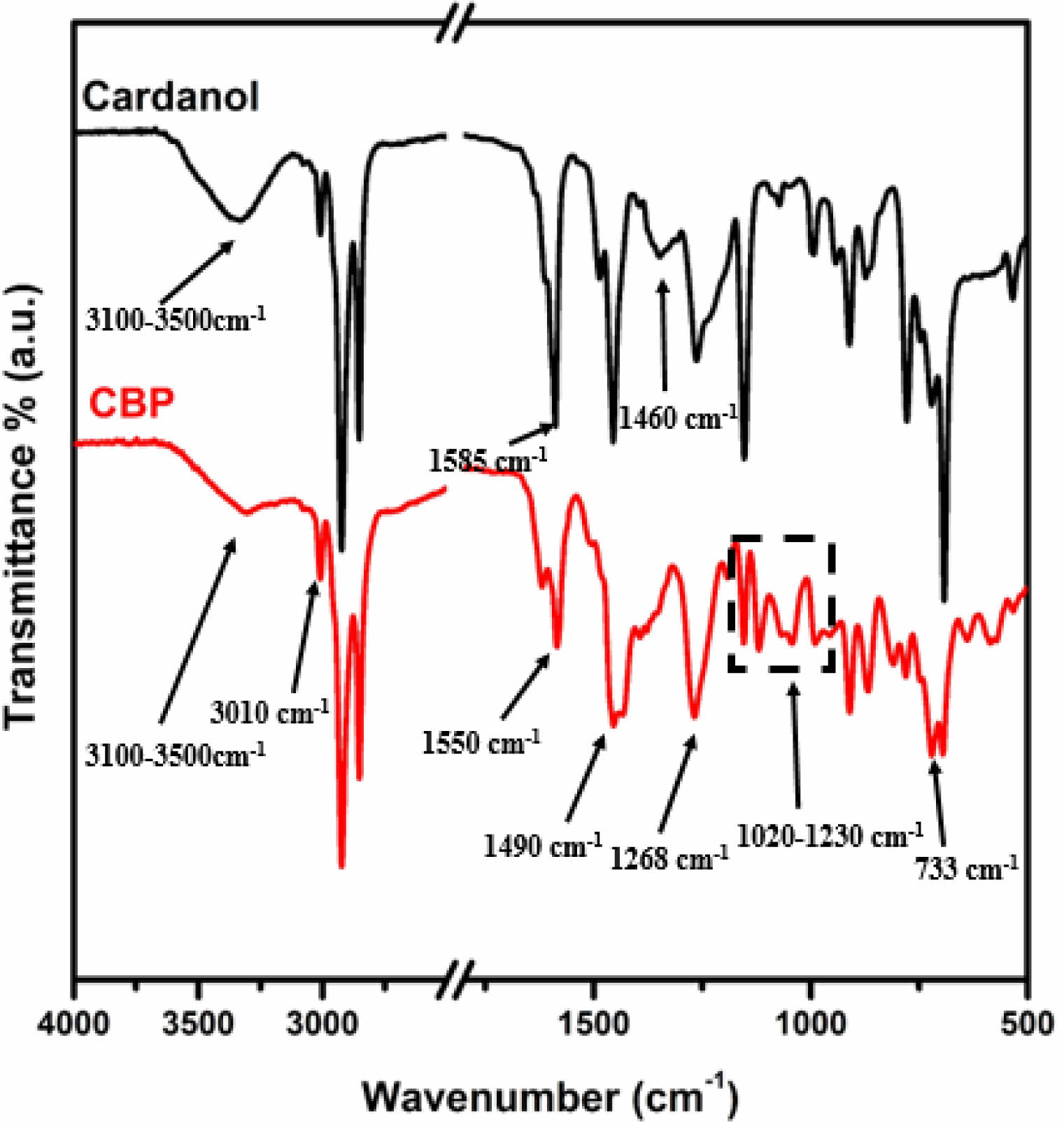
CBP의 화학적 구조는 FTIR 분석을 통해 추가적으로 확인하였다(Figure 2). 카다놀 페놀기의 -OH에 해당하는 피크는 3100-3500 cm-1에서, 페놀기의 C-O stretching에 해당하는 피크는 1268 cm-1에서 각각 관찰되었으며, 불포화 탄화수소 사슬의 -C=CH stretching에 해당하는 피크는 3010 cm-1에서 확인되었다. 이외에 페놀기에 포함된 방향족 C=C 이중결합에 해당하는 피크는 1585 cm-1, 1460 cm-1, 1490 cm-1에서 확인되었다.10,20 카다놀과 마찬가지로, CBP의 불포화 탄화수소 사슬의 -C=CH stretching과 방향족 이중결합이 각각 3010 cm-1와 1490 cm-1에서 확인되었으며, C-O stretching에 해당하는 피크는 1268 cm-1에서 관찰되었다. 이는 Mannich reaction에서 카다놀의 불포화 탄화수소 사슬의 이중결합과 페놀기는 개질되지 않았음을 의미하였다. 또한, Mannich bridge에 해당하는 N-H wagging 피크는 733 cm-1 및 1550 cm-1에서, C-N stretching 피크는 1020-1230 cm-1에서 각각 확인되었다.
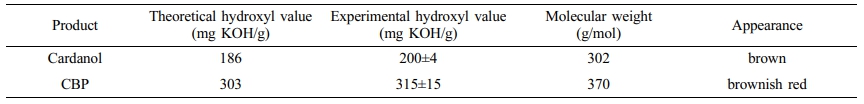
CBPU를 제조하기 위해 카다놀 및 CBP의 이론상 hydroxyl value를 식 (2)를 이용하여 계산하였고, 무수초산-피리딘 방법을 통해 hydroxyl value의 실험값을 측정하였다(Table 1). 카다놀의 평균 분자량은 302 g/mol이며 한 개의 수산기를 갖고 있으므로, 계산을 통해 얻은 이론상 hydroxyl value는 186 mg KOH/g이다. 마찬가지로 CBP의 분자량은 370 g/mol이며 두개의 수산기를 갖고 있으므로, 같은 계산으로 얻은 이론상 hydroxyl value는 303 mg KOH/g이다. 무수초산-피리딘 방법으로 측정에서 얻은 카다놀과 CBP의 hydroxyl value 실험값은 각각 200±4 mg KOH/g와 315±15 mg KOH/g로 실험적 오류를 고려하면 CBP가 이전 1H NMR 및 FTIR 분석을 통해 확인된 화학적 구조를 가지고 있음을 다시 한번 확인할 수 있었다. CBPU는 실험에서 얻은 CBP의 hydroxyl value를 기반으로 필름 형태로 제조하였다. 먼저, NCO/OH의 비율이 1인 조건하에서 폴리우레탄 필름을 제조하였을 경우, 균일한 독립형 필름(free-standing film)을 얻지 못했다. 이는 이미 보고된 결과와 일치하는 것으로, 일반적으로 NCO/OH의 비율이 1의 조건하에서 분자량이 500 g/mol 이하인 폴리올을 이용하여 폴리우레탄 필름을 제조할 경우 균일한 독립형 필름이 형성되지 않는 것으로 알려져 있다.10,23 따라서, 폴리우레탄 필름 제조시 알로파네이트와 뷰렛 반응을 통한 가교 네트워크를 형성을 유도하기 위해 NCO/OH의 비율을 조절하여 실험을 진행한 결과, NCO/OH의 비율을 1.4로 하였을 경우 균일한 독립 형태의 필름을 얻을 수 있는 것을 확인하였다.15 또한, CBPU의 필름 제조시 CBP와 HDI를 혼합 후 DBTDL 촉매를 첨가하였을 경우 우레탄 반응의 높은 반응속도로 인해 형성된 필름의 내부에 기포가 형성되는 것을 확인할 수 있었다. 이에 CBP와 DBTDL 촉매를 우선 혼합하여 CBP와 DBTDL 사이의 중간체 형성을 유도한 후, HDI를 첨가하는 방법으로 폴리우레탄 반응을 진행하였다. 이와 같은 폴리우레탄 반응속도의 상대적인 조절을 통해 필름 내부의 기포 생성을 제어하여 균일한 형태의 독립 필름을 얻을 수 있었다.24 대조군인 PEGU는 PEG의 hydroxyl value를 기준으로 CBPU와 동일 조건인 NCO/OH=1.4의 비율을 사용하여 독립형 필름을 제조하였다.
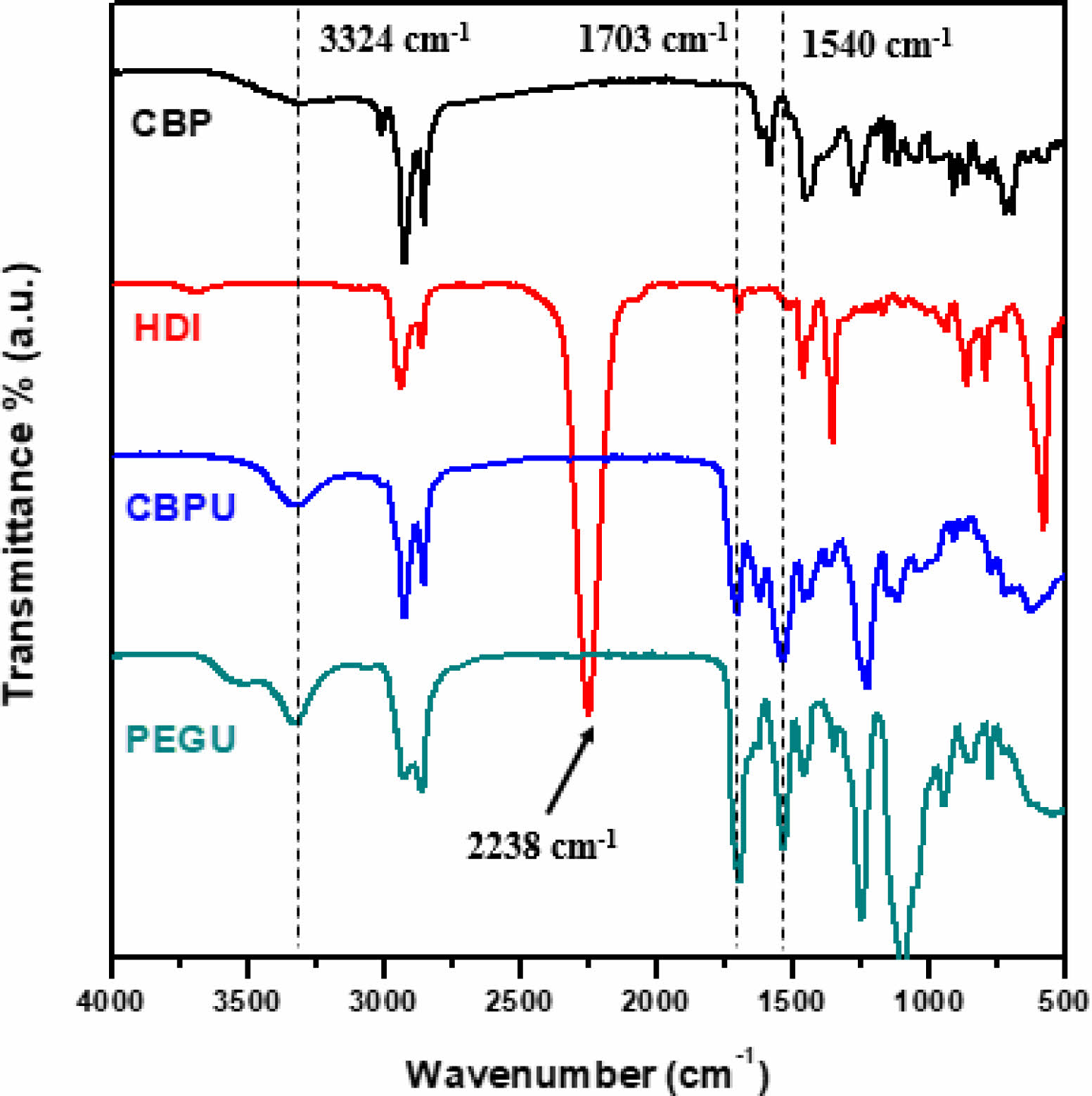
CBPU와 PEGU의 제조는 Figure 3의 FTIR 분석을 통해 확인하였다. CBPU와 PEGU의 FTIR 결과로부터, HDI의 N=C=O 결합을 나타내는 2238 cm-1 피크가 완전히 사라지는 것을 확인할 수 있다. 본 연구에서 과량의 이소시아네이트를 사용한 점을 고려하였을 때, 이는 우레탄 반응과 더불어 알로파네이트 및 뷰렛 형성 반응을 포함하는 부반응이 동시에 진행되었음을 알 수 있다.15 또한, CBPU와 PEGU의 FTIR 결과에서는 우레탄 결합의 형성을 나타내는 N-H stretching과 N-H bending 피크가 각각 3324 cm-1 및 1540 cm-1에서 관찰되었고, C=O stretching 피크가 1703 cm-1에서 관찰되었다. 따라서, CBPU 및 PEGU는 HDI와 CBP 및 PEG 사이의 각각에 대한 우레탄 반응을 통하여 성공적으로 제조되었음을 확인할 수 있었다.
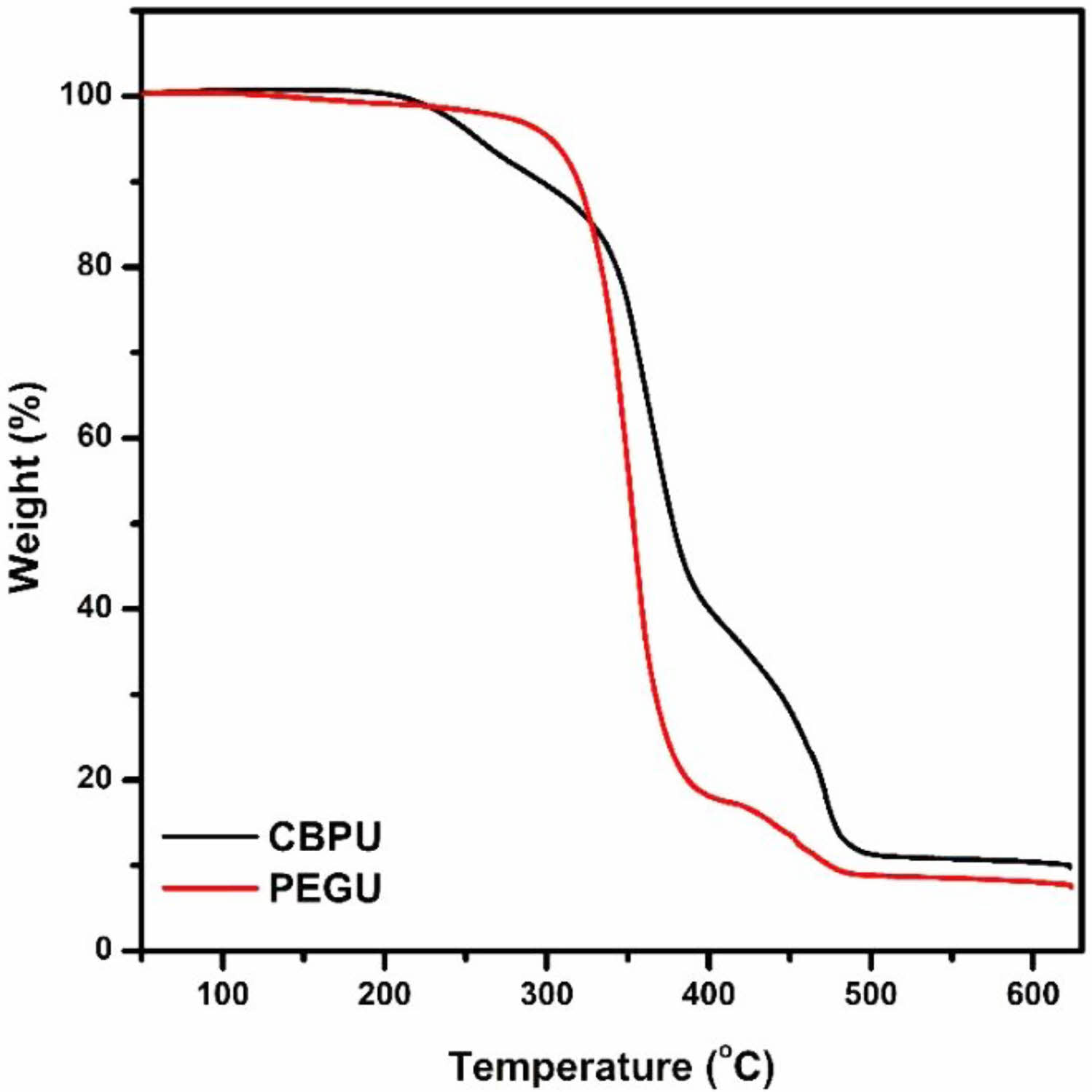
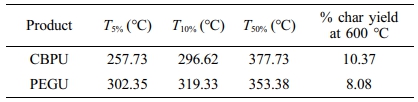
CBPU의 열적 특성.CBPU 및 PEGU의 열 안정성을 평가하기 위하여 열 중량 분석기를(TGA)를 이용하여 50 oC에서 600 oC까지의 열분석을 진행하였다. Figure 4와 Table 2는 CBPU와 PEGU의 TGA 결과를 보여준다. 일반적으로 바이오 유래 폴리우레탄의 경우 열적 안정성 및 물리적 안정성이 낮은 것으로 알려져 있지만, CBPU는 방향족 고리화합물을 포함하고 있는 폴리올인 CBP를 사용하여 제조하였기 때문에 상대적으로 높은 열적 안정성을 나타내고 있는 것으로 판단된다.25 Figure 4에서 확인할 수 있듯이 PEGU는 2단계의 분해 거동을 보였으며, CBPU는 3단계의 분해 거동을 나타내었다. PEGU의 T5%는 302.75 oC이며 CBPU의 T5%는 257.73 oC로 초기 열분해는 CBPU가 PEGU에 비해 상대적으로 더 낮은 온도에서 진행된다.
폴리우레탄의 열적 안정성은 폴리우레탄을 구성하고 있는 폴리올과 이소시아네이트의 화학적 구조이외에 우레탄 반응시에 적용된 NCO/OH의 비율에도 영향을 받는 것으로 알려져 있다. 즉, NCO/OH의 비율이 증가할수록 우레탄 반응의 부반응으로 인한 알로파네이트와 뷰렛 구조가 형성되어 열적 안정성이 증가한다.26 본 연구에서는 CBPU와 PEGU 모두 동일한 이소시아네이트와 NCO/OH의 비율로 제조하였기 때문에 CBPU의 초기 분해온도가 PEGU 보다 더 낮은 이유는 CBP와 PEG가 지닌 폴리올의 구조에 따른 차이로 판단된다. 우레탄 결합의 분해는 우레탄 결합을 구성하고 있는 분자 구조에 따른 결합력의 차이에 따라 일반적으로 약 200-400 oC에서 발생한다.27 예를 들어, 페놀-지방족 이소시아네이트 사이의 우레탄 결합은 지방족 수산기-지방족 이소시아네이트로 이루어진 우레탄 결합에 비해 상대적으로 약한 결합력으로 인해, 약 250 oC에서 분해가 진행되는 지방족 수산기-지방족 이소시아네이트의 우레탄 결합에 비해 낮은 온도인 180 oC 부근에서 분해가 시작되는 것으로 보고되어 있다.15,27 PEGU의 경우 지방족 수산기-지방족 이소시아네이트로 구성된 우레탄 결합만을 포함하지만, CBPU는 CBP의 화학적 구조를 고려하였을 경우, 지방족 수산기-지방족 이소시아네이트로 구성된 우레탄 결합과 페놀-지방족 이소시아네이트로 구성된 우레탄 결합을 모두 포함하고 있음을 알 수 있다. 따라서, 180 oC에서 확인되는 CBPU의 첫번째 분해는 CBP의 페놀기와 지방족 이소시아네이트 사이의 우레탄 결합의 분해이며, CBPU와 PEGU의 지방족 수산기-지방족 이소시아네이트의 우레탄 결합의 분해는 250-350 oC에서 시작되는 것으로 판단된다. 400-500 oC에서 진행되는 마지막 분해 단계는 고분자 사슬의 라디칼 분해이다.27 열분해 거동 분석 결과 CBPU와 PEGU의 T50%는 각각 377.73 oC와 353.38 oC이였으며, char yield는 각각 10.37%와 8.08%로 CBPU가 PEGU에 비해 상대적으로 더 많은 양의 char를 생성하는 것으로 확인되었다. 이는 CBPU가 분자구조에 열적으로 안정한 방향족 고리화합물을 포함하고 있기 때문일 것으로 설명할 수 있다.10
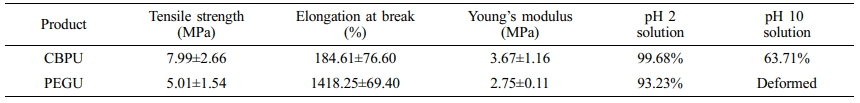
CBPU의 벌크 특성. 기존 연구를 통해 고분자 재료에 방향족 고리화합물과 소수성을 나타내는 불포화 탄화수소 사슬을 포함하고 있는 개질된 카다놀이 도입되었을 경우 재료 고유의 기계적 강도와 내화학성이 향상된다는 것이 이미 알려져 있다.28 본 연구에서도 CBP의 도입에 따른 폴리우레탄 필름의 내화학성 향상을 확인하기 위해 내산 및 내염기성 측정실험을 진행하였다. 이를 위해 20 mm×20 mm×10 mm의 CBPU 및 PEGU 필름 샘플을 각각 준비하였다. 각 샘플을 내산 측정을 위한 pH 2 용액과 내염기성 측정을 위한 pH 10의 각 용액에 24시간 동안 침지한 후 2일 동안 건조하였다. 이때 중량 감소율(%)을 관찰하였으며 그 결과를 Table 3에 나타내었다. 이전 연구에서 폴리우레탄 필름은 산성 수용액에서는 우수한 내구성을 나타내지만, 염기성 수용액에서는 상대적으로 약한 내구성을 지닌 것으로 보고된 바 있다.29 본 연구에서도 산성 수용액(pH 2)에서 PEGU와 CBPU의 두 시료는 각각 93.23% 와 99.68%의 중량을 유지하며 우수한 내산성을 나타냈다. CBPU가 PEGU에 비해 상대적으로 더 우수한 내산성을 나타낸 것은 CBP와 PEG 분자의 화학적 구조차이에 의한 것으로 설명할 수 있다. 친수성이며 선형구조를 가지고 있는 PEG를30 이용하여 제조한 PEGU는 폴리우레탄 내부로 산성 수용액이 침투되는 것이 상대적으로 용이하다. 그러나, 소수성 불포화 탄화수소 사슬을 지니며 분자 구조 내의 방향족 고리화합물을 포함하고 있는 CBP를 이용하여 제조된 CBPU의 경우 산성 수용액이 폴리우레탄 내부로의 침투되는 것을 효과적으로 차단할 수 있기 때문에 상대적으로 높은 내산성을 나타내는 것으로 판단된다.31 또한, 내산성에 비해 CBPU와 PEGU의 낮은 내염기성은 염기조건하에서 폴리우레탄 결합이 갖고 있는 고유의 가수분해에 따른 영향으로 판단된다.32 염기성 수용액(pH 10)에서 PEGU는 완전히 용해되었지만, CBPU는 초기 중량 대비 36.29%의 중량 감소가 발생하였다. 이는 산성 수용액의 결과와 마찬가지로 염기성 수용액에서도 CBP 분자 구조의 영향으로 PEGU에 비해 CBPU가 상대적으로 높은 내염기성을 나타난 것이다. 또한, PEGU의 경우 폴리올로 사용된 PEG는 주사슬이 염기조건하에서 가수분해가 용이한 폴리에테르로 구성되어 있기 때문에 내염기성이 전혀 관찰되지 않은 것으로 판단된다.33 위 결과를 바탕으로 카다놀을 기반으로 제조된 CBPU는 석유계 폴리우레탄 PEGU와 비교하여 산성 및 염기성 수용액 모두에서 내화학성이 향상되는 것을 확인하였다.
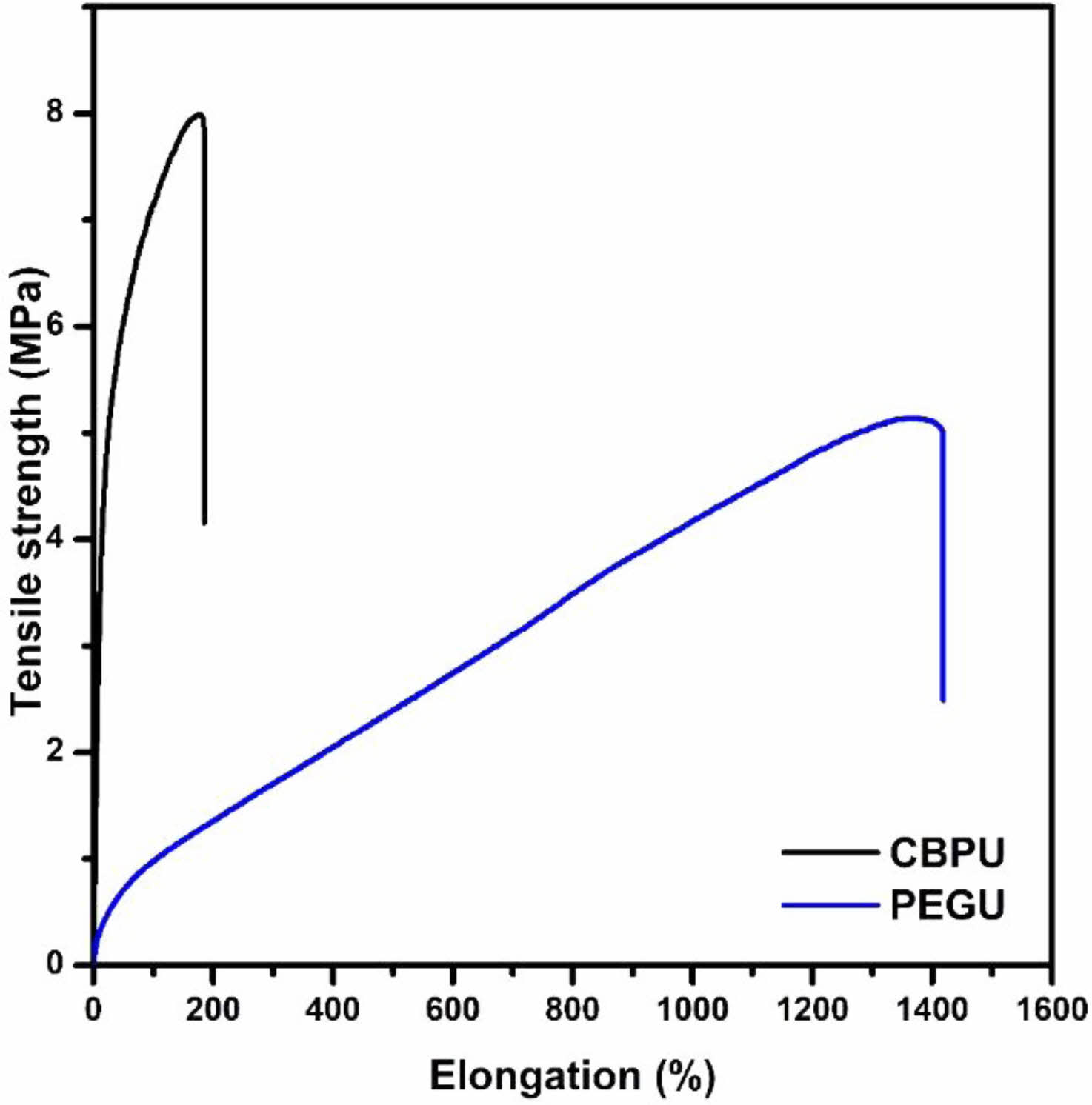
폴리우레탄의 기계적 물성은 hard segment와 soft segment의 조성비에 크게 영향을 받으며, NCO/OH의 비율에 따른 가교 네트워크 등에 따라서 민감하게 변화한다. Table 3과 Figure 5은 CBPU와 PEGU 필름 시편에 대한 인장강도 시험 결과를 보여준다. 일반적으로 석유계 폴리우레탄에 비해 바이오 폴리우레탄이 실생활에 직접적으로 적용되기 어려운 이유중의 하나는 2-4 MPa 정도에서 나타나는 바이오 폴리우레탄의 상대적으로 낮은 인장강도이다.34,35 반면, 본 연구에서 사용된 CBPU의 인장강도는 석유계 PEGU의 인장강도 5.01± 1.54 MPa에 비해 약 1.4배 높은 7.99±2.66 MPa로 나타났으며 이는 다음과 같은 폴리우레탄 사슬내의 soft segment와 hard segment의 함량 차이에 의한 것으로 설명할 수 있다. 폴리우레탄의 soft segment는 폴리에스테르, 폴리에테르 등의 긴 선형 사슬 고분자를 뜻하고 hard segment는 극성이 강하고 견고한 우레탄기, 우레아, 방향족 고리화합물을 의미하며 각 segment의 조성비에 따라 물성의 80%까지 조절된다.36 PEGU의 폴리올로 사용된 PEG는 분자 구조의 주사슬이 사슬 연장재 역할을 하는 에테르 결합으로 구성 되어있으며, 폴리우레탄의 soft segment에 해당된다. 반면, CBPU의 폴리올로 사용된 CBP는 분자 구조 내부에 hard segment인 방향족 고리화합물을 포함하고 있으며 선형 폴리올인 PEG와는 차별적으로 2차원 평면 구조를 가진다. CBP의 평면 구조는 폴리우레탄 사슬에 강직성을 띄게 해주어 hard segment의 역할을 하게 된다. 따라서 CBPU는 폴리우레탄 사슬 내 hard segment의 함량이 PEGU에 비해 상대적으로 높기 때문에 CBPU의 인장강도가 향상되었다고 판단된다.37 또한, 카다놀을 개질하여 고분자 재료에 적용하였을 때, 카다놀 분자 구조의 불포화 탄화수소 사슬 사이의 얽힘 현상이 보고된 바 있다.38 일반적으로 고분자 사슬의 얽힘 현상은 인장강도를 증가시키는 요인이 된다.39 PEGU는 곁사슬이 없는 선형 고분자로 구성되어 있는 반면, CBPU는 분자 구조에 불포화 탄화수소 곁사슬을 포함하고 있다. 따라서 CBPU의 불포화 탄화수소 곁사슬은 폴리우레탄 사슬과 사슬 사이의 얽힘 현상을 유도할 수 있으며, 이로 인해 CBPU의 인장강도 향상에 영향을 준 것으로 판단된다. 또한, 폴리우레탄이 지닌 탄성계수를 확인하기 위해 Young's modulus를 확인하였다. Young's modulus는 폴리우레탄의 탄성 변형에 대한 저항을 나타내는 값으로 Young's modulus가 증가할수록 변형에 대한 내성이 증가한다. 폴리우레탄의 Young's modulus는 hard segment와 soft segment의 함량에 따라 변화하며, 일반적으로 hard segment의 함량이 증가함에 따라서 Young's modulus는 증가한다.40 본 연구에서 CBPU와 PEGU의 Young's modulus는 각각 3.67±1.16 MPa와 2.75±0.11 MPa로 나타났다. CBPU는 PEGU보다 hard segment 함량이 높기 때문에, CBPU의 Young’s modulus가 더 높게 나타난 것으로 판단된다.
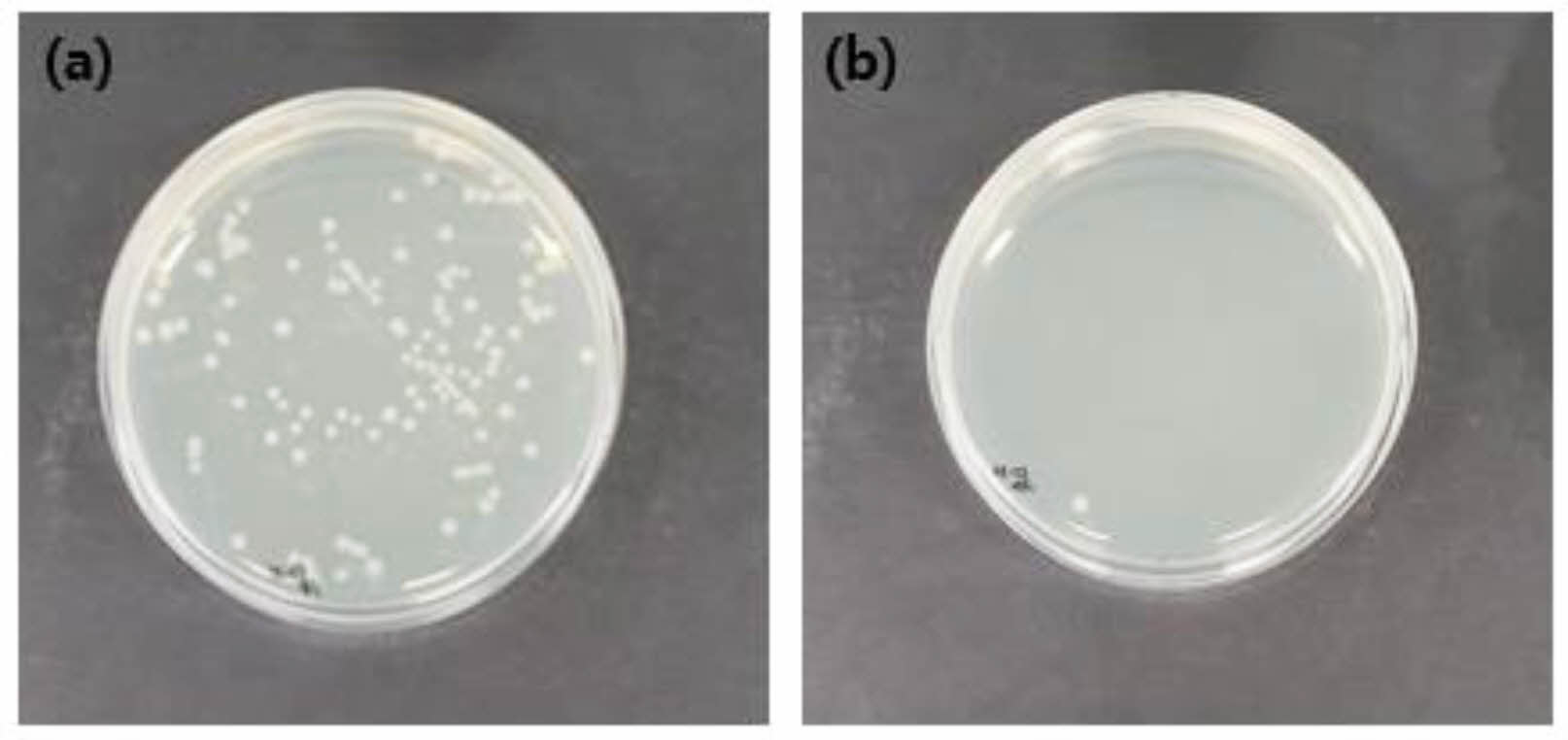
CBPU의 항균 특성.일반적으로 식물이나 과일에서 얻어지는 천연 페놀 화합물은 항균성 및 항산화작용을 지닌 것으로 알려져 있다.41 천연 페놀 화합물인 카다놀의 항균 메커니즘은 정확히 밝혀지지는 않았지만, 개질된 카다놀을 이용하여 제조된 고분자의 우수한 항균성은 이미 여러 연구를 통해서 입증되었다.42,43 또한, 본 연구진은 이전 연구를 통해 카다놀의 페놀기를 개질하여 폴리우레탄에 적용하였을때 카다놀의 항균 특성이 유지되는 것을 확인하였다.9,10 이를 바탕으로 본 연구에서는 필름 부착법을 통해 CBPU와 PEGU의 E. coli에 대한 항균특성을 분석하였다. Figure 6은 PEGU와 CBPU의 항균성 측정 결과를 보여준다. 대조군 PEGU는 E. coli의 감소를 보이지 않았으며, CBPU는 E. coli가 기준 대비 90.1% 감소한 것으로 나타났다. 화학적 구조분석 결과를 통해 CBPU에 사용된 CBP의 경우 카다놀을 Mannich reaction을 통해 개질하는 과정에서 카다놀의 불포화 탄화수소사슬이 변형되지 않고 유지되는 것을 확인하였다. 따라서 본 연구에서 제조된 CBPU의 항균성은 CBP의 메타 위치의 불포화 탄화수소 사슬이 중요한 영향을 미치며, 이는 CBP의 불포화 탄화수소 사슬이 박테리아 세포벽을 구조적으로 파괴하여 항균 특성을 나타내는 것으로 설명할 수 있다.9,10,44
|
Figure 1 1H NMR of (a) Cardanol; (b) CBP. |
|
Figure 2 FTIR spectra of Cardanol and CBP. |
|
Figure 3 FTIR spectra of CBP, HDI, CBPU and PEGU. |
|
Figure 4 TGA curves of CBPU and PEGU. |
|
Figure 5 Stress-strain curves of CBPU and PEGU. |
|
Figure 6 Photography showing the antibacterial test of (a) PEGU; (b) CBPU. |
본 연구에서는 비식용 바이오 매스 원료인 카다놀을 사용하여 바이오 폴리올(CBP)을 합성하였다. 기존의 두 단계 이상의 합성 과정을 통해 제조되는 카다놀 기반 바이오 폴리올과 다르게 CBP는 카다놀, 에탄올아민, 포름알데히드를 사용한 Mannich reaction을 통해 한단계의 합성 과정으로 제조하였다. CBP의 화학적 구조는 1H NMR과 FTIR을 통해 확인하였으며, CBP의 hydroxyl value 실험값인 315±15 mg KOH/g을 기반으로 NCO/OH=1.4의 조건하에서 HDI와 CBP의 우레탄 반응을 통해 바이오 폴리우레탄(CBPU)를 제조하였다. 실험의 대조군으로 사용하기 위해 동일한 NCO/OH 비율로 폴리에틸렌글리콜(PEG)를 사용하여 석유계 폴리우레탄(PEGU)을 제조하였다. CBPU는 CBP 고유의 구조적 특성의 영향으로 E. coli에 대해 90.1%의 균 감소율을 나타냈고 PEGU의 인장강도 5.01±1.54 MPa와 비교하여 CBPU의 인장강도는 7.99±2.66 MPa로 1.4배 증가하였으며 내화학성 또한 향상되었다. 결론적으로 본 연구에서 제조된 CBPU는 간단한 제조방법과 친환경성, 높은 인장강도, 내화학성, 항균성을 기반으로 인테리어, 의료용 폴리우레탄 및 폴리우레탄 산업의 지속 가능성을 지원하기 위한 다양한 응용 분야에 적용될 수 있을 것으로 판단된다.
- 1. Kim, S.; Lee, J.; Han, H. Synthesis of UV Curable, Highly Stretchable, Transparent Poly(urethane-acrylate) Elastomer and Applications Toward Next Generation Technology. Macromol. Res. 2020, 28, 896-902.
-

- 2. Filip, D.; Macocinschi, D.; Tuchilus, C. G.; Zaltariov, M. F.; Varganici, C. D. Synthesis, Characterization of Erythromycin Propionate Core-Based Star Poly(ether urethane)s and Their Antibacterial Properties. Macromol. Res. 2021, 29, 613-624.
-

- 3. Zhang, C.; Wang, H.; Zeng, W.; Zhou, Q. High Biobased Carbon Content Polyurethane Dispersions Synthesized from Fatty Acid-based Isocyanate. Ind. Eng. Chem. Res. 2019, 58, 5195-5201.
-

- 4. Tan, S.; Abraham, T.; Ference, D.; Macosko, C. W. Rigid Polyurethane Foams from a Soybean Oil-based Polyol. Polymer 2011, 52, 2840-2846.
-

- 5. Pawlik, H.; Prociak, A. Influence of Palm Oil-based Polyol on the Properties of Flexible Polyurethane Foams. J. Polym. Environ. 2012, 20, 438-445.
-

- 6. Bresolin, D.; Estrella, A. S.; da Silva, J. R.; Valério, A.; Sayer, C.; de Araújo, P. H.; de Oliveira, D. Synthesis of a Green Polyurethane Foam from a Biopolyol Obtained by Enzymatic Glycerolysis and its Use for Immobilization of Lipase NS-40116. Bioprocess Biosyst. Eng. 2019, 42, 213-222.
-

- 7. Balgude, D.; Sabnis, A. S. CNSL: An Environment Friendly Alternative for the Modern Coating Industry. J. Coat. Technol. Res. 2014, 11, 169-183.
-

- 8. Lomonaco, D.; Santiago, G. M. P.; Ferreira, Y. S.; Arriaga, Â. M. C.; Mazzetto, S. E.; Mele, G.; Vasapollo, G. Study of Technical CNSL and its Main Components as New Green Larvicides. Green Chem. 2009, 11, 31-33.
-

- 9. Choi, Y. S.; Kim, K. H.; Kim, D. G.; Kim, H. J.; Cha, S. H.; Lee, J. C. Synthesis and Characterization of Self-cross-linkable and Bactericidal Methacrylate Polymers Having Renewable Cardanol Moieties for Surface Coating Applications. RSC Adv. 2014, 4, 41195-41203.
-

- 10. Kim, S. H.; Kim, S. B.; Cha, S. H. Preparation and Characterization of Biopolyurethane Film with a Novel Cross-linkable Biopolyol Based on Cardanol. Polymer 2018, 42, 736-746.
-

- 11. Suresh, K. I. Rigid Polyurethane Foams from Cardanol: Synthesis, Structural Characterization, and Evaluation of Polyol and Foam Properties. ACS Sustain. Chem. Eng. 2013, 1, 232-242.
-

- 12. Bo, C.; Hu, L.; Jia, P.; Liang, B.; Zhou, J .; Zhou, Y. Structure and Thermal Properties of Phosphorus-containing Polyol Synthesized from Cardanol. RSC Adv. 2015, 5, 106651-106660.
-

- 13. Suresh, K. I.; Kishanprasad, V. S. Synthesis, Structure, and Properties of Novel Polyols from Cardanol and Developed Polyurethanes. Ind. Eng. Chem. Res. 2005, 44, 4504-4512.
-

- 14. Mishra, V.; Desai, J.; Patel, K. I. (UV/Oxidative) Dual Curing Polyurethane Dispersion from Cardanol Based Polyol: Synthesis and Characterization. Ind. Crops Prod. 2018, 111, 165-178.
-

- 15. Wang, H.; Zhou, Q. Synthesis of Cardanol-based Polyols via Thiol-ene/thiol-epoxy Dual Click-reactions and Thermosetting Polyurethanes Therefrom. ACS Sustain. Chem. Eng. 2018, 6, 12088-12095.
-

- 16. Feng, J.; Zhao, H.; Yue, S.; Liu, S. One-pot Synthesis of Cardanol-derived High-efficiency Antioxidants Based on Intramolecular Synergism. ACS Sustain. Chem. Eng. 2017, 5, 3399-3408.
-

- 17. Chun, B. C.; Cho, T. K.; Chong, M. H.; Chung, Y. C. Structure-property Relationship of Shape Memory Polyurethane Cross-linked by a Polyethyleneglycol Spacer Between Polyurethane Chains. J. Mater. Sci. 2007, 42, 9045.
-

- 18. Cocks, L. V.; Van Rede C. Laboratory Handbook for Oil and Fat Analysts. Laboratory handbook for oil and fat analysts. 1966.
- 19. Zhang, Q.; Yang, P.; Deng, Y.; Zhang, C.; Zhu, R.; Gu, Y. Effect of Phenol on the Synthesis of Benzoxazine. RSC Adv. 2015, 5, 103203-103209.
-

- 20. Kathalewar, M.; Sabnis, A. Effect of Molecular Weight of Phenalkamines on the Curing, Mechanical, Thermal and Anticorrosive Properties of Epoxy Based Coatings. Prog. Org. Coat. 2015, 84, 79-88.
-

- 21. Li, S.; Zou, T.; Feng, L.; Liu, X.; Tao, M. Preparation and Properties of Cardanol‐based Polybenzoxazine/SiO2 Hybrids by Sol‐gel Technique. J. Appl. Polym. Sci. 2013, 128, 4164-4171.
-

- 22. Mythili, C.; Retna, A. M.; Gopalakrishnan, S. Synthesis, Mechanical, Thermal and Chemical Properties of Polyurethanes Based on Cardanol. Bull. Mater. Sci. 2004, 27, 235-241.
-

- 23. Lapprand, A.; Boisson, F.; Delolme, F.; Méchin, F.; Pascault, J. P. Reactivity of Isocyanates with Urethanes: Conditions for Allophanate Formation. Polym. Degrad. Stab. 2005, 90, 363-373.
-

- 24. Niyogi, S.; Sarkar, S.; Adhikari B. Catalytic Activity of DBTDL in Polyurethane Formation. Indian J. Chem. Technol. 2002, 9, 330-333.
- 25. Alam, M.; Ashraf, S.; Ray, A. R.; Ahmad, S. Development of Anticorrosive Poly(ether-urethane) Amide Coatings from Linseed Oil: A Sustainable Resource. J. Polym. Environ. 2010, 18, 208-215.
-

- 26. Dutta, S.; Karak, N. Effect of the NCO/OH Ratio on the Properties of Mesua Ferrea L. seed Oil‐modified Polyurethane Resins. Polym. Int. 2006, 55, 49-56.
-

- 27. Chattopadhyay, D. K.; Webster, D. C. Thermal Stability and Flame Retardancy of Polyurethanes. Prog. Polym. Sci. 2009, 34, 1068-1133.
-

- 28. Aggarwal, L.; Thapliyal, P.; Karade, S. Anticorrosive Properties of the Epoxy-cardanol Resin Based Paints. Prog. Org. Coat. 2007, 59, 76-80.
-

- 29. Desai, S. D.; Patel, J. V.; Sinha, V. K. Polyurethane Adhesive System from Biomaterial-based Polyol for Bonding Wood. Int. J. Adhes. Adhes. 2003, 23, 393-399.
-

- 30. Ma, T. Y.; Hollander, D.; Krugliak, P.; Katz, K. PEG 400, a Hydrophilic Molecular Probe for Measuring Intestinal Permeability. Gastroenterology 1990, 98, 39-46.
-

- 31. Kim, S. H.; Kim, S. W.; Cha, S. H. Synthesis and Characterization of Biopolyol-based Polyurethane Films Derived from Modified Cardanol through Two-step Reaction. Polymer 2016, 40, 1005-1014.
-

- 32. Zafar, F.; Ashraf, S. M.; Ahmad, S. Self-cured Polymers from Non-drying Oil. Indian J. Chem. Technol. 2008, 2, 285-294.
- 33. Elschenbroich, C. Organometallics, Third Completely Revised and Extended Edition. Wiley-VCH, Weinheim J. Am. Chem. Soc. 2006, 128, 12029-12030.
-

- 34. Indumathi, M.; Rajarajeswari, G. Mahua Oil-based Polyurethane/chitosan/nano ZnO Composite Films for Biodegradable Food Packaging Applications. Int. J. Biol. Macromol. 2019, 124, 163-174.
-

- 35. Zhang, C.; Madbouly, S. A.; Kessler, M. R. Biobased Polyurethanes Prepared from Different Vegetable Oils. ACS Appl. Mater. Interfaces 2015, 7, 1226-1233.
-

- 36. Yoo, S. R.; Lee, H. S.; Seo, S. W. Orientation and Phase Separated Structure of Polyurethanes Having Various Chemical Structures. Polymer 1997, 21, 467-479.
- 37. Korley, L. T. J.; Pate, B. D.; Thomas, E. L.; Hammond, P. T. Effect of the Degree of Soft and Hard Segment Ordering on the Morphology and Mechanical Behavior of Semicrystalline Segmented Polyurethanes. Polymer 2006, 47, 3073-3082.
-

- 38. Yin, F.; Chen, Q.; Lin, J.; Deng, Y.; Mao, X. Effect of Different Peroxide Initiators on the Reaction Extrusion of Polypropylene-graft-cardanol and its Compatibilization on PP/PC. J. Polym. Res. 2014, 21, 411.
-

- 39. Kil, H. B.; Yoon, S. H.; Ahn, C. W.; Lee, S. W.; Yun, Y. J. Evaluation of Thermal and Mechanical Properties of High Temperature Resin. Proceedings of the 39th KSPE Fall Conference on Aerospace Engineering Topics, Yeosu-si, Korea, November 22-23, 201.
- 40. Ginzburg, V. V.; Bicerano, J.; Christenson, C. P.; Schrock, A. K.; Patashinski, A. Z. Theoretical Modeling of the Relationship Between Young's Modulus and Formulation Variables for Segmented Polyurethanes. J. Polym. Sci. Part B: Polym. Phys. 2007, 45, 2123-2135.
-

- 41. Xu, Y.; Burton, S.; Kim, C.; Sismour, E. Phenolic Compounds, Antioxidant, and Antibacterial Properties of Pomace Extracts from Four Virginia‐grown Grape Varieties. Food Sci. Nur. 2016, 4, 125-133.
-

- 42. Choi, Y. S.; Kim, N. K.; Kang, H.; Jang, H. K.; Noh, M.; Kim, J.; Shon, D. J.; Kim, B. S.; Lee, J. C. Antibacterial and Bio- compatible ABA-triblock Copolymers Containing Perfluoro- polyether and Plant-based Cardanol for Versatile Coating Applications. RSC Adv. 2017, 7, 38091-38099.
-

- 43. Choi, Y. S.; Kang, H.; Kim, D. G.; Cha, S. H.; Lee, J. C. Mussel-inspired Dopamine-and Plant-based Cardanol-containing Polymer Coatings for Multifunctional Filtration Membranes. ACS Appl. Mater. Interfaces 2014, 6, 21297-21307.
-

- 44. Nguyen, T. K.; Lam, S. J.; Ho, K. K.; Kumar, N.; Qiao, G. G.; Egan, S.; Boyer, C.; Wong, E. H. Rational Design of Single-chain Polymeric Nanoparticles that Kill Planktonic and Biofilm Bacteria. ACS Infect. Dis. 2017, 3, 237-248.
-

- Polymer(Korea) 폴리머
- Frequency : Bimonthly(odd)
ISSN 0379-153X(Print)
ISSN 2234-8077(Online)
Abbr. Polym. Korea - 2023 Impact Factor : 0.4
- Indexed in SCIE
 This Article
This Article
-
2022; 46(1): 13-21
Published online Jan 25, 2022
- 10.7317/pk.2022.46.1.13
- Received on Aug 14, 2021
- Revised on Nov 8, 2021
- Accepted on Nov 8, 2021
 Services
Services
Shared
 Correspondence to
Correspondence to
- Sang-Ho Cha
-
Department of Chemical Engineering, Kyonggi University, 154-42, Gwanggyosan-ro, Yeongtong-gu, Suwon 16227, Korea
- E-mail: sanghocha@kgu.ac.kr
- ORCID:
0000-0001-6066-3859










 Copyright(c) The Polymer Society of Korea. All right reserved.
Copyright(c) The Polymer Society of Korea. All right reserved.