Graphene oxide-g-poly(ε-caprolactone)
(GO-g-PCL) was synthesized and characterized in order to use it as a
nanofiller for enhancing the toughness of poly(vinyl chloride) (PVC). Graphene
oxide (GO) prepared from graphite was reacted with thionyl chloride to obtain
acyl derivative of GO, and then GO-g-PCL was synthesized by grafting
PCLs of three different molecular weights (530, 1250, 2000 g/mol) on it with
various reactant ratios at 50 oC using a grafting-to method.
Graft yield of the GO-g-PCL was obtained by TGA analysis comparing
solvothermal treated GO. When the molar concentration of PCL per g GO was
constant during the synthesis, increasing the MW of PCL reduced the number of
PCL molecules grafted onto GO but increased the maximum graft yield. PVC/GO-g-PCL
composite films were prepared by adding 0.3 wt% of GO-g-PCLs with a
similar graft yield of 5.3-5.5% to PVC and their toughness changes were
analysed. The composite films showed excellent increases in toughness compared
to neat PVC, and the degree of increase was greater when the MW of PCL used for
grafting was smaller.
폴리염화비닐(PVC)의
인성 향상을 위한 나노필러로 사용하기 위해 산화 그래핀-g-폴리(ε-카프로락톤)(GO-g-PCL)을
합성하고 그 특성들을 분석하였다. 이를 위해 흑연으로부터 제조한 산화 그래핀(GO)에 염화티오닐을 반응시켜 염화아실 유도체화 GO를 얻었으며, 여기에 3가지 분자량(530,
1250, 2000 g/mol)의 폴리(ε-카프로락톤)(PCL)의 반응비를 변화시키면서 50 oC에서 grafting-to법으로
반응시켜 GO-g-PCL을 합성하였다. 합성한 GO-g-PCL은 TGA 분석으로부터 용매열 처리 GO와 비교하여 그래프트율을 구하였다. GO 단위무게당 일정한 몰비의 PCL을 반응시킬 때 PCL 디올의 분자량이 클수록 GO에 그래프트되는 PCL의 상대적인 분자 수는 적어지지만 얻을 수
있는 최대 그래프트율은 커졌다. 그래프트율이 5.3~5.5%로
비슷한 GO-g-PCL을 PVC에 0.3 wt%로 첨가한 PVC/GO-g-PCL 복합체
필름을 제조하고 이들의 인성 변화를 분석하였다. 복합체 필름은 순수
PVC에 비해 매우 큰 인성 증가를 나타내었으며, 그래프팅 시 사용한 PCL의 분자량이 작을수록 증가정도가 커졌다.
Graphene oxide-g-poly(ε-caprolactone)
(GO-g-PCL) was synthesized and characterized in order to use it as a
nanofiller for poly(vinyl chloride) (PVC). Graphene oxide (GO) was reacted with
thionyl chloride to obtain acyl derivative of GO, and then GO-g-PCL was
synthesized by grafting PCL diol on it using
a grafting-to method. PVC/GO-g-PCL composite film showed excellent increase in toughness compared to
neat PVC.
Keywords: graphene oxide, poly(ε-caprolactone), grafting, graphene oxide-g-poly(ε-caprolactone), toughness of poly (vinyl chloride)
고분자 복합체는 매트릭스인
고분자의 기계적 성질을 개선하거나 열적, 전기적 성질 등의 기능성 부여 또는 재료 비용을 낮추기 위해 필러를 첨가하여 제조한다.1
전통적으로 매트릭스 고분자에 첨가하는 필러로는 유리 섬유, 탄소 섬유, 금속 입자 및 광물 입자 등 섬유, 시트 및 입자 형태의 물질이 대부분이었으며,
이러한 필러를 사용한 고분자 복합체는 고분자 매트릭스와 필러와의 상이한 성질로 인해 계면결합력이 부족하여 충분한 기계적 성질의 향상을 얻을 수
없고 경우에 따라 제조 비용이 증가하는 등의 문제점이 있다.
그러나 최근에는 탄소나노튜브(CNT)와
그래핀(graphene)과 같은 나노소재를 고분자에 필러로 첨가하여 제조한 나노복합체가 등장하게 되었다. 이러한 나노복합체는 사용하는 나노필러의
첨가량이 매우 소량이므로 고분자 매트릭스와 필러 사이의 물리적 성질 차이로 인한 문제점이 적고, 큰 표면적을 가지므로 계면접촉을 크게 할 수 있어
계면강도가 증가하여 기계적 성질을 크게 향상시킬 수 있게 되었다.2 CNT는 내부 공간에 고분자가 접근할 수 없지만 그래핀은
양쪽 면이 모두 고분자 사슬과의 접촉이 가능하므로 고분자와 상호작용할 수 있는 표면적이 상대적으로 더 큰 장점이 있다.3 한편,
그래핀과 같은 평면 형태의 탄소 구조체에 카복시기, 히드록시기, 에폭시기 등의 산소함유 관능기가 다수 결합된 산화 그래핀(GO)은 그래핀보다는
낮지만 여전히 높은 기계적 강도를 나타내며, 산화에 의해 sp2 구조가 sp3 구조로 바뀌면서 방향족 성질이
감소하고 물리적 및 화학적 처리 과정에서 탄소 구조의 결함이 발생하여 전기적인 성질을 잃게 된다.4 그러나 GO는 산소함유
관능기를 가지고 있고 자기들끼리의 반데르발스 상호작용이 적어 물이나 용매에 대한 분산성이 좋으며, 폴리염화비닐(PVC)과 같은 극성 고분자와 혼합하면 고분자와의 상호작용이 커 나노복합체 형성이 용이하다.5
범용 고분자 중 하나인
PVC는 재질이 딱딱하고 신도가 작으며 인성이 약해 잘 깨지기 쉽다. 이러한 단점을 개선하기 위해 GO를 나노필러로 하여 PVC와 혼합한 복합체를
제조하면 어느 정도의 인성 향상 효과를 얻을 수 있다.6 한편, 폴리(ε-카프로락톤)(PCL)은 메틸렌기와 카르보닐기의
비율이 5:1로, 카보닐기가
PVC의 a-수소와 최적의 상호작용을 형성할 수 있어 PVC와의 상용성이
좋은 것으로 알려져 있다.7,8 또한 PCL은 유리전이온도가
낮고 유연한 분자사슬을 가지고 있어, PVC에 첨가 시 가소화 효과를 나타내며 일반 가소제를 첨가할 경우보다 신도 및 인성 향상 효과가 크다.9 따라서 GO에
PCL을 그래프팅시켜 기능화하고 이를 PVC의 나노필러로 사용하면 단순히 GO를 사용할 경우보다 더욱 큰 인성 향상 효과가 있을 것으로 기대된다.
GO에 고분자를 그래프팅시켜
기능화하는 방법에는 grafting-from법과 grafting-to법이 있다. Grafting-from법은 개시제를 GO의 산소함유 관능기에
먼저 반응시키고 단량체를 중합하여 GO에 성장시키는 방법으로, 원자이동 라디칼 중합(atom transfer radical
polymerization, ATRP),10,11
RAFT 중합(reversible addition-fragmentation chain-transfer polymeri-zation),12 자유 라디칼 중합에13 의한 방법 등이 있다.
Grafting-to 법은 말단에 반응 활성기를 가지고 있는 고분자를 GO에 반응시키는 방법으로, 입체효과에 의해 높은 그래프트 밀도를 얻을 수는
없지만 원하는 분자량의 고분자를 선택적으로 그래프팅하여 특성 제어가 용이한 장점이 있다.12 Grafting-to 법에서는 GO를 먼저 개질하여
반응기를 부여하고 고분자를 반응시키는데, 폴리비닐알코올(PVA),5 폴리에틸렌글리콜(PEG),14 폴리디메틸실록산(PDMS)15 등 여러 고분자를
그래프팅시키는 방법들이 보고되고 있다.
GO를 PCL로 기능화한
기존의 연구로는 GO에 메틸렌디이소시아네이트를 도입하고 메틸렌디이소시아네이트에 PCL 디올을 그래프팅시켜 폴리우레탄의 필러로 적용한 경우가 있다.16 이 경우 GO와 PCL 사이에 메틸렌디이소시아네이트 구조가
있어 본 연구에서 시도하고자 하는 GO에 PCL을 직접 결합하는 경우와는 차이가 있다. 또한 PCL로 기능화한 GO를 PVC의 인성 향상을 위한
필러로 적용한 경우는 아직 보고된 바가 없다는 점에서 본 연구의 차별성이 있다.
본 연구에서는
PVC의 인성을 향상시키는 나노필러로 사용하기 위해 GO에 염화티오닐을 반응시켜 반응기인 염소기를 부여하고, 여기에 grafting-to법으로
분자량이 다른 PCL 디올을 그래프팅시킴으로써 기능화 GO인 산화 그래핀-g-폴리(ε-카프로락톤)(이하 GO-g-PCL로
약함)을 합성하는 방법을 검토하였으며, 합성된 GO-g-PCL의 그래프트율 등 여러 가지 특성들을 분석하였다. 또한 합성된 GO-g-PCL을
PVC에 첨가한 필름을 제조하여 인성향상 효과를 분석하였다. 이때 그래프팅 시 사용한 PCL의 분자량이 다르지만 비슷한 그래프트율(5.3~5.5%)을
갖는 GO-g-PCL을 일정 함량(0.3 wt%)으로 추가한 필름 시료들의 인성을 분석하여, GO에 그래프트되어 있는 PCL 분자량이 PVC의 인성에
미치는 영향을 검토하였다.
재료 및 시약. GO의 원료로는 Alfa Aesar사의 입자 크기
100 mesh, 순도 99.9995%의 천연 흑연 분말을 사용하였다. 그래프팅에 사용한 분자량 530 및 2000 g/mol의 PCL 디올은 Sigma-Aldrich, 분자량 1250 g/mol의 PCL 디올은 Polyscience사의 제품을 정제하지 않고 그대로 사용하였다. PVC는
LG화학의 중합도 1000인 분말 제품(K-value: 66, 입도: 45 mesh 0.2% 이하, 겉보기밀도: 0.56 g/cm3, 휘발감량: 0.3% 이하)을
사용하였다. 황산(98%)은 대정화금, 질산나트륨(98%)은 삼전순약, 과망간산칼륨(99.3%)은 삼전순약, 과산화수소(35%)는
Junsei, 염화티오닐(99%)은 대정화금의 제품을 정제 없이 그대로 사용하였다. N,N-디메틸포름아미드(DMF), 디메틸 술폭사이드(DMSO),
테트라하이드로퓨란(THF), 에틸알코올 등의 유기 용매는 HPLC급 시약을 정제 없이 그대로 사용하였다.
GO의 합성. GO는 Hummers 법을17 참고하여 다음과 같이
합성하였다. 98 wt% 황산 70 mL, 질산나트륨 1.5 g 및 흑연 2 g을 반응조에 넣고 얼음물을 채운 배스에 반응조를 넣어
0 °C 이하로 유지하면서 균일하게 교반하였다. 여기에 과망간산칼륨
12 g을 천천히 첨가하여 0 °C를 계속 유지하면서 30분간 교반한 후 얼음물 배스를
제거하였다. 이후 상온에서 갈색이 될 때까지 충분히 교반한 후, 물 280 mL를 천천히 첨가하여 교반하고 과산화수소 10 mL를 첨가하였다. 과산화수소 첨가에 의해 반응액이 오렌지색으로 변한 것을 확인한 후,
5% 염산과 탈이온수로 수세와 원심분리를 수차례 반복하여 수분산액으로 만들었다. 만들어진 수분산액을 Spectrumlabs사의 재생 셀룰로오스(regenerated
cellulose, RC) 멤브레인 튜브(12~14 kD)에 넣고 탈이온수로 48시간 투석하여 금속 이온과 산을 제거한 후, 5 mTorr로 감압하여 -70 °C에서 3일간 동결 건조하여 GO 분말을 얻었다.
GO-g-PCL의 합성. GO 100 mg을 DMF 40 mL에 넣고 30분간 초음파 처리하여 분산액을 제조하였다.
환류 냉각기가 장착된 100 mL 용량의 3구 반응조에 제조한 분산액을 넣고 질소
분위기에서 교반하면서 염화티오닐 20 mL를 천천히 적가하였다. 적가 완료 후 70 °C로 승온하여 질소 분위기에서 24시간 반응시켰다.
반응 완료 후 THF로 수세하여 PTFE 멤브레인 필터(직경 47 mm, 공경 0.45 μm)로 여과하였다. 다시 THF로 수세 및 여과를 수차례 반복하여 미반응 염화티오닐 및 부반응물을 제거하고,
상온에서 24시간 진공 건조하여 염화아실 유도체화 GO를 얻었다.
진공 건조한 염화아실
유도체화 GO와 여러 분자량의 PCL 디올을 DMSO 20 mL에 넣어 30분간 초음파 처리하여 분산액을 제조하였다. PCL 디올의 농도 변화에 따른 결과를 얻는 실험에서는
1 g GO에 반응시키는 PCL 디올의 농도를 4~32 m-mol/g-GO로 변화시켰지만, 그 외의 실험에서는
적합한 농도로 판정된(뒤의 실험결과에서 설명) 24 m-mol/g-GO로 PCL 디올의 농도를 일정하게 하였다. GO 100 mg에 대해서는 2.4 m-mol이 되어야 하므로 분자량이 각각 530,
1250, 2000 g/mol인 PCL 디올을 각각 1.27, 3,
4.8 g을 넣어 분산액을 제조하였다. 환류 냉각기가 장착된
100 mL 용량의 3구 반응조에 제조한 분산액을 넣고 교반하면서
50 °C로 승온하여 질소 분위기에서 12~72시간 동안 반응시켰다.
반응시간을 달리한 실험 이외의 경우에는 모두 50 °C에서 48시간 동안 반응시켰다. 이후의 여러가지 실험에서 PCL 농도와 그래프팅 시간을 달리하여 얻은
결과(Figure 9) 이외의 시료들은 모두 PCL 디올의 농도는 24 m-mol/g-GO로 하면서 50 °C에서 48시간 반응시킨 것들이다.
반응 완료 후
50~60 °C의 에틸알코올로 수세하여 나일론 멤브레인 필터(직경
47 mm, 공경 0.45 μm)로 여과하였다. 다시 에틸알코올로 수세 및 여과를
수차례 반복하여 미반응 PCL 디올을 제거하고, 상온에서 48시간 진공 건조하여 GO-g-PCL을 얻었다. 특별히 그래프트율(x%)을
나타낼 필요가 있는 경우에는 시료를 GO-g(x%)-PCL로 표기하였으며, 합성 시 사용한 PCL의 분자량을 나타낼 경우에는 GO-g-PCL(1250)과
같이 PCL 다음의 괄호에 표기하였다.
용매열 처리 GO 시료의 제조. 그래프트율 분석을 위해 반응 약제 없이 용매만 처리한
GO 시료를 제조하였다. 이를 위하여 염화티오닐을 첨가하지 않고 용매인 DMF 40 mL만 사용하여 GO 100 mg을 분산시키고, 70 °C에서 24시간 동안 처리한 후 수세 및 건조하였다.
이를 다시 PCL 디올을 첨가하지 않고 용매인 DMSO 20 mL만 사용하여 분산시키고, 50 °C에서 GO-g-PCL을 합성할 때와 동일한
시간 동안 반응시킨 후 수세 및 건조하여 용매열 처리된(solvothermal treated) GO를 얻었다.
PVC/GO-g-PCL 복합체 필름의 제조. PVC를 THF에 녹여 PVC 용액을 제조하였다. 그리고
그래프트율이 5.3~ 5.5 wt%인 여러 분자량의 GO-g-PCL을
PVC에 대한 무게비로 0.3 wt%가 되도록 THF에 넣고 30분간 초음파 처리하여
분산액을 제조하였다. 제조한 PVC 용액과 분산액을 혼합하여 24시간 교반하고 다시 90분간 초음파 처리하여 PVC와 GO-g-PCL을
포함하는 THF 혼합 용액을 제조하였다. 제조된 혼합 용액을 수평을 맞춘 깨끗한 유리판(패트리디쉬) 위에 캐스팅하고 상온에서 건조하여 필름 형태로
만들고, 이를 유리판에서 분리한 후 80 °C의 진공건조기에서 무게 변화가 없을 때까지 24시간 이상 진공 건조하여 두께 약 0.3 mm인 필름으로 제조하였다. 비교를 위해 100%
PVC도 THF에 용해하여 동일한 방법으로 필름으로 제조하였다.
분석. Bruker사의 VEREX 70 FTIR
Spectrometer를 사용하여 KBr 펠렛법으로 분해능 4 cm-1, 스캔수 32의 조건으로 600~4000 cm-1의 범위에 대해서 FTIR
스펙트럼들을 얻었으며 Thermo Scientific사의 DXR2xi Raman Imaging Microscope를 사용하여 532 nm의 다이오드 레이저를 광원으로 하여 50~3500 cm-1의 범위에서 Raman 스펙트럼들을
얻었다. Bruker사의 400 MHz NMR spectrometer를 사용하여, 시료들을
중수소화 클로로포름(CDCl3)에 용해시킨 후 스캔수 16으로 1H NMR 스펙트럼을 측정하였다. 이 때 용매인 CDCl3에
대한 PCL 디올 시료의 농도는 0.2 wt%로 하고 나머지 시료들은 1 wt% 농도로 하여 측정하였으며, 잔류 CHCl3
피크를 internal reference(d=7.29 ppm)로 하여 chemical shift(d) 0~ 10 ppm에 대한 스펙트럼을 얻었다. Perkin
Elmer사의 Diamond DSC를 사용하여 질소 분위기(50 mL/분)에서 10 °C/분의 속도로 80 °C까지 승온한 후 3분간 등온 유지하여 시료들의 열이력을 제거하고, -10 °C/분의 속도로 -30 °C까지 온도를 낮추면서 강온 곡선을 측정하였고,
-30 °C에서 3분간 등온 유지시킨 후 다시 10 °C/분의 속도로 80 °C까지 온도를 올리면서 재승온 곡선을 얻었다.
Bruker사의 D2 PHASER X-ray diffractometer를 사용하여, 파장 1.54 Å의 CuKa X-선에 의해 스캔 속도 0.0167° s-1로 5~50°의 2q 범위에서 적도 방향으로
0.02° 크기로 스텝 스캔하여 시료들의 XRD 회절 곡선을 얻었다. Jeol사의 JEM-2100F transmission electron
microscope (TEM)를 사용하여, 에틸알코올에 분산시킨 시료들을 holey carbon - Cu grid 위에 drop casting하고 상온에서
진공 건조하여 가속전압 200 kV로 관찰하였다. Mettler Toledo사의
TGA/DSC 1을 사용하여, 시료들에 대해 질소 분위기(50 mL/분)에서 20 °C/분의 속도로 100 °C까지 승온시킨 후 20분간 등온 유지하여 수분을 제거하고, 10 °C/분의 속도로 800 °C까지 승온하여 TGA 곡선을 측정하였다.
Thermo Scientific사의 K-Alpha+ X-ray photoelectron spectrometer(XPS)를 사용하여 AlKa(h=1486.6 eV)의 X-선으로 step size 1 eV, pass energy 200 eV의 조건으로 survey scan하고, step
size 0.1 eV, pass energy 50 eV의 조건으로 high resolution 스펙트럼을
얻었다. 200 N 로드셀을 장착한 Hounsfield사의
H10KS UTM을 사용하여 ASTM D 638에 따라 필름 시료들에 대해 폭 3.18 mm, 파지 길이 25.4 mm, 크로스헤드 속도 10 mm/min의 조건으로 하여 인성을 측정하였다.
|
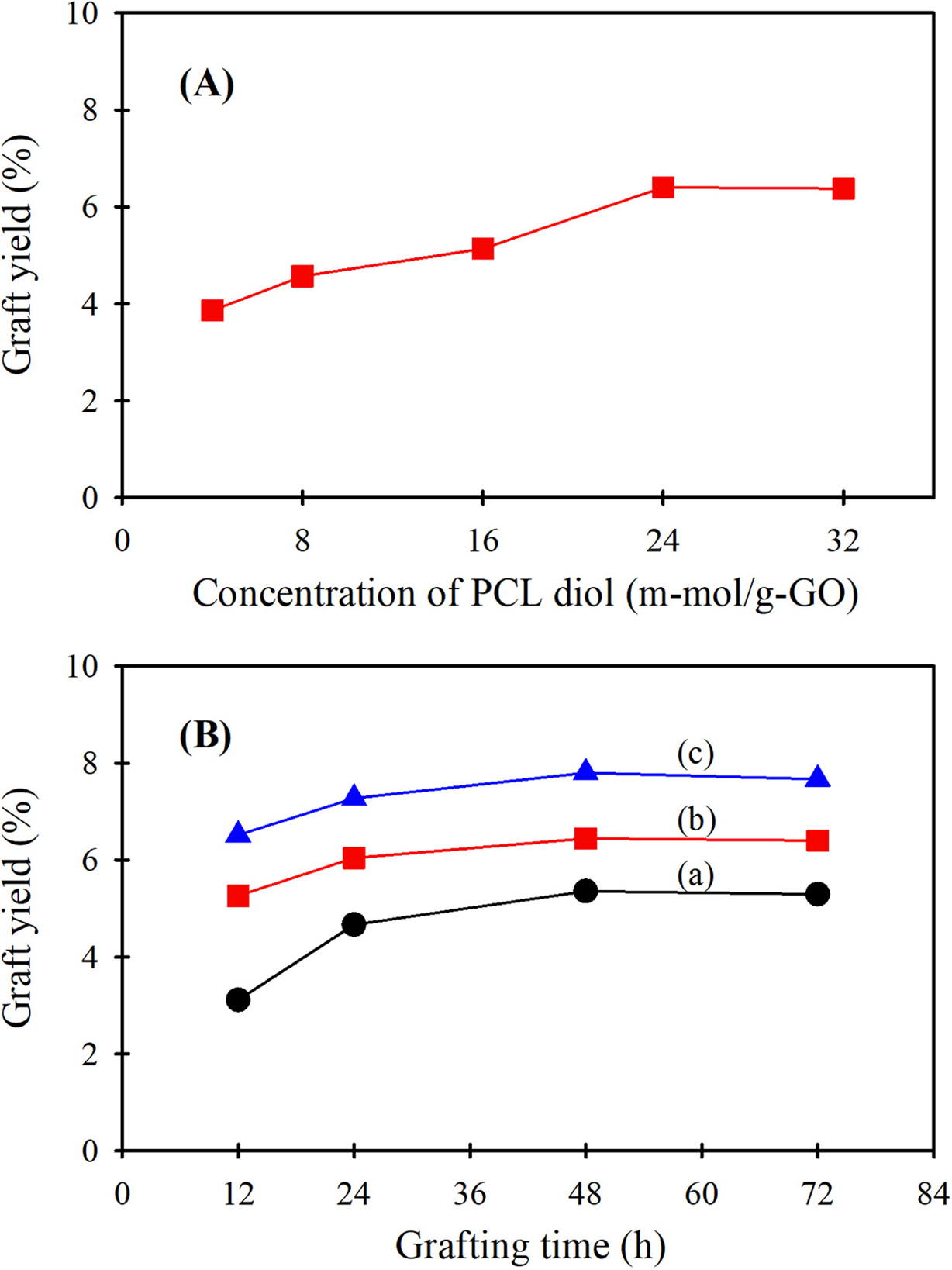
Figure 9 Changes in graft yield with (A) increasing PCL diol concentration at 50 °C for 48 h using PCL diols of MW of 1250 g/mol;
(B) increasing grafting time at 50 °C using PCL diols of MW of (a)
530 g/mol; (b) 1250 g/mol; (c) 2000 g/mol. |
GO-g-PCL의 합성 및 확인. GO-g-PCL의 합성에 사용한 GO는
흑연으로부터 제조하였다. Table 1은 본 연구에 사용한 흑연 및 이로부터 제조한 GO의 X선 회절 분석 결과를 나타낸 것으로, 제조된 GO는
0.80 nm의 d-spacing을 나타내어 d-spacing이 0.34 nm인 흑연보다 큰
면간 거리를 나타내었다. 이러한
결과로부터 흑연의 산화 및 층간 화합물 형성에 의해 층간 거리가 크게 확장되었음을 알 수 있었다. 또한 원소 분석 결과 GO의 제조에 사용한 원료인
흑연은 99.6%가 탄소로 이루어져 있는데 반해, 이로부터 제조한 GO는 탄소 51.3% 이외에 산소 36.2% 및 소량의 수소,
질소, 황 원자가 포함되어 있었다. Hummers는 GO의 탄소/산소 원자 무게비 2.25를 제시하고 있는데,17 본 연구에서 제조한
GO는 탄소/산소 원자 무게비가 1.42로 이보다 작아서 상대적으로 Hummers가 제시한 것보다 산소 원자 함량이 많았다. 이는 본 연구에서
제조한 GO에 산소함유 관능기가 충분히 포함되어 있음을 나타낸다.
이러한 GO를 원료로
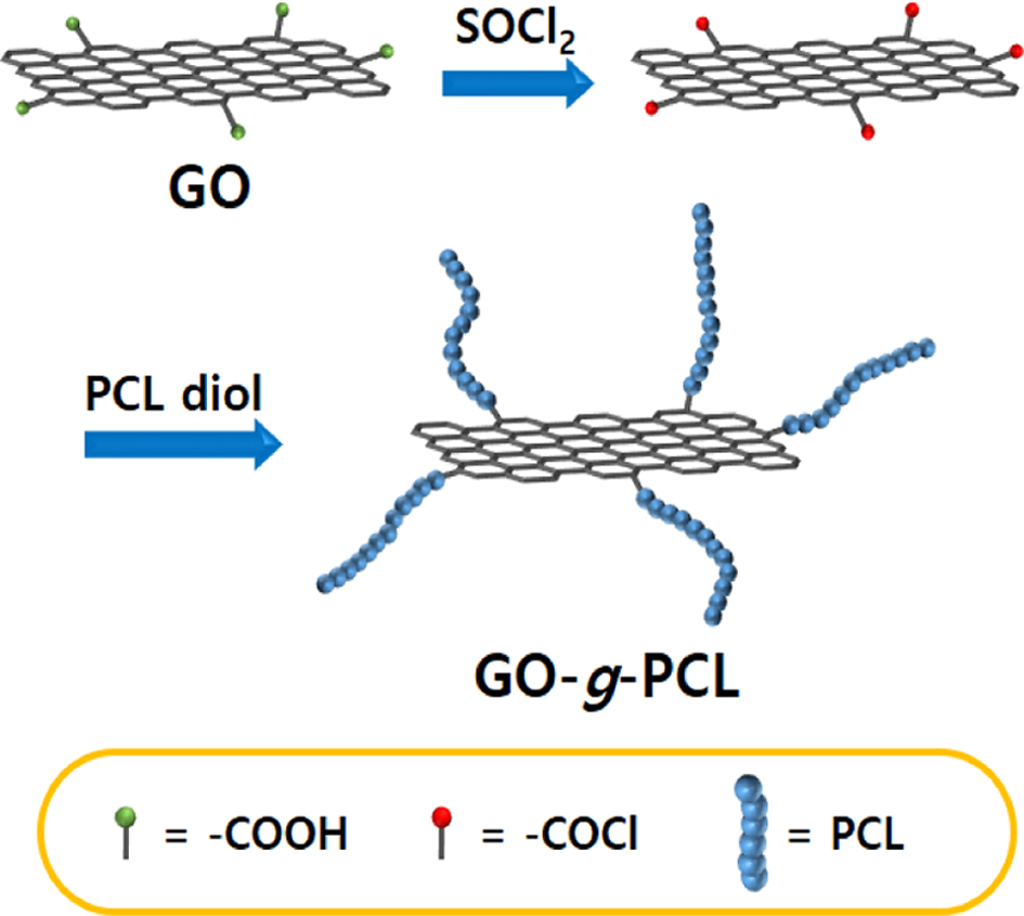
한 GO-g-PCL의 합성 방법은 Scheme 1과 같이 ① 1단계 GO의 염화아실 유도체화와 ② 2단계 PCL 디올의 그래프팅으로
되어 있다. 염화아실 유도체화 단계는 DMF 용매 하에서 염화티오닐을 반응시켜 GO에 염소기를 부여해주는 것이다. 그래프팅 단계는 DMSO 용매
하에서 PCL 디올의 히드록시기를 염소기와 반응시켜 최종적으로 GO-g-PCL이 합성되게 한다.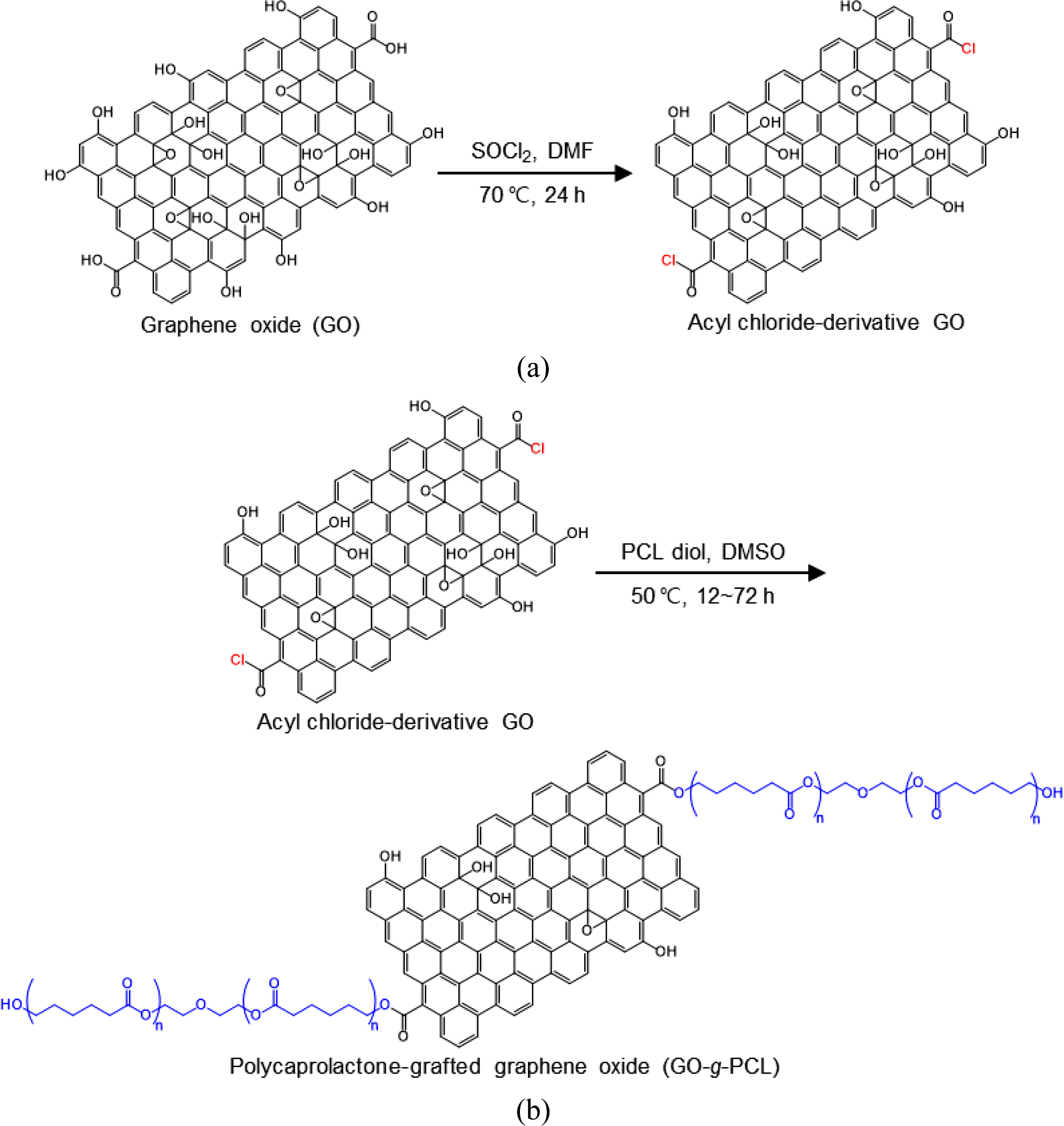
Scheme 1. Scheme for the synthesis of (a) acyl chloride derivative of GO from GO and thionyl chloride; (b) GO-g-PCL by grafting of PCL
diol on it.
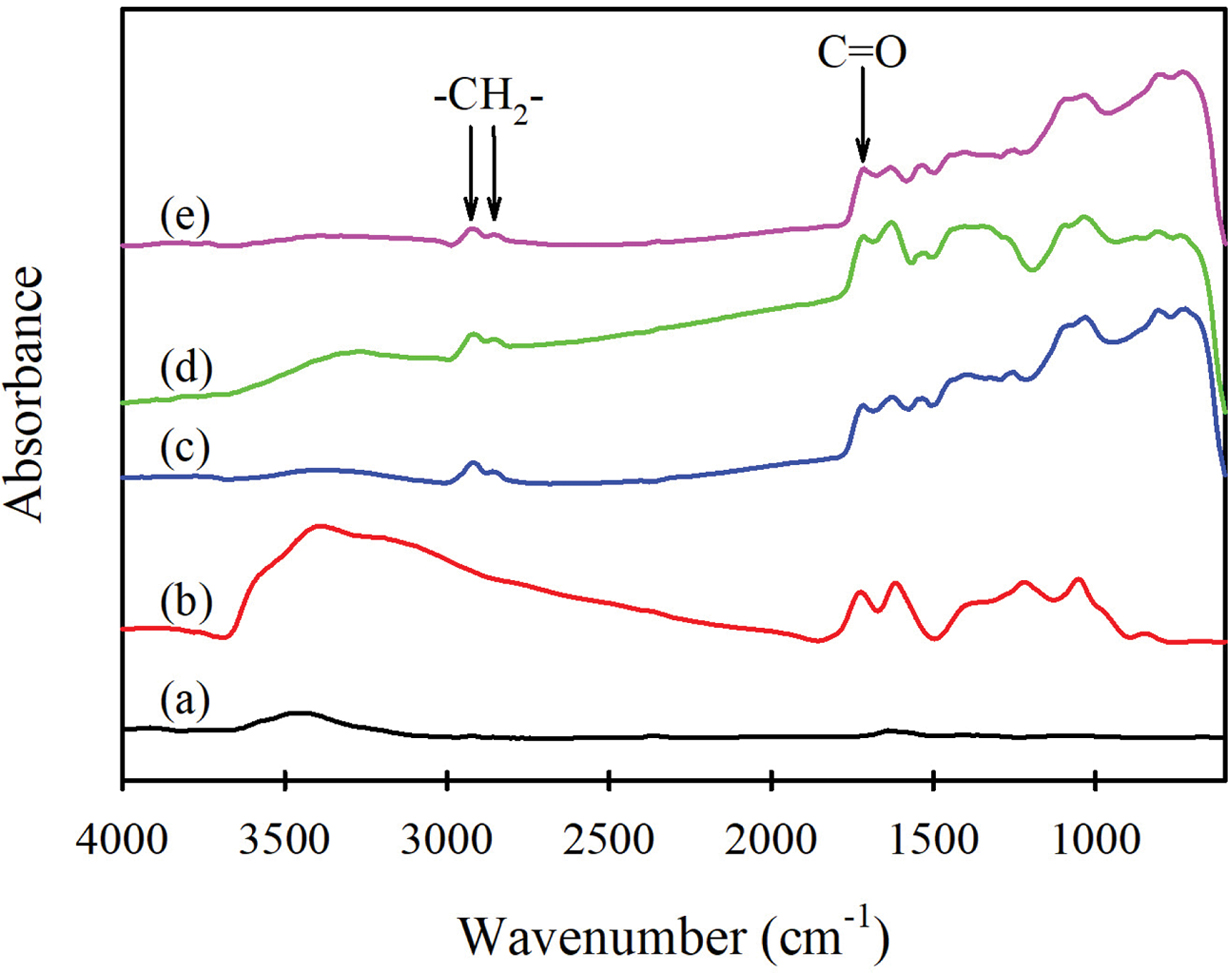
Figure 1은
흑연, GO와 이러한 GO를 염화아실 유도체화한 후 분자량이 각각 530, 1250, 2000 g/mol인 PCL 디올을 각각 GO 1 g 당 24 m-mol의 농도로 하여 50 °C에서 48시간 동안 그래프팅시켜 얻은 3가지
GO-g-PCL의 FTIR 스펙트럼을 나타낸 것이다. 흑연에는 특성 밴드가 거의 나타나지 않는데 반해, 이를 원료로 하여 제조한
GO는 3400 cm-1에 히드록시기의 O-H 신축진동,
1724 cm-1에 카복시기의 C=O 신축진동,
1219 cm-1에 에폭시기의 C-O 신축진동에 의한 밴드가 나타났다.6 따라서 흑연이 산화되어 여러 산소함유
관능기가 부여된 GO가 제조되었음을 알 수 있다. 3 종류의 GO-g-PCL은 모두 2922와 2850 cm-1에 GO에는 없는 메틸렌기에
의한 특성밴드가 나타나고 있어 GO에 메틸렌기를 가진 PCL이 그래프팅되었음을 알 수 있다.18 또한 1724 cm-1에 C=O 신축진동 밴드가
나타나는데, 이는 그래프팅되지 않고 잔류한 GO의 카복시기와 그래프팅된 PCL의 에스테르기에 의한 것이다.
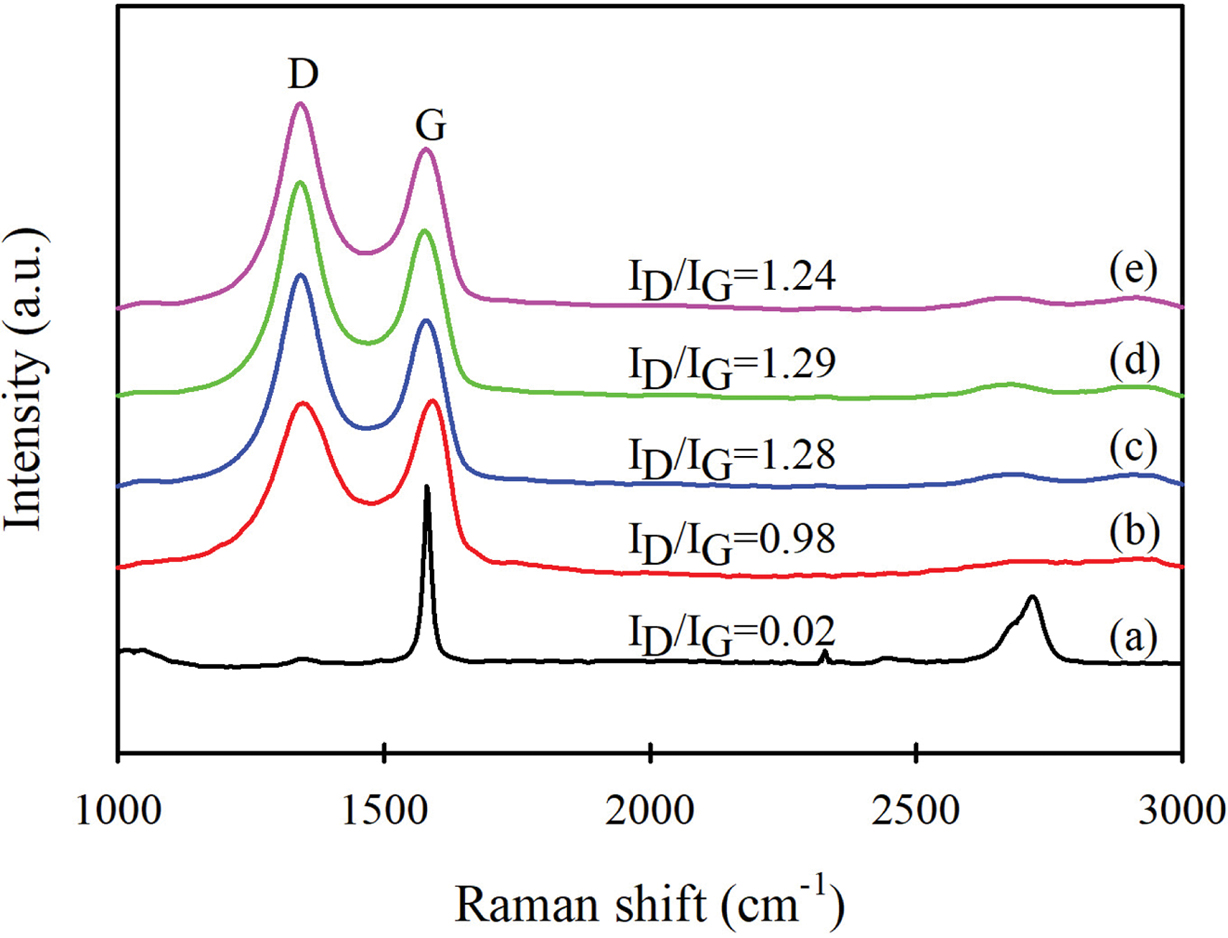
Figure 2는
흑연, GO와 이로부터 합성한 GO-g-PCL 시료들의 라만 스펙트럼을 나타낸 것이다. 흑연이나 그래핀은 산화나 공유 결합에 의한
기능화에 의해 표면의 손상이 발생하고, 이에 따라 D 밴드의 크기가 증가한다.11 흑연은 뚜렷한 G 밴드가 나타나지만 D 밴드는 거의 나타나지
않는다.6 그러나 본 연구에서 제조한 GO는 D 밴드가 뚜렷하게 나타났는데, 이는 강한 산화 반응에 의해
의해 sp2 구조가 sp3 구조로 변화하여 그래핀 평면의 sp2 영역의 크기가 감소하여
나타나는 현상이다.19 G 밴드에 대한 D 밴드의 상대적인 강도비인 ID/IG를
구하여 산화뿐만 아니라 그래프팅과 같은 화학적 개질의 정도를 파악하는데, 제조된 GO의 ID/IG는
0.98로, 0.02의 ID/IG를 나타낸 흑연과 비교하여 산화에 의해 D 밴드의
크기가 증가하였다. 따라서 산화에 의한 산소함유 관능기가 효과적으로 부여되었음을 알 수 있다. GO-g-PCL은 이보다 D 밴드의
크기가 더욱 증가하여 더 큰 1.24~1.29의 ID/IG를 나타내었으며, 이에
따라 GO에 PCL이 반응하였음을 알 수 있다.
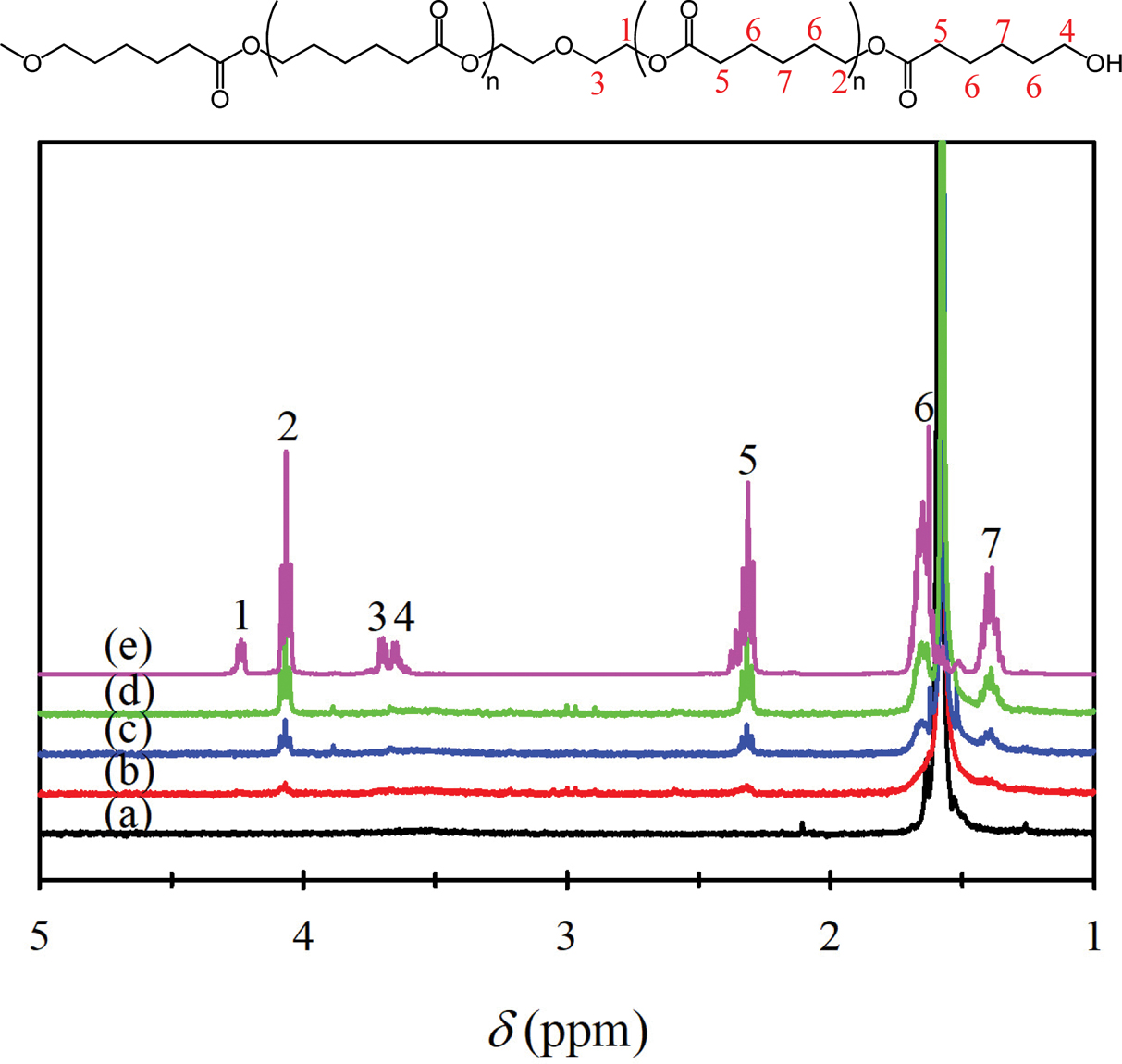
Figure 3은
GO, 합성한 3 종류의 GO-g-PCL 및 PCL 디올(MW 1250 g/mol)의 1H NMR 스펙트럼을 나타낸 것으로, PCL 디올은 구조
중 1~7번 위치의 수소에 해당하는 특성 피크들이 스펙트럼에 나타나고 있다.20-22 반면, GO의 경우는
이러한 특성 피크들이 전혀 나타나지 않았다. 3가지 종류의 GO-g-PCL에서는 PCL 디올의 화학구조 중 반복 단위의 수소 위치에
해당하는 2, 5, 6, 7번 위치의 특성 피크들이 나타났으며, 반복 단위 이외의 수소에 해당하는 1, 3, 4번 위치의 특성 피크들은 나타나지
않았다. 또한 3가지 GO-g-PCL 시료의 2, 5, 6, 7번 피크 크기가 (b)→(c)→(d) 순서로 커지고, 각 시료의 그래프트율도
각각 5.4, 6.4, 7.8%로 (b)→(c)→(d) 순서로 높아져 PCL 디올 특성 피크의 크기와 그래프트율의 결과가 어느 정도 일치함을 알
수 있다. PCL 디올에 있는 4번 위치의 피크는 말단기 -OH에 인접한 탄소에 붙어 있는 수소에 의한 것으로 GO-g-PCL에는 나타나지
않고 있다. 하지만, 이것이 반응에
의한 것인지 아니면 낮은 그래프트율과 PCL 디올의 수소 중 상대적인 양의 적음으로 인한 것인지는 알 수 없으며, 보다 정확한 반응 여부의 확인을
위해서는 다음에 설명할 추가적인 실험 결과들을 함께 고려해야 할 것으로 판단된다.
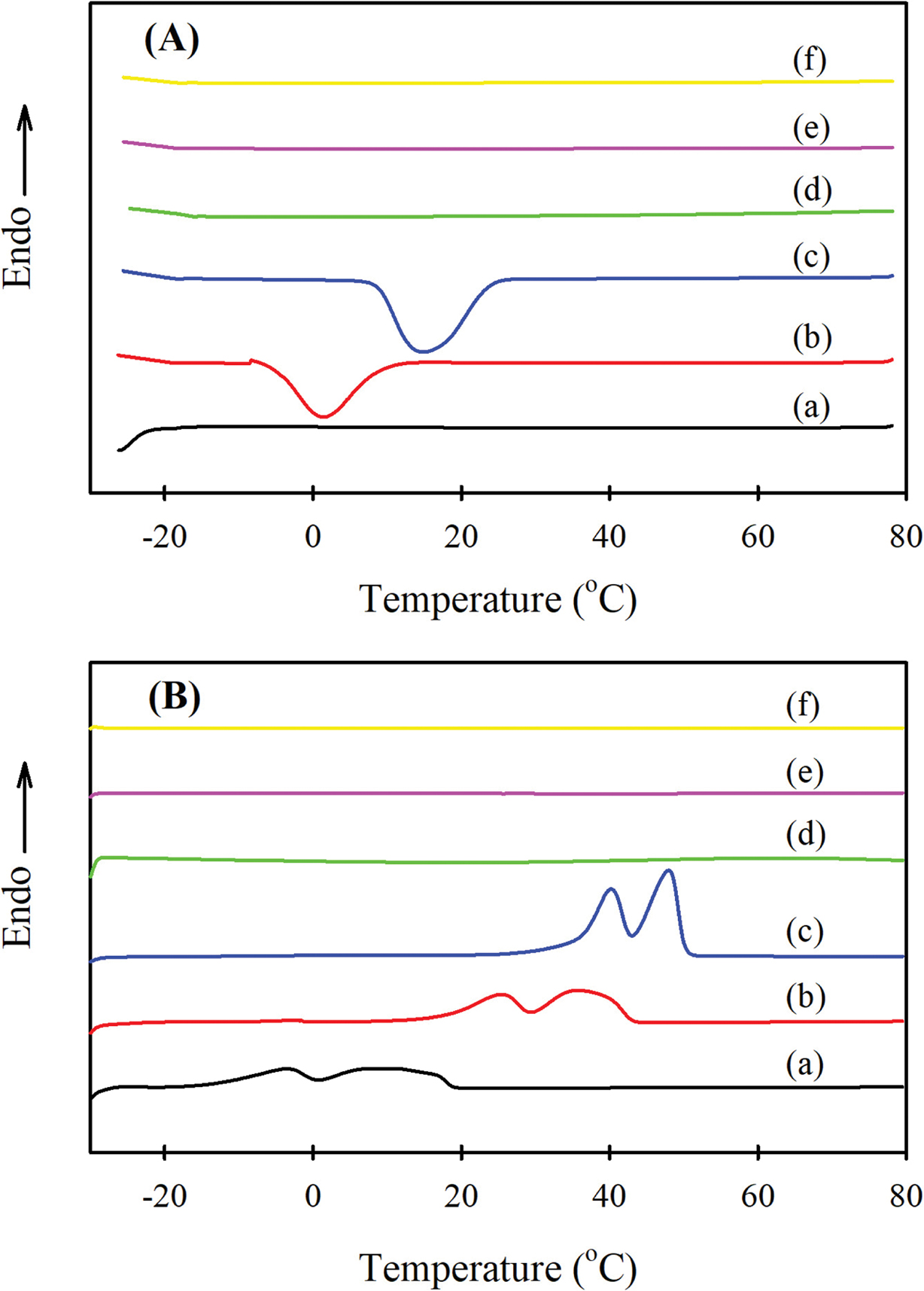
GO-g-PCL의
열적 특성을 알아보기 위하여 DSC 분석을 진행하였다. Figure 4는 원료로 사용한 3 종류의 PCL 디올과 이들로부터 합성한 GO-g-PCL들의
80 °C에서의 용융 후 강온 곡선과 이들의 재승온 곡선을
나타낸 것이다. 3종류의 PCL 디올은 모두 냉각과정에서 결정화에 의한 발열피크가 나타나고 재승온 과정에서 결정의 용융에 의한 흡열피크가 나타났으며,
분자량이 커질수록 결정화 및 용융온도가 높아지고 결정화열과 용융열도 크게 나타났다. 반면에, 합성된 3 종류의 GO-g-PCL들은
모두 결정화나 용융에 해당하는 피크가 나타나지 않았다. 한편, Figure 1의 FTIR 스펙트럼과 Figure 3의 NMR 스펙트럼 결과에서는
GO-g-PCL에 PCL 성분이 존재하는 것이 확인되었다. 따라서 GO-g-PCL에 PCL이 존재하기는 하지만, 결정을
형성하거나 용융될 수 있는 집합체 상태로 존재하는 것이 아니라 각각의 PCL 분자가 그래프팅 반응에 의해 별도로 GO에 공유결합되어 있는 상태라는
것을 알 수 있다. 즉, 이들 GO-g-PCL의 그래프트율은 5.4~7.8% 이기 때문에 시료에 존재하는 PCL의 양이 작기도 하지만,
각각의 PCL 분자들이 별도로 결정을 형성할 만한 집합체 상태가 아니기 때문이다.
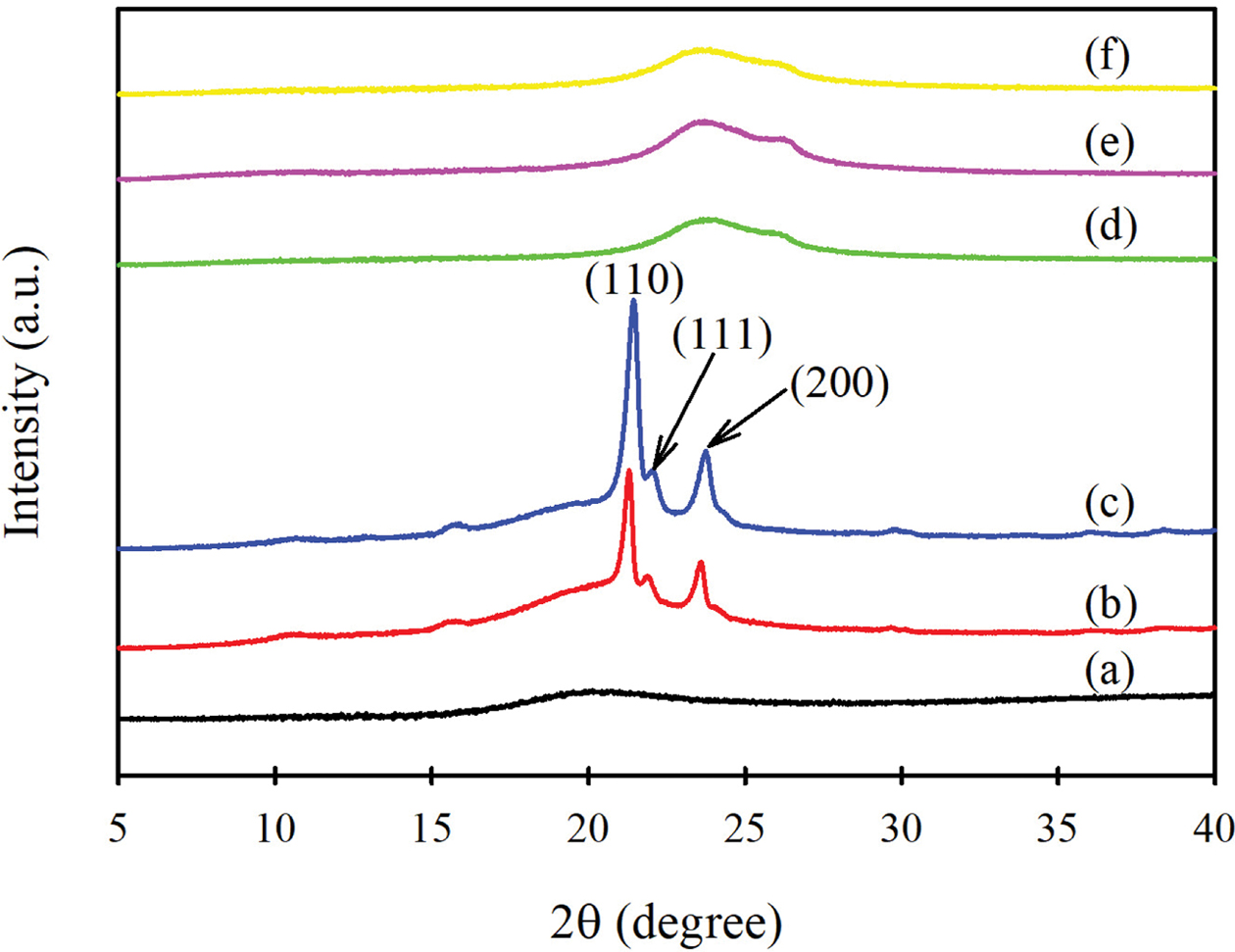
이러한 사실을 좀더
확인하기 위해 X-ray 분석을 실시하였다. Figure 5는 원료로 사용한 3가지 분자량의 PCL 디올과 이들을 사용하여 합성한 GO-g-PCL의
X선 회절 곡선을 나타낸 것이다. 분자량이 530 g/mol인 PCL 디올은 융점이 매우 낮아 상온에서 액체 상태로 존재하여 결정 피크가 나타나지 않았다.
분자량 1250과 2000 g/mol인 PCL 디올은 2q= 21.4°, 22.0°, 23.7°에서 각각 (110), (111) 및 (200) 결정면에 해당하는 결정 피크들이 나타났다.23,24 그러나 GO-g-PCL에는 이들 PCL 결정면에
해당하는 피크들이 나타나지 않고 무정형 halo 만이 나타났다. 따라서 GO-g-PCL에서 PCL이 별도 집합체로 존재하여 결정을
형성하는 것이 아니라 그래프팅에 의해 각 PCL 분자들이 GO에 공유결합되어 있다는 것을 확인할 수 있으며, 이러한 결과는 Figure 4의
DSC 측정 결과와 일치한다.
한편, GO에
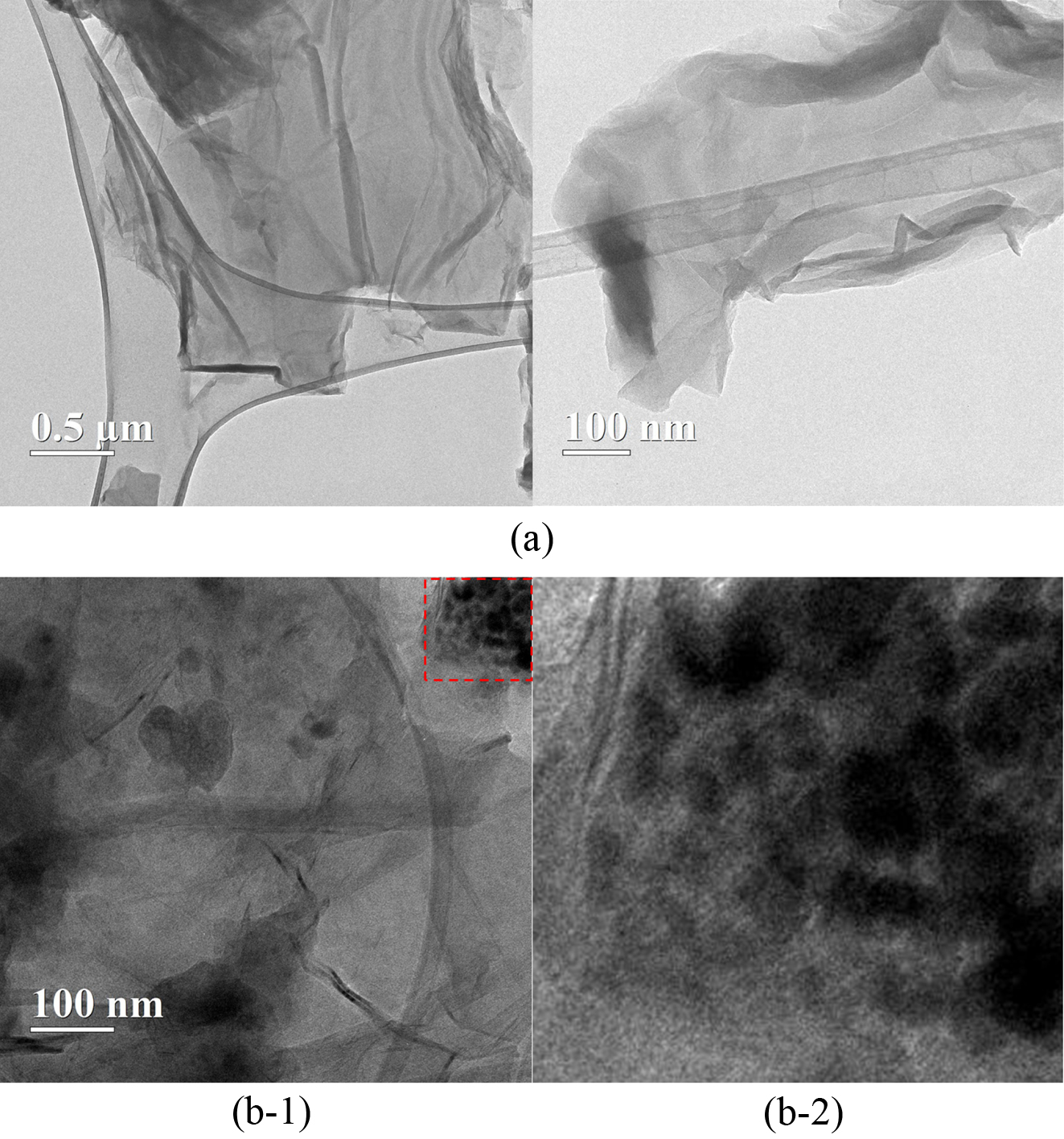
PCL이 그래프팅되어 있음을 다른 방법으로 재확인하기 위해 GO 및 GO-g-PCL의 TEM 이미지를 측정하여 Figure 6에 나타내었다.
Figure 6(a)는 GO의 TEM 사진으로, 구김 및 접힘이 있는 얇은 판상 구조를 보이면서 반점이나 응집체의 형태가 없이 깨끗한 표면을 나타내고
있어 일반적으로 보고되는 GO 형태임을 알 수 있다.25 Figure 6(b)는 GO에 분자량 1250
g/mol의 PCL 디올을 그래프팅시킨 GO-g(6.4%)-PCL(1250)의 TEM 사진이다. 이를 보면 GO와는 달리 표면에 수
nm에서 수십 nm 크기의 반점 또는 응집체 형태의 진한 부분이 랜덤하게 존재하고 있다. 이러한 TEM 사진은 전형적으로 다른 물질들이 결합된
것을 나타내는 것이다. Ye 등과12 Goncalves 등은18
GO에 PMMA를 그래프팅시킨 시료의 TEM 분석에서 비슷한 결과를 제시하고 있다. TEM 사진에서 나타나는 contrast 차이는 에너지 밀도
차이에 기반되는데, 그래프팅에 의해 본체에 결합된 고분자는 균일하게 분포되기 보다 불균일하게 분포되기 쉽다. 특히 그래프트율이 낮고 이미 만들어진
고분자 자체를 결합시키는 grafting-to법을 사용하면 불균일 분포가 되기 쉽다. Figure 6(b) 시료의 경우 그래프트율이 6.4% 정도로
작고 결합시킨 PCL의 분자량은 상당히 크기 때문에 불균일하게 분포되어 있을 가능성이 크며, 이에 따라 에너지 밀도 차이가 발생하여 TEM에서
contrast 차이로 나타난 것으로 판단된다. 다만, 이들 contrast 차이 변화가 전적으로 PCL의 그래프팅에 의한 것만이 아니라, 시료
제조시의 오염이나 GO의 일부 파편일 가능성도 있다. 그러나 본 연구의 TEM 결과만 단독으로 놓고 보면, Figure 6(b)의 GO-g(6.4%)-PCL(1250)
시료에 나타난 반점 또는 응집체가 PCL의 그래프팅에 의한 것인지 오염에 의한 것인지 명확히 구분할 수는 없지만, 앞의 FTIR, NMR,
DSC, XRD 등의 분석에 의하여 GO에 PCL이 반응한 것이 이미 확인되었고, Figure 6(a)의 GO와는 확연한 차이를 보이므로 GO에
PCL이 그래프팅되었다고 판단할 수 있다.
GO-g-PCL의 TGA 분석. 어떤 기질에 고분자가 그래프트된 시료들은 그래프트된
양인 그래프트율이 매우 중요하다. GO에 PCL이 그래프트된 GO-g-PCL 시료에서도 PCL의 그래프트율이 GO-g-PCL의
특성에 매우 큰 영향을 미친다. 그래프트율을 구하는 방법은 반응 전후의 무게 차이로부터 구하는 등 여러 가지가 있지만, 반응 후의 수세나 정제과정을
거치면 처음 출발물질의 양을 정확히 알기 어렵기 때문에 반응 후 얻어진 물질 자체를 사용하는 것이 편리한데, 이러한 방법의 하나로 TGA 열분해
곡선을 이용하는 방법이 있다. 본 연구에서 합성한 GO-g-PCL의 그래프트율을 구하기 위해서 TGA 열분해 곡선 분석법을 사용하였다.
TGA 곡선에 의한 그래프트율 분석은 기질과 그래프트된 고분자의 열분해온도가 다르다는 사실을 이용하며, 출발 물질인 GO가 차지하는 무게 분율에
대해 그래프팅된 PCL이 차지하는 무게 분율의 백분율로서 구할 수 있다.
Figure 7은
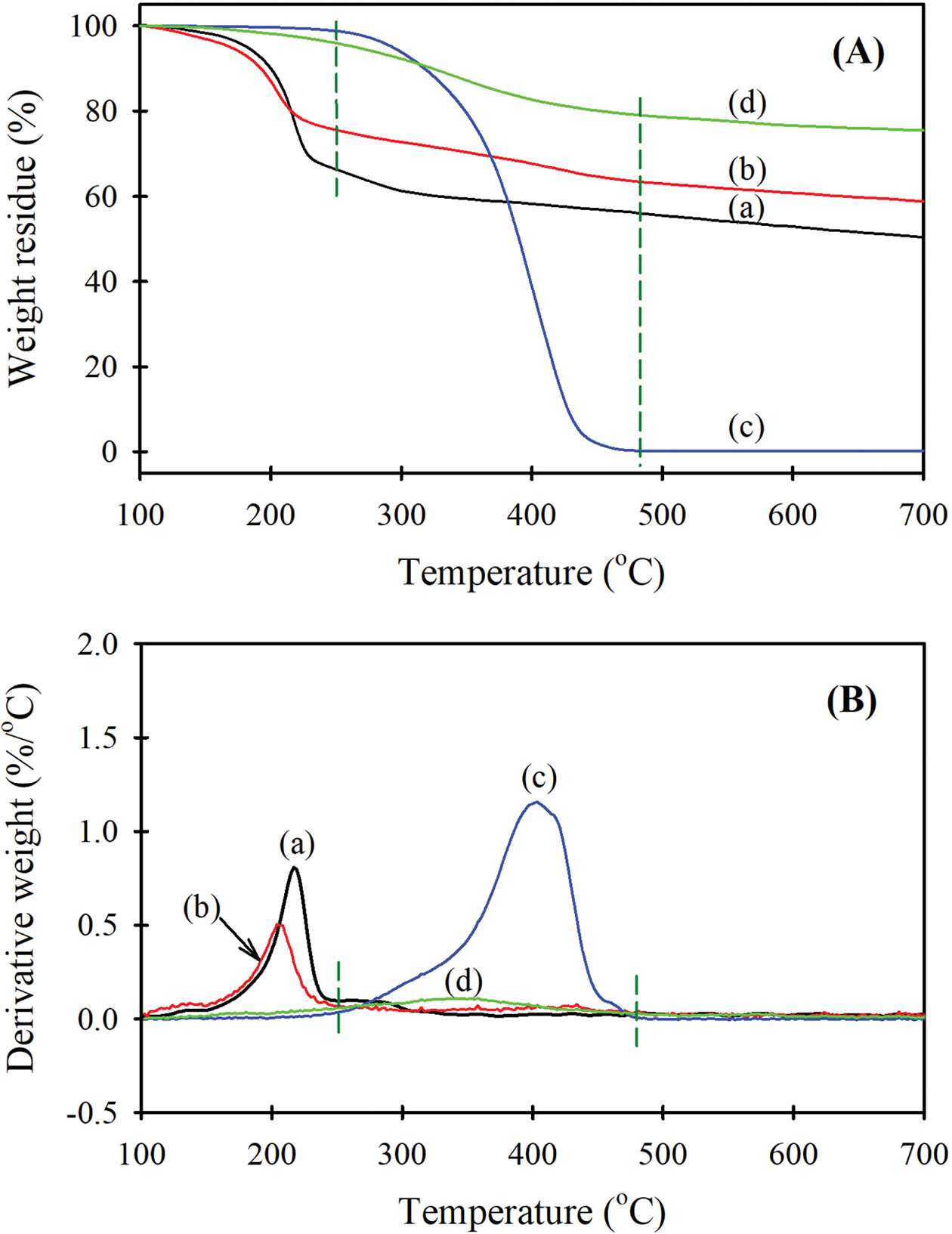
GO, 용매열 처리된 GO, PCL 디올 및 GO-g(6.4%)-PCL(1250)의 TGA 및 DTG 곡선을 나타낸 것이다. 먼저
GO는 135 °C 부근에서 열분해가 시작되어 200 °C 부근에서 급격히 열분해가 일어나는데, 이는 산화에
의해 생성된 산소함유 관능기가
CO, CO2 및 물로 분해되기 때문이다.19 이러한 산소함유 관능기의 분해에 의해 250 °C까지 약 33.7%의 무게가 감소한 후 250 °C 이상의 온도부터는 완만한 분해 거동을 보이며,
700 °C에서 약 50% 정도의 잔량을 나타내었다. 이에 비해
PCL 디올은 250 °C 부근에서 열분해가 시작되어 점차 분해가 된 후
480 °C 정도가 되면 거의 100% 분해가 되어 잔량이 거의
없게 되었다. GO-g-PCL은 GO에 비해 초기 열분해 온도가 높아지고 이후 완만한 분해 거동을 나타내며 700 °C에서의 잔존량은 GO보다 훨씬 크게 나타났다. 이는
다음과 같은 2가지 이유 때문으로 판단된다. 첫 번째로 GO에 PCL 디올이 그래프팅되는 과정에서 용매와 열에 의한 처리를 받게 되는데, 이러한
용매열적 환원에 의해 GO의 산소함유 관능기 양이 줄어들기 때문이다. 이러한 사실을 확인하기 위하여 반응 약제인 PCL 디올 없이 GO를 그래프팅
시와 동일한 용매와 처리조건에서 처리한 용매열 처리 GO를 준비하여 함께 TGA 분석하였다. Figure 7을 보면 용매열 처리한
GO(Figure 7(b))는 GO(Figure 7(a))에 비해 열분해 개시온도가 낮아지고, 250 °C까지의 무게감소율이 줄어들며 열분해 후인 700 °C에서의 잔량도 GO보다 증가하였음을 알 수 있다.
두 번째로 GO에 도입된 PCL 분자에 의해 GO의 분자 내 상호작용 및 분자간 상호작용이 증가하여 열안정성이 높아지기 때문이다.10,26 본 연구 결과와 같이 출발 물질인 GO에 비해 고분자를
그래프팅시킨 후 시료의 초기 분해온도가 더 높아지고 분해 후의 잔존량이 많아지는 예로 GO에 PEG를 그래프팅한 경우나18
GO에 PMMA를 그래프팅한 경우가14 보고되고 있다.
이러한 TGA 설명을
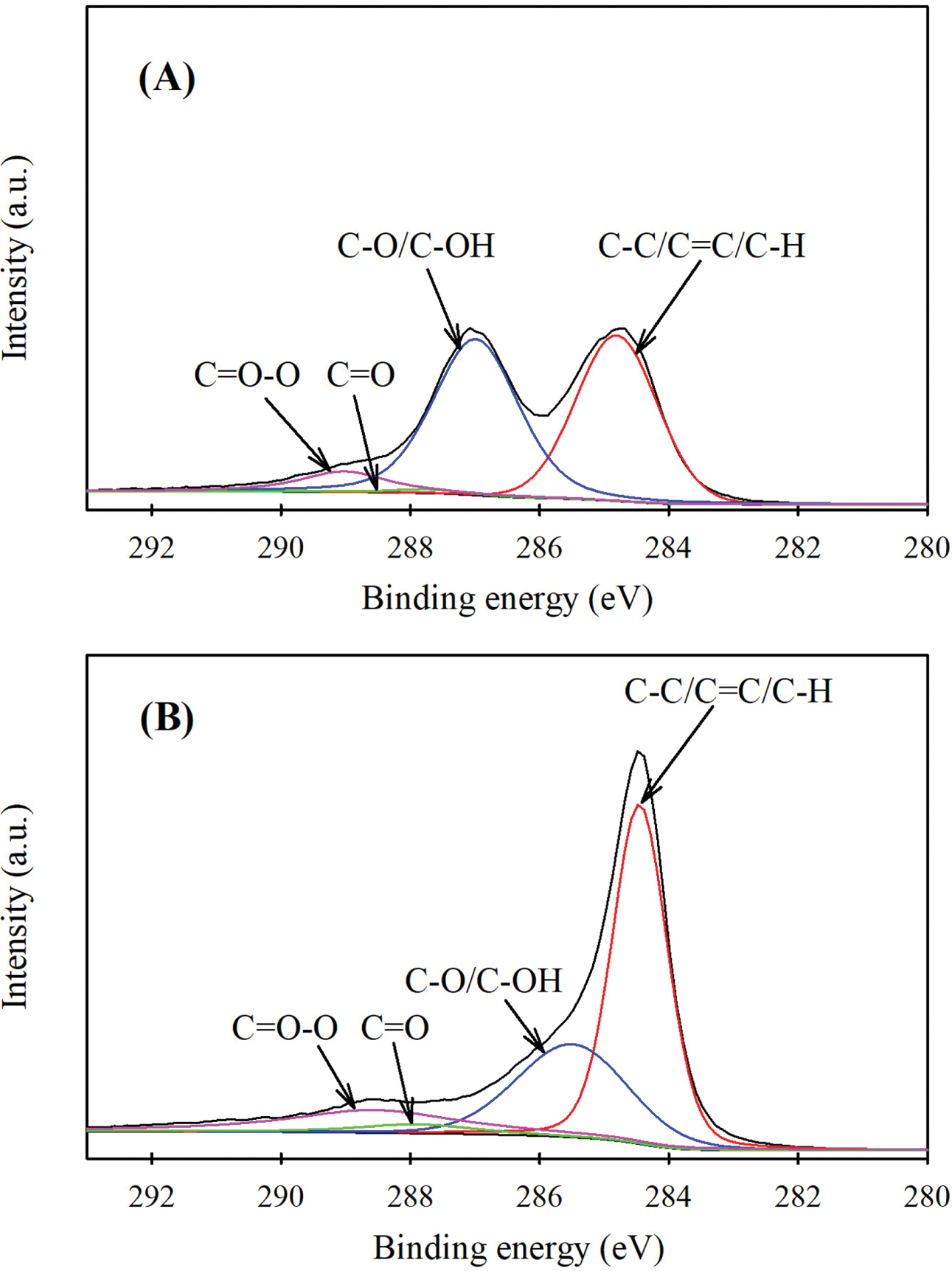
뒷받침하기 위하여 XPS 분석을 통해 시료들의 원소 조성비를 알아보았다. Figure 8은 TGA 분석 시료와 동일한 GO 및 GO-g(6.4%)-PCL(1250)의
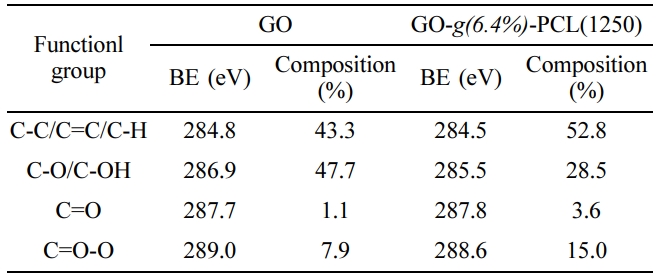
C1s에 대한 XPS 스펙트럼을 나타낸 것이며, Table 2는 각 관능기의 특성 피크에 해당하는 결합에너지 및 조성비를 구하여 나타낸 것이다.27,28 GO와 비교했을 때 GO-g-PCL은
C-C/C=C/C-H의 양이 상대적으로 많아졌고, C-O/C-OH의 양은 상대적으로 적어졌으며, C=O 및 C=O-O의 양은 상대적으로 많아졌다.
이는 그래프팅에 의해 GO에 PCL이 도입됨에 따라 PCL 주사슬의 C-C 및 C-H의 상대적인 양이 많아졌고, 염화아실화 및 그래프팅 중 용매열적
환원에 의해 GO에 있던 산소함유 관능기의 양이 감소하여 C-O 및 C-OH의 상대적인 양이 줄어들었으며, PCL 주사슬의 에스테르기의 증가에
의해 C=O-O 및 C=O의 상대적인 양이 많아진 것으로 해석할 수 있다. 이러한 결과로부터 GO-g-PCL 시료는 염화아실 유도체화
및 PCL의 그래프팅 과정에서 PCL 분자가 도입되고, 용매열 환원에 의해 일부 산소함유 관능기는 감소되었다는 것을 확인할 수 있다.
한편,
Figure 7에서 용매열 처리 GO(Figure 7(b))는 염화아실 유도체화와 그래프팅 시 염화티오닐 및 PCL 디올은 사용하지 않고 용매만
사용하여 그래프팅 시와 동일한 온도 및 시간으로 처리한 것이다. 이를 보면 200 °C 부근에서 급격한 열분해가 이루어지며, 250 °C에서 약 24.5%의 무게 감소를 보이고 이후 완만하게
분해가 이루어진다. 이는 용매열 처리하지 않은 GO(Figure 7(a))가 250 °C까지의 무게 감소가 약 33.7%인 것에 비해 적은
값이다. 이렇게 용매열 처리에 의해 GO의 무게 감소가 적어지는 이유는 DMF와 같은 유기용매는 환원력을 가지고 있기 때문에 용매열 처리에 의해
GO에 있는 산소함유 관능기의 일부가 환원됨에 따라 시료에 포함된 산소함유 관능기의 상대적인 양이 감소하기 때문이다.15
GO-g-PCL의 그래프트율 분석. 합성한 GO-g-PCL의 그래프트율 분석에는
TGA에 의한 무게감소율을 이용하였다. XPS 결과에서 확인한 바와 같이 합성된 GO-g-PCL에는 PCL 분자의 도입 이외에 용매열
환원에 의한 산소함유 관능기의 감소도 일어나기 때문에, GO-g-PCL의 보다 정확한 그래프트율을 구하기 위해서는 GO가 아닌 용매열
처리된 GO를 기준 물질로 한 무게감소율을 반영해야 한다. 한편, Figure 7에서 PCL 디올(Figure 7(c))의 열분해 곡선을 보면
250 °C에서 분해가 시작되어 480 °C에서 완전히 분해가 이루어진다. 따라서 GO-g-PCL
시료 중 PCL의 무게 분율은 GO-g-PCL의 250~480 °C에서의 무게감소율과 용매열 처리 GO 시료의
250~480 °C에서의 무게감소율의 차이로 나타낼 수 있다. 결과적으로는
GO-g-PCL의 그래프트율은 GO-g-PCL 시료에서 PCL을 제외한 나머지 성분의 무게 분율(100에서 PCL의 무게
분율을 뺀 값)에 대한 PCL의 무게 분율의 상대적 비를 백분율로 하여 구할 수 있다.
Figure 9는
PCL 디올의 농도와 분자량, 그래프팅 시간이 그래프트율에 미치는 영향을 검토한 것이다. PCL 디올의 분자량이 1250 g/mol인 것을 사용하면서 그 농도를 달리하여 50 °C에서 48시간 동안 그래프팅시켜 얻은 GO-g-PCL의
그래프트율을 TGA 분석에 의해 구하여 PCL 농도에 대해서 나타낸 것이 Figure 9(A)이다. PCL 디올의 분자량이 일정한 경우 PCL
디올의 농도가 증가함에 따라 그래프트율이 점차 커졌지만, 24 m-mol/g-GO 이상에서는 거의 일정한 그래프트율을 나타내어 이 농도를 사용하는 것이 적합하다는 것을
알 수 있다. 한편, PCL 디올의 농도를 24 m-mol/g-GO로 고정하면서 PCL 디올의 분자량 및 그래프팅시키는 시간을 12~72 시간으로 변화시켜
얻은 시료들의 그래프트율을 Figure 9(B)에 나타내었다. PCL 디올의 분자량과 무관하게 3가지 종류 모두 그래프팅 시간이 길어짐에 따라
그래프트율이 증가하였으며, 48시간 반응 시 최대 그래프트율을 나타내고 이후 시간에서는 더 이상 그래프트율이 증가하지 않았다. 이러한 결과들을
토대로, 본 연구에서 여러 가지 기기분석에 사용한 시료들을 제조할 때 PCL 디올의 농도는 24 m-mol/g-GO로, 그래프팅시키는 시간은 48시간으로
일정하게 한 것이다.
Figure
9(B)에서 전체적으로 볼 때 사용한 PCL 디올의 분자량이 커질수록 그래프트율은 커졌으며, 분자량이 530→1250→2000 g/mol로 약 2.36배 및 3.78배 증가하였지만
48시간 반응시킨 시료의 그래프트율은 각각 5.4, 6.4, 7.8%를 나타내고 있어 그 값이 상대적으로 약 1.19배, 1.44배 증가하였다.
이는 PCL 디올의 분자량이 커지면 동일한 개수의 PCL이 그래프트되는 것이 아니라 그래프트되는 분자 수는 상대적으로 적어졌음을 나타낸다. 분자량이
큰 PCL 디올의 경우, 그래프트된 분자수는 작지만 분자량이 커서 그래프트율은 상대적으로 큰 값을 나타내었다. 이를 좀 더 구체적으로 분석하기
위하여 GO 무게 1 g 당 그래프트된 PCL의 몰수인 그래프트 밀도(graft
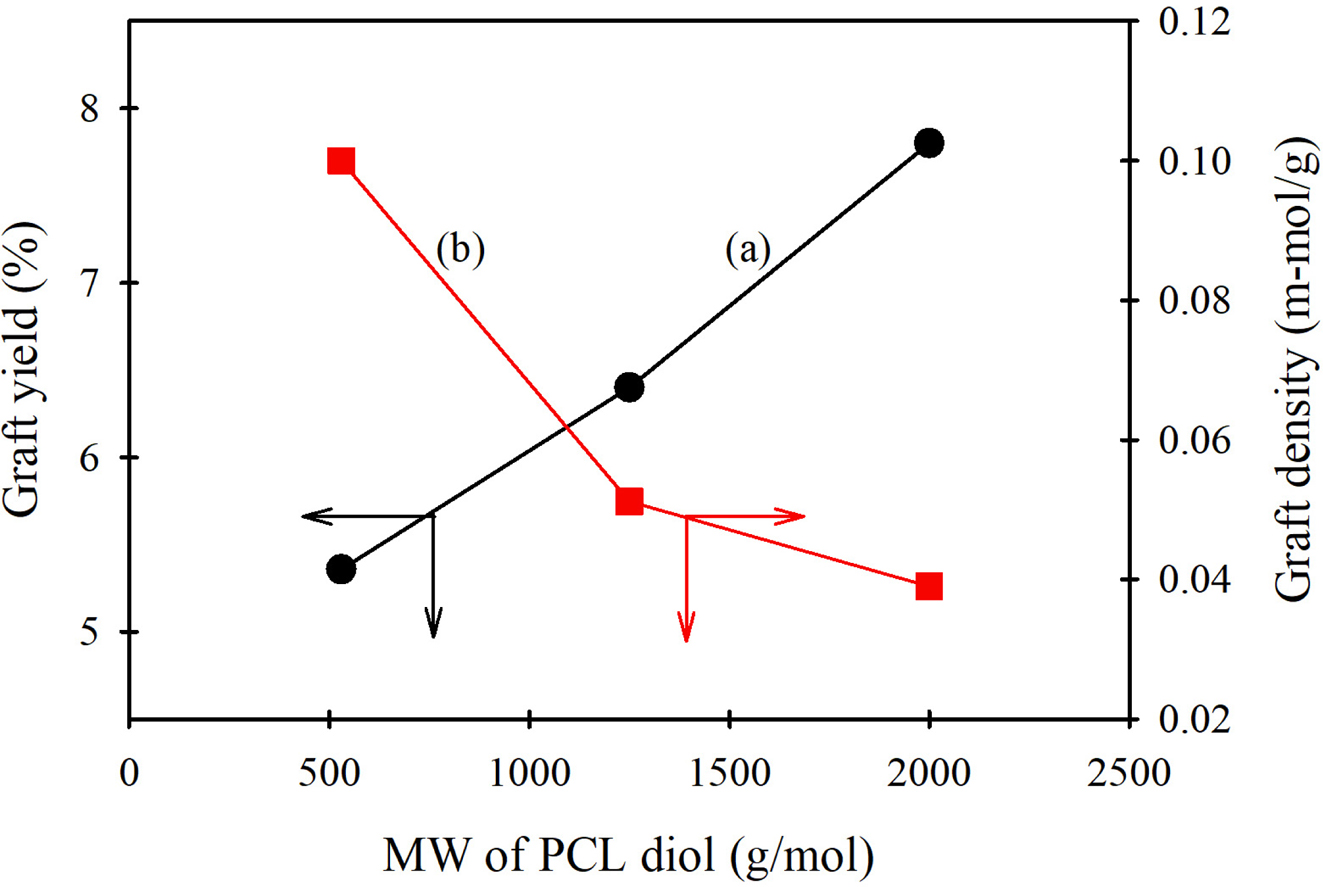
density)와 연관지어 고찰하였다. Figure 10은 530, 1250, 2000 g/mol의 3가지 분자량의 PCL 디올을 그래프팅하여
얻어진 각각의 최대 그래프트율과 이를 그래프트 밀도로 환산하여 같이 나타낸 것이다. PCL 디올의 분자량이 증가하면 그래프트율은 차례대로 각각
5.4, 6.4, 7.8%로 증가하였고 그래프트 밀도는 차례대로 각각 0.10, 0.05 및 0.04 m-mol/g로 감소하여 그래프트시키는 PCL의 분자량이
클수록 그래프트된 PCL 분자의 수가 적어졌다. 이는 분자량이 큰 PCL은 분자량이 작은 것보다 그래프팅 후 상대적으로 큰 입체적 공간을 차지하기
때문에 이웃하여 그래프트되는 PCL 분자 수에 제한을 주기 때문이다.
GO-g-PCL 첨가에 의한 PVC 필름의 인성 향상. 합성한 GO-g-PCL이 실제 PVC의 인성
향상에 기여하는 가를 알아보기 위하여 PVC/GO-g-PCL 복합체 필름을 제조하고 이들의 인성을 측정하였다. 다만, 본 연구에서는
이들이 PVC의 인성 향상에 기여할 수 있는지에 대해서만 보고하고, 복합체 필름의 강신도 변화와 같은 다른 물성들은 제시하지 않았다.
Figure 11은
분자량이 다른 3종류(530, 1250, 2000 g/mol)의 PCL 디올을 사용하여 합성한 GO-g-PCL을 0.3 wt% 첨가한 PVC 필름 및 순수한 PVC 필름의 인성을
측정하여 나타낸 것이다. 이 때 비교를 위하여 3가지 GO-g-PCL 시료는 그래프트율이 5.3~5.5%로 서로 비슷한 것들을 사용하였다.
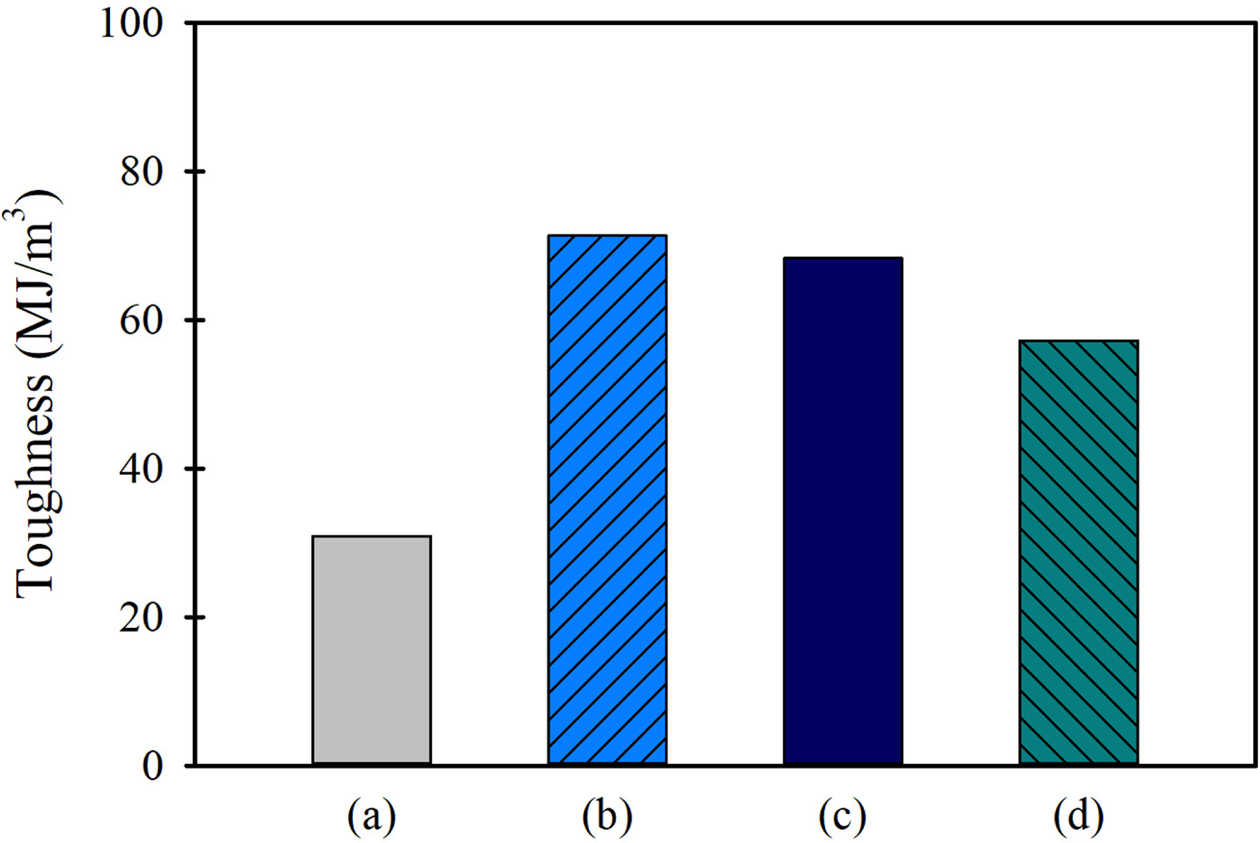
Figure 11을 보면 순수
PVC 필름의 인성이 31.0 MJ/m3인 것에 비하여, GO-g-PCL을 첨가한 필름들은 71.3, 68.3,
57.2 MJ/m3을 나타내어 각각 2.30 배, 2.20배, 1.85배로
크게 증가하였다. GO-g-PCL을 0.3 wt% 첨가한 3가지 PVC 중에서는 분자량이 530 g/mol로 가장 작은 PCL 디올을 그래프팅시킨
GO-g(5.4%)-PCL(530)을 첨가한 PVC 필름의 인성증가가 가장 크게 나타났고, 분자량이 2000 g/mol로 가장 큰
PCL 디올을 그래프팅시킨 GO-g(5.5%)-PCL(2000)을 첨가한 PVC 필름의 인성증가가 가장 작게 나타났다. 비슷한 그래프트율일
경우 분자량이 가장 작은 PCL 디올을 그래프팅시킨 시료의 그래프트 밀도가 높으며 GO에 그래프팅된 PCL 분자수가 가장 많다. GO에 도입된
PCL 분자의 개수가 많을수록 PVC와의 계면접착력이 커지고, 이에 따라 인성이 더 크게 증가하는 것으로 판단된다. 이러한 이유로 3가지 분자량
중 530 g/mol인 PCL 디올로부터 얻은 GO-g-PCL(530)을 사용하는 경우 복합체 시료의 인성 향상 효과가 가장 클 것으로
기대되지만, 이 경우 얻을 수 있는 그래프트율이 최대 5.4%로 그래프트율을 크게 증가시키는데 제한이 있었다. 분자량 1250 g/mol인
PCL 디올로부터 합성한 GO-g-PCL(1250)을 사용한 경우 그래프트율이 유사할 때 분자량 2000 g/mol인 PCL 디올로부터 합성한 GO-g-PCL(2000)에
비해 상대적으로 높은 인성 향상 효과가 있었으며, 얻을 수 있는 최대 그래프트율도 6.4%로 분자량 530 g/mol인 PCL 디올로부터 합성한 GO-g-PCL(530)에
비해 높았다.
|
Figure 1 FTIR spectra of (a) graphite; (b) GO; (c) GO-g(5.4%)-
PCL(530); (d) GO-g(6.4%)-PCL(1250); (e) GO-g(7.8%)-PCL(2000). |
|
Figure 2 Raman spectra of (a) graphite; (b) GO; (c) GO-g(5.4%)-
PCL(530); (d) GO-g(6.4%)-PCL(1250); (e) GO-g(7.8%)-PCL(2000). |
|
Figure 3 1
H NMR spectra of (a) GO; (b) GO-g(5.4%)-PCL (530);
(c) GO-g(6.4%)-PCL(1250); (d) GO-g(7.8%)-PCL(2000); (e) PCL
diol (MW 1250 g/mol). Solvent: CDCl3. |
|
Figure 4 (A) DSC cooling; (B) reheating curves of (a) PCL(530);
(b) PCL(1250); (c) PCL(2000); (d) GO-g(5.4%)-PCL(530), (e) GOg(6.4%)-PCL(1250); (f) GO-g(7.8%)-PCL(2000). |
|
Figure 5 X-ray diffraction curves of (a) PCL(530); (b) PCL(1250);
(c) PCL(2000); (d) GO-g(5.4%)-PCL(530); (e) GO-g(6.4%)-PCL
(1250); (f) GO-g(7.8%)-PCL(2000). |
|
Figure 6 TEM images of (a) GO; (b-1) GO-g(6.4%)-PCL(1250);
(b-2) enlarged image of the area indicated by the small square in (b1). |
|
Figure 7 (A) TGA; (B) DTG curves of (a) GO; (b) solvothermal
treated GO; (c) PCL diol(1250); (d) GO-g(6.4%)-PCL(1250). |
|
Figure 8 High resolution C1s XPS spectra of (A) GO; (B) GO-g
(6.4%)-PCL(1250) with peak separation of each functional group. |
|
Figure 10 Change in (a) maximum graft yield; (b) graft density of
GO-g-PCL with MW of PCL diol. |
|
Figure 11 Toughness of PVC/GO-g-PCL composite films containing 0.3 wt% GO-g-PCL prepared from different MW of PCL. (a)
neat PVC; (b) PVC/GO-g(5.4%)-PCL(530); (c) PVC/GO-g(5.3%)-
PCL(1250); (d) PVC/GO-g(5.5%)-PCL(2000). |
|
Table 2 Binding Energy (BE) of Each Functional Group in
GO and GO-g-PCL and Its Composition Obtained by C1s
XPS Spectrum |
PVC의 나노필러로
사용하기 위해 GO를 염화아실 유도체화한 후 여러 가지 분자량의 PCL 디올을 그래프팅 반응시켜 GO-g-PCL을 얻고, 이들을 분석하여
다음과 같은 결론들을 얻었다.
GO에 염화티오닐을
반응시켜 염화아실 유도체화 GO를 얻을 수 있으며, 여기에 PCL 디올을 그래프팅 반응시켜 GO-g-PCL을 합성할 수 있다. 합성된
GO-g-PCL은 FTIR, Raman, 1H NMR, DSC, X-ray 등의 여러 기기분석으로 확인할
수 있으며, GO-g-PCL에 그래프트된 PCL은 각각의 분자 형태로 결합되어 결정을 형성하지 못한다.
GO-g-PCL의
TGA 열분석 결과를 용매열 처리 GO와 비교하여 그래프트율을 구할 수 있다. 일정 온도(50 °C)에서 GO 1 g에 반응시키는 PCL의 몰 농도를 일정하게 하는 경우(24 m-mol) 그래프팅시키는 시간이 길어질수록 그래프트율이
커지지만 어느 이상의 시간(48시간)에서는 그래프트율이 더 이상 증가하지 않는다. 그래프팅에 사용하는 PCL 디올의 분자량이 클수록 최대 그래프트율은
커지지만, 그래프트되는 PCL의 상대적인 분자 수는 적어진다.
PVC에 GO-g-PCL을
첨가하면 인성 향상 효과가 있으며, GO-g-PCL의 합성에 사용한 PCL 디올의 분자량이 작을수록 인성 향상 효과는 커진다. 따라서
합성된 GO-g-PCL은 PVC의 인성 향상을 위한 필러로 응용이 가능하다. PVC의 필러로 GO-g-PCL을 사용하는 경우 그래프트율이나 첨가량 변화, 가소제와의 병행 사용 등이 PVC의 물성에 미치는 영향
등에 대한 추가 연구가 필요하다.
- 1. W. V. Titow, PVC Plastics: Properties, Processing, and Applications, Elsevier Applied Science, London and New York, p 258 (1990).
-

- 2. K. Hu, D. D. Kulkarni, I. Choi, and V. V. Tsukruk, Prog. Polym. Sci., 39, 1934 (2014).
-

- 3. Q. Bao, H. Zhang, J. Yang, S. Wang, D. Y. Tang, R. Jose, S. Ramakrishna, C. T. Lim, and K. P. Loh, Adv. Funct. Mater., 20, 782 (2010).
-

- 4. B. C. Thompson, E. Murray, and G. G. Wallace, Adv. Mater., 27, 7563 (2015).
-

- 5. H. K. F. Cheng, N. G. Sahoo, Y. P. Tan, Y. Pan, H. Bao, L. Li, S. H. Chan, and J. Zhao, ACS Appl. Mater. Interf., 4, 2387 (2012).
-

- 6. P. Oh, G. Y. Kim, and Y. H. Kim, Polym. Korea, 43, 575 (2019).
-

- 7. F. Chiu and K. Min, Polym. Int., 49, 223 (2000).
-

- 8. R. Kalousková, H. Fartáková, L. Malinová, and J. Brozžek, J. Appl. Polym. Sci., 131, 41066 (2014).
-

- 9. M. Rusu, M. Ursu, and D. Rusu, J. Thermoplast. Compos. Mater., 19, 173 (2006).
-

- 10. H. Roghani-Mamaqani, RSC Adv., 5, 53357 (2015).
-

- 11. M. Fang, K. Wang, H. Lu, Y. Yang, and S. Nutt, J. Mater. Chem., 20, 1982 (2010).
-

- 12. Y. Ye, Y. Chen, J. Wang, J. Rick, Y. Huang, F. Chang, and B. Hwang, Chem. Mater., 24, 2987 (2012).
-

- 13. Z. Liu, Z. Xu, X. Hu, and C. Gao, Macromol., 46, 6931 (2013).
-

- 14. S. Zhang, P. Xiong, X. Yang, and X. Wang, Nanoscale, 3, 2169 (2011).
-

- 15. A. Guimont, E. Beyou, P. Alcouffe, G. Martin, P. Sonntag, and P. Cassagnau, Polymer, 54, 4830 (2013).
-

- 16. Q. Jing, W. Liu, Y. Pan, V. V. Silberschmidt, L. Li, and Z. Dong, Mater. Des., 85, 808 (2015).
-

- 17. W. S. Hummers and R. E. Offeman, J. Am. Chem. Soc., 80, 1339 (1958).
-

- 18. G. Goncalves, P. A. A. P. Marques, A. Barros-Timmons, I. Bdkin, M. K. Singh, N. Emami, and J. Gracio, J. Mater. Chem., 20, 9927 (2010).
-

- 19. S. Stankovich, D. A. Dikin, R. D. Piner, K. A. Kohlhaas, A. Kleinhammes, Y. Jia, Y. Wu, S. T. Nguyen, and R. S. Ruoff, Carbon, 45, 1558 (2007).
-

- 20. Y. Lemmouchi, M. C. Perry, A. J. Amass, K. Charkraborty, and E. Schacht, J. Polym. Sci., Part A: Polym. Chem., 46, 5363 (2008).
-

- 21. G. Shi, D. G. Cooper, and M. Maric, Polym. Degrad. Stabil., 96, 1639 (2011).
-

- 22. T. Yu, J. Ren, S. Gu, and M. Yang, Polym. Adv. Technol., 21, 183 (2010).
-

- 23. H. Hu and D. L. Dorset, Macromol., 23, 4604 (1990).
-

- 24. B. Wang, Y. Li, G. Weng, Z. Jiang, P. Chen, Z. Wang, and Q. Gu, Compos. Sci. Technol., 96, 63 (2014).
-

- 25. D. Du, L. W. Y. Shao, J. Wang, M. H. Engelhard, and Y. Lin, Anal. Chem., 83, 746 (2011).
-

- 26. D. Wang and C, A, Wilkie, J. Vinyl Add. Technol., 8, 238 (2002).
-

- 27. S. Stankovich, R. D. Piner, X. Chen, N. Wu, S. T. Nguyen, and R. S. Ruoff, J. Mater. Chem., 16, 155 (2006).
-

- 28. A. Benkaddour, K. Jradi, S. Robert, and C. Daneault, Nanomater., 3, 141 (2013).
-

- Polymer(Korea) 폴리머
- Frequency : Bimonthly(odd)
ISSN 0379-153X(Print)
ISSN 2234-8077(Online)
Abbr. Polym. Korea - 2023 Impact Factor : 0.4
- Indexed in SCIE
 This Article
This Article
-
2020; 44(5): 641-651
Published online Sep 25, 2020
- 10.7317/pk.2020.44.5.641
- Received on Apr 8, 2020
- Revised on May 25, 2020
- Accepted on Jun 7, 2020
 Services
Services
Shared
 Correspondence to
Correspondence to
- Young Ho Kim
-
Department of Organic Materials and Fiber Engineering, Soongsil University, Dongjak-gu, Seoul 06978, Korea
- E-mail: ssyhkim@ssu.ac.kr
- ORCID:
0000-0001-8889-3285











 Copyright(c) The Polymer Society of Korea. All right reserved.
Copyright(c) The Polymer Society of Korea. All right reserved.