- Synthesis of Chelate Resins with Multiple Functional Groups Based on Simplified Reaction Using Mixed Solvent and Their Improved Boron Adsorption Characteristics
Young-Kill Bang*,**, Changhyun Park*,**, Junghyun Han**, Taejin Lee**, Youngju Choi**,
Jinmi Jung**, and Hyung-Il Kim*,†
*Department of Industrial Chemistry, Chungnam National University, Daejeon 34134, Korea
**R&D Center, BP Chemical Co. Ltd., Daejeon 34314, Korea- 혼합용매에 의한 단순화 반응 기반 다중 관능기 도입 킬레이트 수지의 합성 및 보론 흡착특성 향상
*충남대학교 공과대학 공업화학과, **㈜비피케미칼, R&D센터
Poly(St-co-DVB)
crosslinked polymer was synthesized by suspension polymerization as a base material for boron adsorption in order to apply
to the water treatment system. Poly(St-co-DVB) crosslinked polymer was
subjected to chloromethylation reaction to synthesize various chelate resins
having glucamine groups, as porous spherical particles of an average size of
500 μm. The chelate resins were synthesized by the simplified reaction of
chloromethylation and glucamine substitution without phase separation by
applying mixed solvent and compatibilizing solvent. Chelate resins with the new
structure were synthesized using low molecular weight amino alcohol containing
a hydroxyl group in order to solve the steric hindrance problem among glucamine
groups in the substitution reaction. As a result, the new structure of chelate
resin enabled the adsorption of boron ion to be improved more than 30% higher.
Boron removal characteristics of chelate resins were evaluated depending on
crosslinking agent content and introduction of both glucamine and aminoalcohol
groups.
수처리 시스템에 적용하기 위한 보론 흡착용 기본 수지로 poly(St-co-DVB) 가교중합체를 현탁중합으로 합성하였다.
기본 수지에 대하여 염화메틸화 반응을 거쳐 글루카민기가 도입된 킬레이트 수지를 평균 입경 500 μm 구형의 고다공성 수지로 합성하였다. 이러한 반응과정에서 혼합용매와
상용화 용매를 사용하여 상분리 없이 반응단계를 간소화하여 킬레이트 수지를 합성하였다. 글루카민기의 입체장애에
따라 글루카민 치환반응이 원활히 진행되지 못하는 문제점을 하이드록시기를 갖는 저분자량 아미노알코올을 사용하여 해결함으로써 보론 이온 흡착률이 30% 이상 향상된 새로운 구조의 킬레이트 수지를 합성하였다. 이러한
킬레이트 수지에 대해서 가교제 함량, 글루카민기 및 아미노알코올기 도입이 보론 흡착특성에 미치는 영향을
조사하였다.
Chelate resins were synthesized by simplified
reaction of chloromethylation and glucamine substitution with mixed solvent and
compatibilizing solvent. Chelate resins, which contained both glucamine and
aminoalcohol groups, showed the improved adsorption capability for boron ion.
Keywords: chelate resin, boron adsorption, glucamine, amino alcohol, water treatment
이 논문은 산업통상자원부
2019년도 산업기술혁신사업 산업핵심기술개발사업(과제번호: 10062871)의 지원으로 수행된 연구입니다.
해수 담수화는 다양한
염류, 중금속 등의 불순물이 함유되어 있는 해수로부터 불순물을 제거하여 음용수나 기타 용도로 이용할 수 있도록 하는 공정이다.1 특히
해수 내에 함유된 중금속 중 보론은 붕산(B(OH)3)과 테트라하이드로보레이트 음이온(B(OH)4-)의
두 가지 형태로 존재하는데, 특히 붕산은 극성이 없고 입자의 크기가 미세하여 종래의 방법으로는 제거가 어렵기 때문에, 일반적으로 보론 함량
3~6 ppm인 해수의 담수화 과정에서 해수 내에 존재하는 보론의
60~70% 정도만 제거된다.2-4 그러나 이렇게 처리된 처리수의 보론 농도는 국내 음용수 수질 기준인 1 ppm 뿐만 아니라 국제보건기구(WHO)의 권고 기준인
0.5 ppm을 초과하여 음용수 수질 기준을 충족시키지 못한다.5-7
한편, 글루카민기가
결합된 킬레이트 수지는 보론 이온에 대해 매우 우수한 선택적 흡착 능력을 보인다.8-10 따라서 높은 보론 농도 수질을 갖는
지역에서의 음용수 제조 및 해수 담수화 처리시스템에서 보론 제거를 위해 매우 중요한 소재로 대두되고 있는 상황이다.11,12
일반적으로 해수 등에
존재하는 보론을 제거하기 위해서 보론 농도를 고려하여 다양한 방법이 적용되고 있다. 저농도의 보론을 함유하는 용액은 이온교환수지, 역삼투막, 담수화
그리고 pH 변화 등의 방법을
이용해 보론을 제거한다.13-15 그러나 고농도의 보론을 함유하는 해수 등으로부터 보론을 효과적으로 제거하기 위해서는 강산성
양이온 교환수지와 강염기성 음이온 교환수지의 조합에 의한 흡착방법이나 킬레이트 수지에 의한 보론 흡착방법이 적용되고 있다.16,17
킬레이트 수지에 의한 보론 흡착방법은 기존의 다른 방법보다 보론 이온에 대한 선택적 흡착능이 우수하며, 킬레이트 수지 흡착제의 반복적인 사용이
가능하다는 장점이 있다.18 하지만, 중금속이온 흡착용 기존 킬레이트 수지로부터 제조된 보론
흡착제는 보론 흡착능력이 불충분할 뿐만 아니라 킬레이트 수지 내에 보론 흡착 능력을 향상시킬 관능기의 도입 반응도 충분하게 진행될 수 없다는 문제점이
있다.19
따라서 본 연구에서는
기존에 사업화되어 있는 흡착 수지를 기본 소재로 하여 기계적 물성 변화를 최소화하면서도 보론 제거 특성을 향상시키기 위해서 극성 혼합용매를 사용하여
수지를 효율적으로 팽윤시킬 뿐만 아니라 반응 단계를 단순화시켜 보론 흡착기능의 글루카민기가 가교수지의 내부까지 충분히 도입될 수 있도록 하였다.
이를 위하여 선행 연구에서 적용했던 가교제 함량 20 wt%의 poly(St-co-DVB) 가교수지뿐만 아니라 가교제 함량 5.0, 7.5,
10.0 및 15.0 wt% 조건에서 합성한 가교수지도 적용하였다.20
이러한 가교수지들에 대해 치환반응 과정을 통해 글루카민기를 도입하였다. 또한, 하이드록시기를 포함하는 저분자량 아민 화합물을 사용하여 아미노알코올기를
추가 도입하는 반응을 통해 치환반응 과정에서 미치환된 염화메틸기 함량을 최소화하였다. 이러한 새로운 방법으로 합성된 킬레이트 수지에 있어서 가교도
및 관능기에 따른 보론의 흡착 성능 변화를 조사하였다.
재료 및 시약. 다공성 비드 형태의 킬레이트 수지를 합성하기 위하여 단량체로
styrene(St, 99%, Aldrich), 가교제로 divinyl benzene(DVB, 55%, Aldrich), 개시제로
benzoyl peroxide(BPO, Aldrich), 기공형성제로 2,2,4-trimethylpentane (isooctane,
99.8%, Aldrich), 그리고 분산안정화제로 hydroxypropyl methylcellulose(HPMC, Aldrich)를 사용하였다.20 염화메틸화 반응을 위해서
chloromethyl methyl ether (CMME, technical grade, Aldrich) 및 zinc chloride(ZnCl2,
³98%, Aldrich)를 사용하였다. 킬레이트 수지에 글루카민기를 도입하기 위해서 N-methyl-D-glucamine(N-MDG,
³99.0%, Aldrich)을 사용하였다. 용매로 methyl ethyl ketone(MEK, 99.0%, Aldrich),
1,2-dichloroethane(DCE, ³99.8%, Aldrich), 그리고 tetrahydrofuran(THF,
99.9%, Aldrich)을 사용하였으며, 이때 반응물들과의 혼화성 향상을 위한 상용화 용매로는 에탄올(95.0%, Aldrich), 메탄올(95.5%, Aldrich) 및
isopropyl alcohol(IPA, 99.5%, Aldrich)을 사용하였다. 아미노알코올기를 도입하기 위해서
diethanolamine(DEA, ³98.0%, Aldrich), N-methylethanolamine(MEA, ³99.0%, Aldrich)를 사용하였다. 또한 각각의 반응과정에서 세척을 위해 메탄올(99.5%, Samchun), 에탄올 및 3차 증류수를 사용하였다.
제조된 킬레이트 수지의 보론 이온 흡착특성 평가를 위해서 보론 표준용액(1000 ppm, Kanto)을 사용하였다.
보론 흡착용 킬레이트 수지 합성. 보론 흡착용 킬레이트 수지는 4단계 반응을 거쳐 합성하였다.
첫번째 단계는 poly(St-co-DVB) 가교수지의 합성, 두번째 단계는 가교수지에 대한 염화메틸화 반응, 세번째 단계는 글루카민기
도입반응, 마지막 단계는 아미노알코올기 도입반응이다.
Poly(St-co-DVB) 가교수지 합성: Poly(St-co-DVB) 가교수지를 합성하기
위한 반응기로 2리터 4구 배플형 이중자켓 반응기를 사용하였다. 반응기 중앙에 패들형(paddle type) 교반기를 설치하고 다른 1구에는 냉각용
콘덴서를 설치하여 반응중 단량체 유적의 균일한 분산과 반응용액의 증발을 방지하였다. 분산안정화제 HPMC 0.1%를 분산매에 넣고 1시간 교반하여
용해시켰다. 0.1% HPMC용액 1200 g을 반응기에 넣고 140~150 rpm으로 교반시키며 분산매 온도를 40 oC로 조절하였다.20
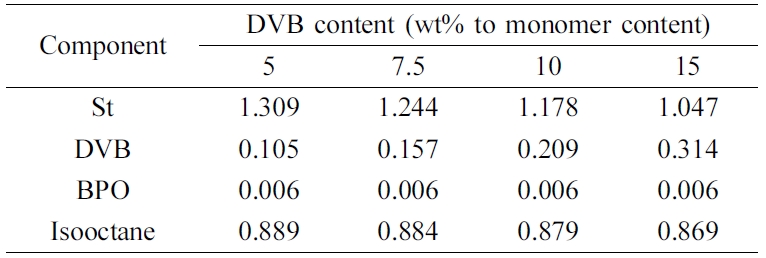
Table 1에 나타낸
조성에 따라 단량체(St), 가교제(DVB), 중합개시제(BPO), 기공형성제(isooctane) 혼합물을 40 oC 분산매에 30분 동안 적가하여 안정한 분산상을 형성하였다. 이후, 40 oC에서부터 4시간에 걸쳐 1시간 간격으로 10 oC씩 승온시키며 80 oC에 도달할 때까지
현탁중합을 진행시키고, 80 oC에 도달한 후 추가로 12시간 동안 중합을 진행시켰다. 현탁중합 완료 후 합성된 가교중합체를 250 μm 체를 이용하여 분리하였다. 합성된 가교중합체는 증류수와
메탄올을 사용하여 충분히 세척하여 불순물을 제거하였고, 세척된 가교중합체는 70 oC의 진공오븐에서 12시간 이상 감압 건조하였다.
염화메틸화 반응: 테프론 코팅된 교반기가 반응기 중앙에 설치되고 다른 1구에는 냉각용 콘덴서가 설치된 1리터
4구 이중자켓 반응기에 poly(St-co-DVB) 가교수지 50 g, CMME 400 g을 넣고 반응물 온도를 10 oC로 유지하며 2시간 동안 140~150 rpm으로 교반시켰다. 이러한 반응물 용액에 루이스산
촉매 ZnCl2 40 g을 20 g씩 2번에 나누어 투입하고 2시간 동안 반응하였다. 이후, 온도를 50 oC로 올려서 추가로 15시간 동안 반응시켰다. 염화메틸화 반응이 완료된 수지를 여과분리한 후 3차 증류수와
에탄올을 이용하여 1차 세척하고 이어서 에탄올로 상온에서 2시간 동안 2차 세척하였다.20
글루카민기 도입 반응: 염화메틸화 반응이 진행된 poly(St-co-DVB)
가교수지에 보론 이온의 흡착 특성을 나타내는 글루카민기가 최대한 치환되도록 하기 위해서 혼합용매 조건에서 글루카민기 도입 반응을 진행하였다. 반응기
중앙에 교반기가 설치되고 다른 1구에는 냉각용 콘덴서가 설치된 1리터 4구 이중자켓 반응기에 염화메틸화 가교수지 50 g을 넣은 후 Table 2에 나타낸 조성에 따라 N-MDG,
용매인 3차 증류수 및 MEK 혼합용매,
그리고 상용화 용제인 에탄올을 넣고 80 oC로 유지하며 20시간 동안 반응시켰다. 글루카민기 도입 반응이 완료된 킬레이트 수지를 3차 증류수로 1차 세척하고
이어서 3차 증류수로 상온에서 2시간 동안 2차 세척하였다.
아미노알코올기 도입 반응: 반응기의 중앙에 교반기가 설치되고, 다른 1구에는 반응
중 용액의 증발을 방지하기 위하여 냉각용 콘덴서가 설치된 1리터 4구 이중자켓 반응기에 글루카민기가 도입된 킬레이트 수지 50 g, DEA 또는 MEA 아미노알코올 25 g, 탈이온수(D.I. water) 225 g을 넣고 약 80 oC의
온도로 유지하며 12시간 동안 반응시켜 아미노알코올기를 도입시킨 킬레이트 수지를 합성하였다. 아미노알코올기 도입 반응이 완료된 킬레이트 수지를 에탄올로 세척한 뒤, 3차 증류수로 여러 번 세척하여 최종적으로 보론 흡착용
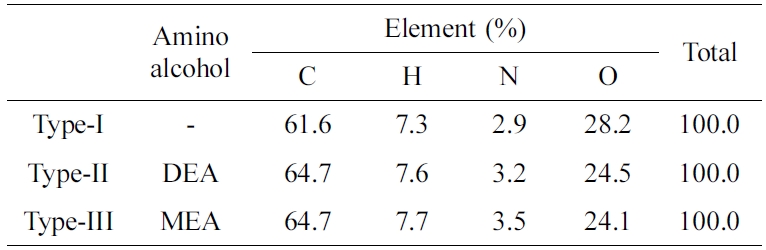
킬레이트 수지를 합성하였다. 이렇게 제조된 보론 흡착용 킬레이트 수지에 대해 원소분석을 통하여 질소함량을 분석하여 Table 3에 나타내었다.
가교에 따른 팽윤도 측정. 가교수지의 팽윤도를 비교하기 위하여 가교제 함량
5.0, 7.5, 10.0 및 15.0 wt%의 조건에서 합성된 염화메틸화 가교수지 10 mL에 MEK 용매 30 mL 넣고 15시간 뒤 증가된 부피를 측정하였다.
Figure 1에 나타낸 바와 같이 가교제 함량이 낮아질수록 팽윤도가 증가하였다. 또한 용매 변화에 따른 가교수지의 팽윤도 변화를 비교하기 위하여
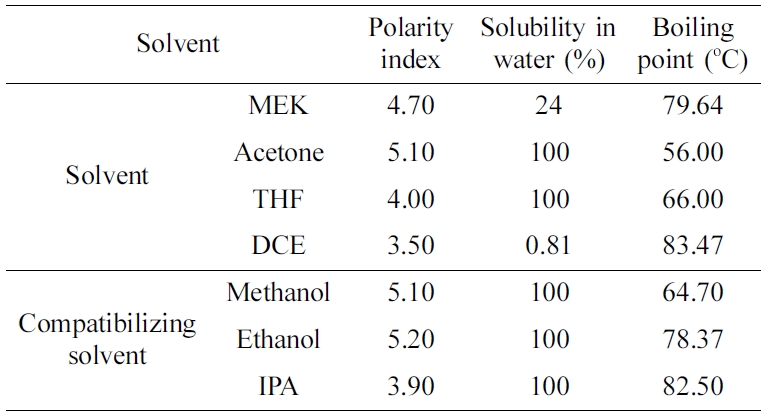
물과의 혼합 용매인 MEK, 아세톤, DCE 및 THF와 상용화 용매를 사용하여 혼합용매를 제조하였다. 상용화 용매로는 극성과 혼합용매의 공비점을
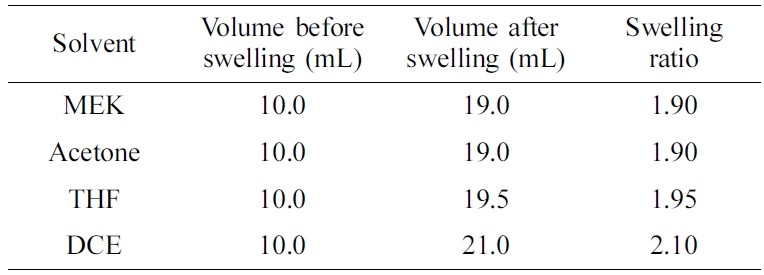
고려하여 다양한 알코올을 사용하였다(Table 4). 용매 종류에 따른 가교수지의 팽윤도를 비교하기 위하여 염화메틸화 가교수지 10 mL에 다양한 혼합용매 30 mL 넣고 15시간 경과 뒤 증가한 부피를 측정하여 그
결과를 Table 5에 나타내었다. Table 5에 나타난 바와 같이 DCE를 용매로 사용한 경우 다른 용매보다 가교수지의 팽윤도가 크지만 보론
이온의 흡착특성을 나타내는 주요 관능기인 글루카민기 도입 반응에 있어서 반응물들의 상용성을 고려하면 반응용매로 MEK를 사용하는 것이 더 적합하였다.
분석. Micromeritics사의 Tristar
TM3000 및 Autopore IV9520을 사용하여 구상 킬레이트 수지의 비표면적과 세공용적을 측정하였다. Scanning
electron microscope(SEM, Tescan, Vega II LSU)를 사용하여 킬레이트 수지의 형태학적 특성을 분석하였다.
Thermo Finnigan사의 Flash EA-1112 series elemental analyzer(EA)를 사용하여 킬레이트 수지 내에 포함된
원소를 분석하였다. Fourier-transform infrared spectroscopy(FTIR, Bruker, Alpha_T)를 사용하여
킬레이트 수지의 관능기를 확인하였다. Agilent사의 400 MHz 54 mm NMR DD2(Solid-NMR)를 사용하여 가교수지에 대한 단계별 반응 진행 후 화학구조 변화를 확인하였다.
킬레이트 수지의 보론 흡착용량을 측정하기 위하여 킬레이트 수지를 0.2 g씩 정확히 측량하여 용기에 넣고, 보론 이온 고농도 용액(200 ppm) 20 mL를 주입한 후 25 oC에서 24시간 동안 서서히 교반하면서 보론 이온을 흡착시켰다.20 원자흡광분광법(Thermo
Scientific, iCAP 7400)을 사용하여 보론 이온 흡착 완료 후 보론 이온
용액의 농도변화를 측정하여 보론 이온 흡착량을 구하였다.21
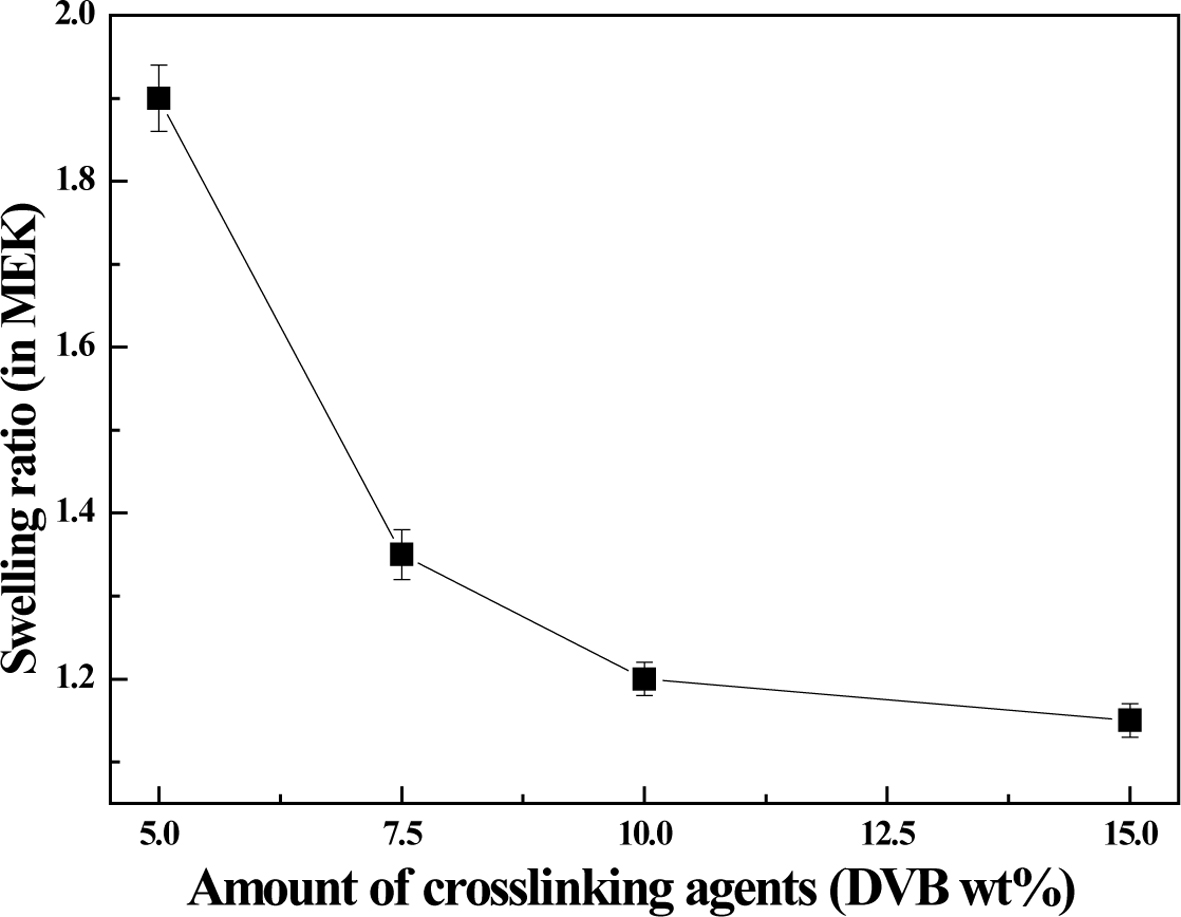
|
Figure 1 Variation of swelling ratio of chloromethylated poly(Stco-DVB) crosslinked resin depending on crosslinking agent content. |
|
Table 1 Reactant Composition for Synthesis of Poly(St-co-DVB) C rosslink ed Resin w ith Isooctane a s Pore F orming Agent (unit: mole) |
|
Table 2 Reactant Mixture Composition for Glucamine Substitution of Chloromethylated Poly(St-co-DVB) Crosslinked Resin |

|
Table 3 Elemental Analysis Results of Various Poly(St-co-DVB) Chelate Resins for Boron Adsorption |
|
Table 4 Polarity, Solubility and Boiling Point of Various Solvents and Compatibilizing Solvents |
|
Table 5 Variation of Swelling Ratio of Chloromethylated Poly(St-co-DVB) Crosslinked Resin with 5.0 wt% Crosslinking Agent |
킬레이트 수지 합성. 킬레이트 수지의 보론 이온 흡착 특성을 최적화하기 위해서는
기본 가교수지를 최대한 팽윤시킨 상태에서 보론 이온 흡착능을 갖는 관능기가 가교수지의 내부까지 충분히 도입되어야 한다. 이를 위해 본 연구에서는
선행 연구에서 킬레이트 수지를 합성하였던 4단계의 공정 중, 세번째 단계로서 악취가 심한 유해 물질을 사용하는 DMS-염화반응 공정을 생략하는
대신 혼합용매를 이용하여 기본 가교수지의 팽윤도를 증가시킨 상태에서 고분자사슬에 글루카민기를 최대한으로 도입하는 단순화 공정방법을 적용하여 킬레이트
수지의 보론 이온 흡착 성능을 최적화하고자 하였다.18,19 또한 글루카민기의 도입반응에서 poly(St-co-DVB)
가교수지에 도입되는 N-MDG의 긴 사슬구조에 따른 정전기적 반발력이 가교수지에 도입된 염화메틸기와 N-MDG 사이의
원활한 치환반응에 입체적 장애요인으로 작용하여 글루카민기 도입 반응 완료 후에도 10~30%의 미치환된 염화메틸기가 존재하고 결과적으로 킬레이트
수지의 보론 흡착능력이 저하되는 문제점이 있었다. 따라서 하이드록시기를 포함하고 분자량이 50~150인 저분자량 아민류 화합물인 DEA 또는
MEA를 사용하여 관능기를 추가 도입하는 단계인 아미노알코올기 도입반응을 추가로 진행시킴으로써 미치환된 염화메틸기 함량을 최소화할 수 있었다.
Scheme 1에 나타낸 반응 과정을 통하여 가교도가 다른 4종류의 구상형 가교 킬레이트 수지들을 합성하였다. 적절한 기계적 강도를 유지하면서
비표면적과 세공용적을 증가시키기 위해서 다공성 구상형 poly(St-co-DVB) 가교수지를 합성하였다.20 용매
함량을 90 vol%로 고정한 상태에서 가교제 함량을 단량체 총량
대비 5.0, 7.5, 10.0 및 15.0 wt%로 변화시켜 가교수지를 합성하였고 가교제 함량에 따른 poly(St-co-DVB) 가교수지의
비표면적 및 세공용적 변화를 조사하였다. 또한 이들 가교수지에 글루카민기를 도입시킨 킬레이트 수지의 비표면적 및 세공용적 변화를 조사하였다.
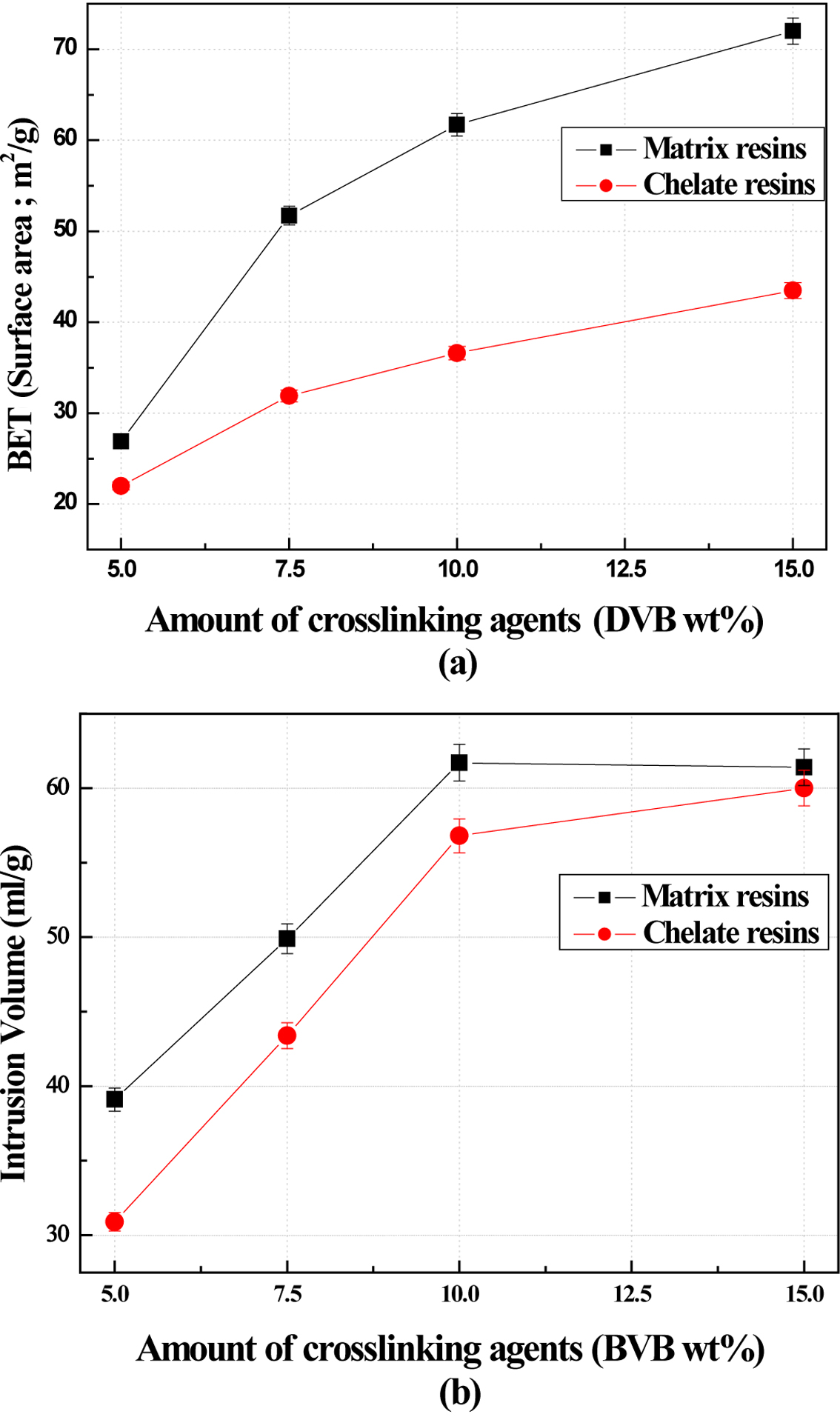
Figure 2에 나타낸 바와 같이 가교제 함량이 증가함에 따라 가교수지 및 킬레이트 수지의 비표면적 및 세공용적이 증가하였다.22,23
많은 양의 관능기가
도입되면 기본 가교수지의 세공용적 보다 킬레이트 수지의 세공용적이 낮아지게 된다. 즉, 기본 가교수지와 킬레이트 수지의 세공용적 차이가 클수록
관능기가 높은 효율로 도입되었음을 의미한다. Figure 2에서 보는 바와 같이 가교도가 낮을수록 기본 가교수지와 킬레이트 수지의 세공용적 차이가
증가하는 경향을 보였다. 따라서 관능기 도입이 최대화된 킬레이트 수지를 합성하기에 적합한 기본 poly(St-co-DVB) 가교수지로는
가교제 함량이 단량체 총량 대비 5.0 wt%로 합성된 가교수지를 사용하였다.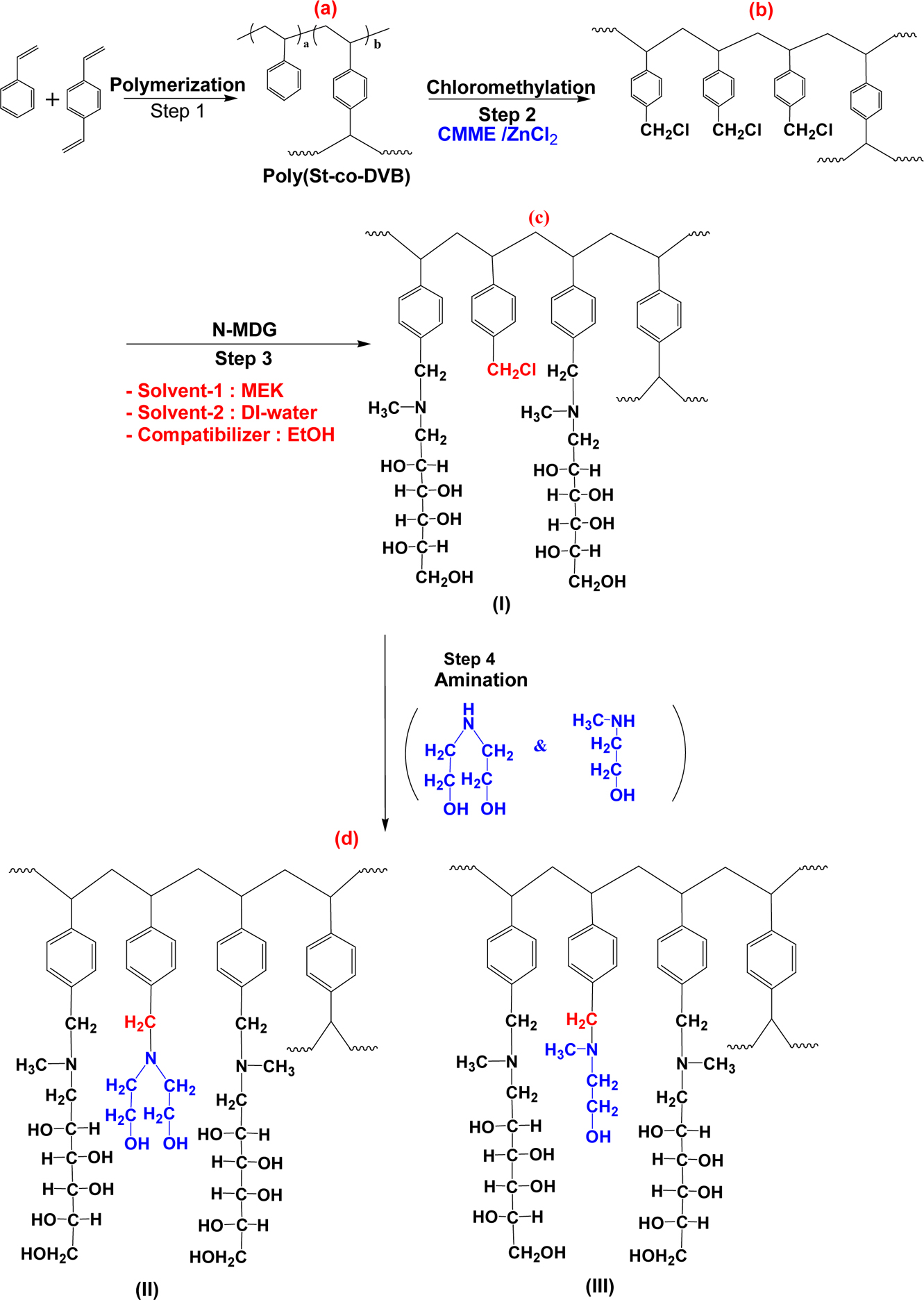
Scheme 1. Schematic synthetic routes for preparation of poly(St-co-DVB) chelate resin.
킬레이트 수지의 구조분석. Poly(St-co-DVB) 가교수지를 합성하고,
이를 기본 가교수지로 하여 염화메틸화 반응, 글루카민기 도입 반응, 아미노알코올기 도입 반응 등의 화학적 개질반응을 진행시켜 보론 흡착용 킬레이트 수지를 합성하였다. 이러한 합성단계에서 각각의 시료에 대해 FTIR 분석을
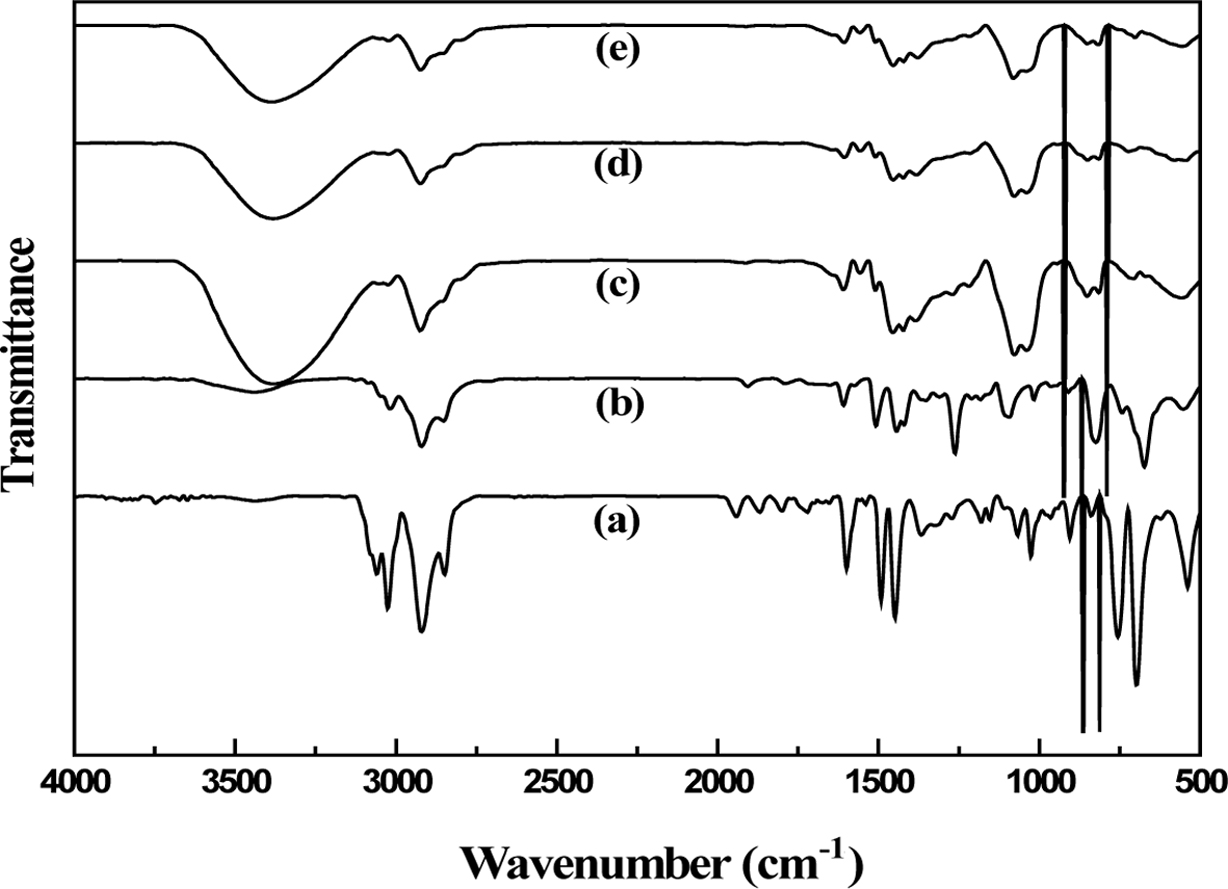
진행하였고 그 결과를 Figure 3에 나타내었다. Poly(St-co-DVB) 가교수지의 경우 650-850 cm-1 영역과 1475-1600 cm-1 영역에서 styrene과
divinyl benzene 방향족에 의한 피이크가 확인되었다. 염화메틸화 반응이 진행된 poly(St-co-DVB) 가교수지의 경우에는
염화메틸기의 C-Cl 특성 피이크가 600-700 cm-1 영역과 1200-1300 cm-1 영역에서 확인되었다. 반면에, 글루카민기 도입 반응이
진행된 poly(St-co-DVB) 가교수지의 경우에는 3300-3500 cm-1 영역에서 -OH기 진동 피이크가
확인되었다.24 또한 글루카민기의 C-N 특성 피이크가 1000-1350 cm-1 영역에서 확인되었다. 마지막으로
아미노알코올로서 DEA가 도입된 poly(St-co-DVB) 킬레이트 수지 및 MEA가 도입된 poly(St-co-DVB)
킬레이트 수지의 경우에는 염화메틸기(-CH2Cl)의 염소 특성 피이크가 훨씬 더 약하게 나타나는 것으로 보아 상기 글루카민기
도입 반응 완료 후 미반응 상태로 존재하던 염화메틸기가 대부분 아미노알코올기로 치환된 것으로 판단되었다.
또한
poly(St-co-DVB) 가교수지 및 단계별 반응이 진행된 킬레이트 수지에 대해서 추가적으로 solid state 13C
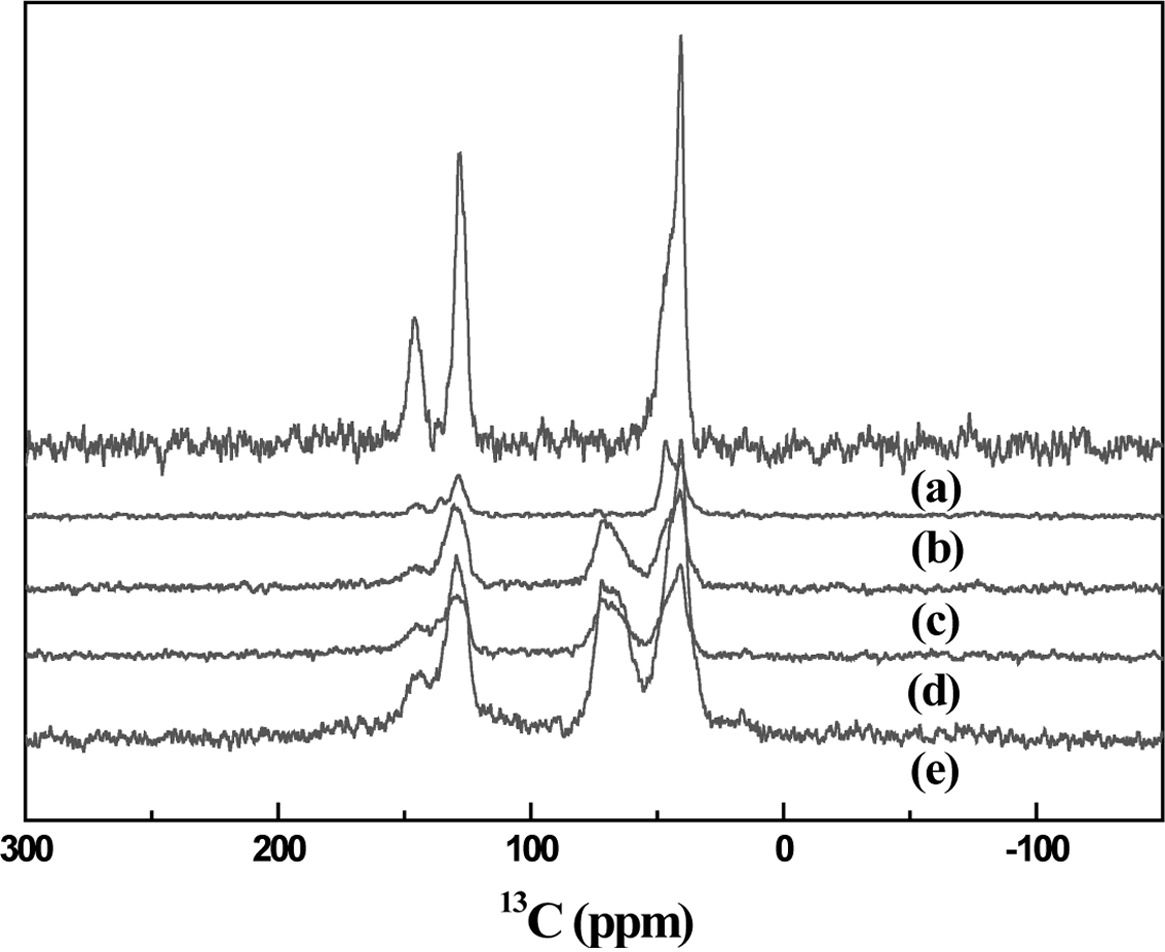
NMR 분석을 통해 벤젠고리에 치환된 관능기의 구조를 확인하여 Figure 4에 나타내었다. 모든 시료에 공통적으로 나타나는 32-48 ppm의 피이크는 poly(St-co-DVB)
가교수지 주사슬 골격의 탄소를 나타내고 125-145 ppm의 피이크는 곁사슬 벤젠고리의 탄소를 나타낸다. 염화메틸기 치환된 poly(St-co-DVB)
가교수지에서 치환기 탄소 피이크가 50 ppm에서 주사슬 골격의 피이크와 일부 겹쳐서 나타났다. 반면에, 글루카민기 및 아미노알코올기가 치환된 킬레이트
수지에서는 해당 관능기의 탄소 피이크가 70-75 ppm에서 뚜렷하게 나타났다.
Poly(St-co-DVB)
기본수지에 대한 단계별 반응의 반응수율에 대해서는 벤젠 고리에 도입되는 염화메틸기에 의한 무게증가 및 도입된 글루카민 또는 아미노알코올기의 질소
함량을 원소분석으로 확인하여 각각 염화메틸화 반응 96.5%, 글루카민 또는 아미노알코올기 도입된 Type I, II, III 킬레이트 수지가
각각 74.0%, 81.6%, 89.3%의 수율을 나타냈다.
킬레이트 수지의 보론 흡착 특성. 가교제 함량을 변화시켜 합성한 4종류 킬레이트 수지의
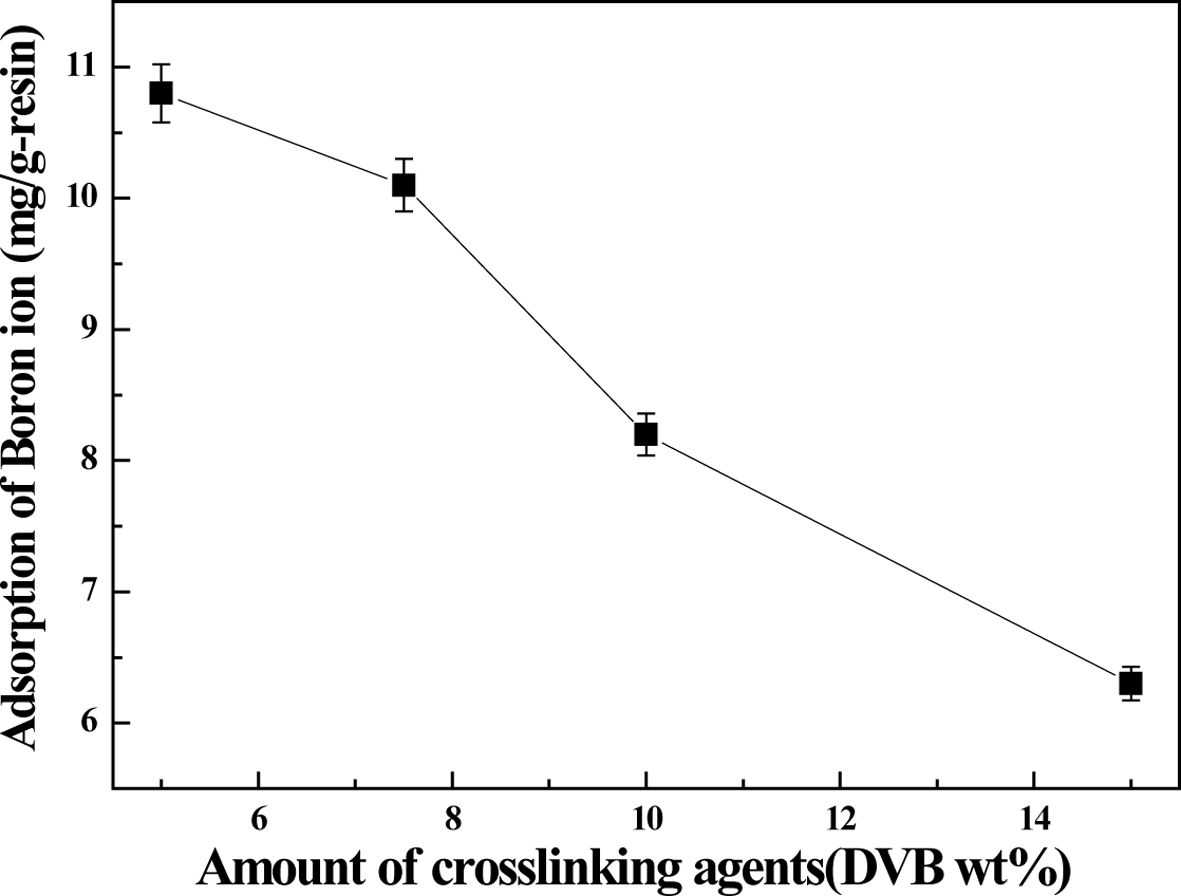
보론 이온 흡착 특성을 조사하여 그 결과를 Figure 5에 나타내었다. 가교제 함량 15.0 및 10.0 wt%로 합성한 poly(St-co-DVB)
가교수지 기반 킬레이트 수지는 총 흡착용량이 각각 6.3 및 8.2 mg/g-resin으로 낮게 나타났다. 이는 보론 이온 흡착 특성을 발현할 수 있는 관능기의 함량이 낮았기
때문인 것으로 판단되었다. 반면에, 가교제 함량 7.5 및 5.0 wt%로 합성한 poly(St-co-DVB) 가교수지 기반 킬레이트 수지는 총 흡착용량이 각각
10.1 및 10.8 mg/g-resin로 높게 나타났다. 이는 가교도가 상대적으로
낮아 팽윤도가 높아진 상태에서 관능기 도입 시 적절한 혼합용매를 사용하여 보론 이온 흡착 특성을 발현할 수 있는 글루카민기 도입 효율을 향상시킬
수 있었고 결과적으로 보론 이온 흡착 특성의 관능기 함량이 증가하였기 때문인 것으로 판단되었다.
또한 아미노알코올과
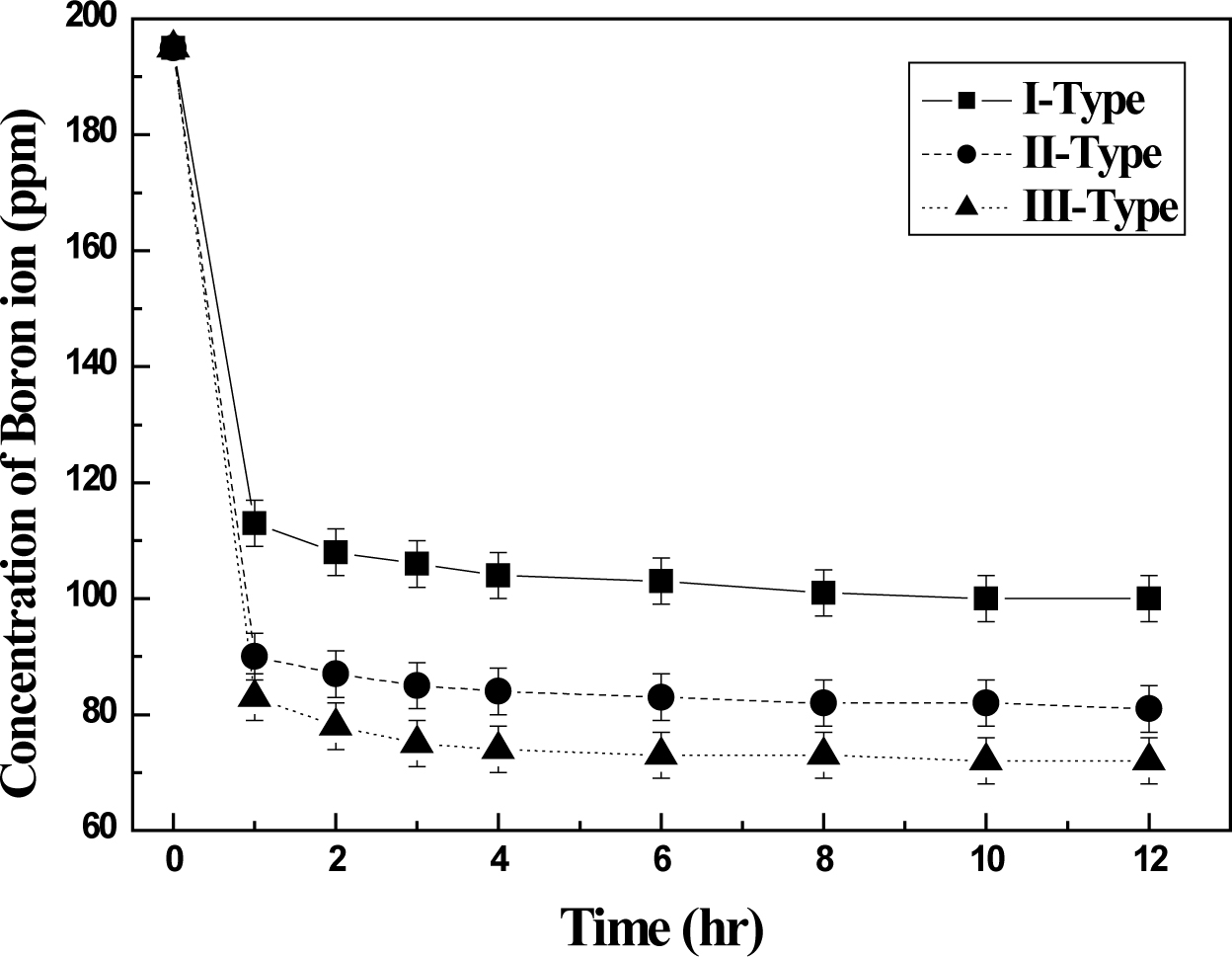
같은 저분자량 작용기의 도입 유무 및 관능기 구조에 따른 킬레이트 수지의 보론 흡착 특성을 조사하여 그 결과를 Figure 6에 나타내었다.
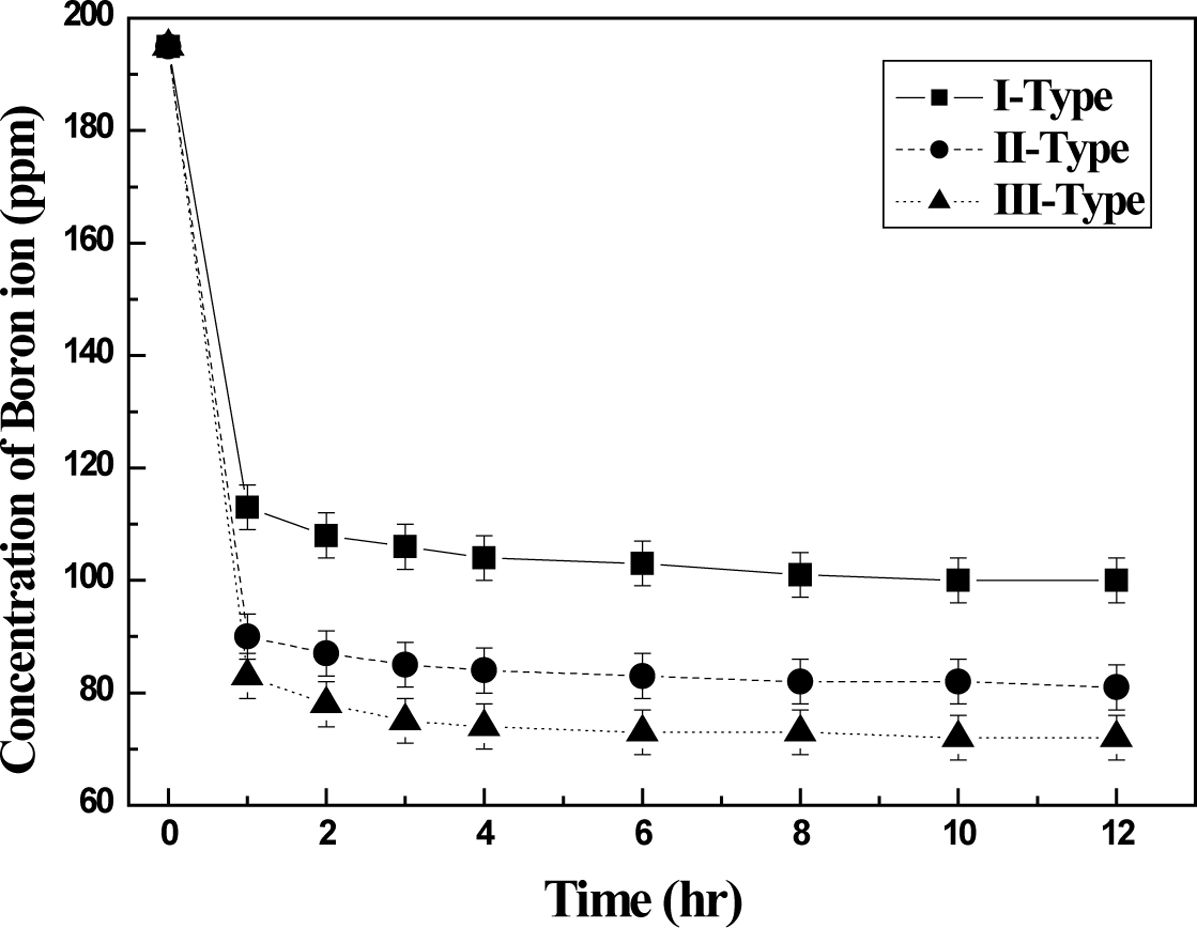
Figure 6에 나타낸 바와 같이, 관능기로 글루카민기만 존재하는 Type-I에 비해 글루카민기 도입 이후 추가로 아미노알코올기가
도입된 Type-II 및 Type-III의 보론 이온 흡착량이 현저히 증가했음을 확인하였다. 이는 킬레이트 수지 내 아미노알코올기의
추가 도입으로 인하여 보론 이온과 관능기 사이의 접촉이 보다 효율적으로 발생한 결과로 판단하였다. 아미노알코올기가 추가로 도입된 킬레이트 수지에
있어서 MEA 아미노알코올기가 도입된 Type-III가 DEA 아미노알코올기가 도입된 Type-II보다 보론 이온 흡착량이 더 높게 나타났다. 이는 글루카민기
도입 반응 이후 남아있는 잔류 염화메틸기에 대한 치환반응에서 입체장애가 낮은 MEA 구조가 더 유리하였기 때문인 것으로 판단되었다.
또한 Type-I, Type-II 및 Type-III 킬레이트 수지에서
대부분의 보론 이온이 약 1시간
이내에 모두 흡착되었다. 하지만, Type-I에 비하여 아미노알코올기가 도입되었던 Type-II 및 Type-III 킬레이트 수지가 더
빠른 보론 이온 흡착속도를 나타내었다. 결과적으로 아미노알코올기와 같은 관능기를 추가로 도입했을 때 보론 이온을 보다 더 빠르게 많은 양을 흡착하여
흡착제로서의 흡착효율을 향상시키는 것이 확인되었다.
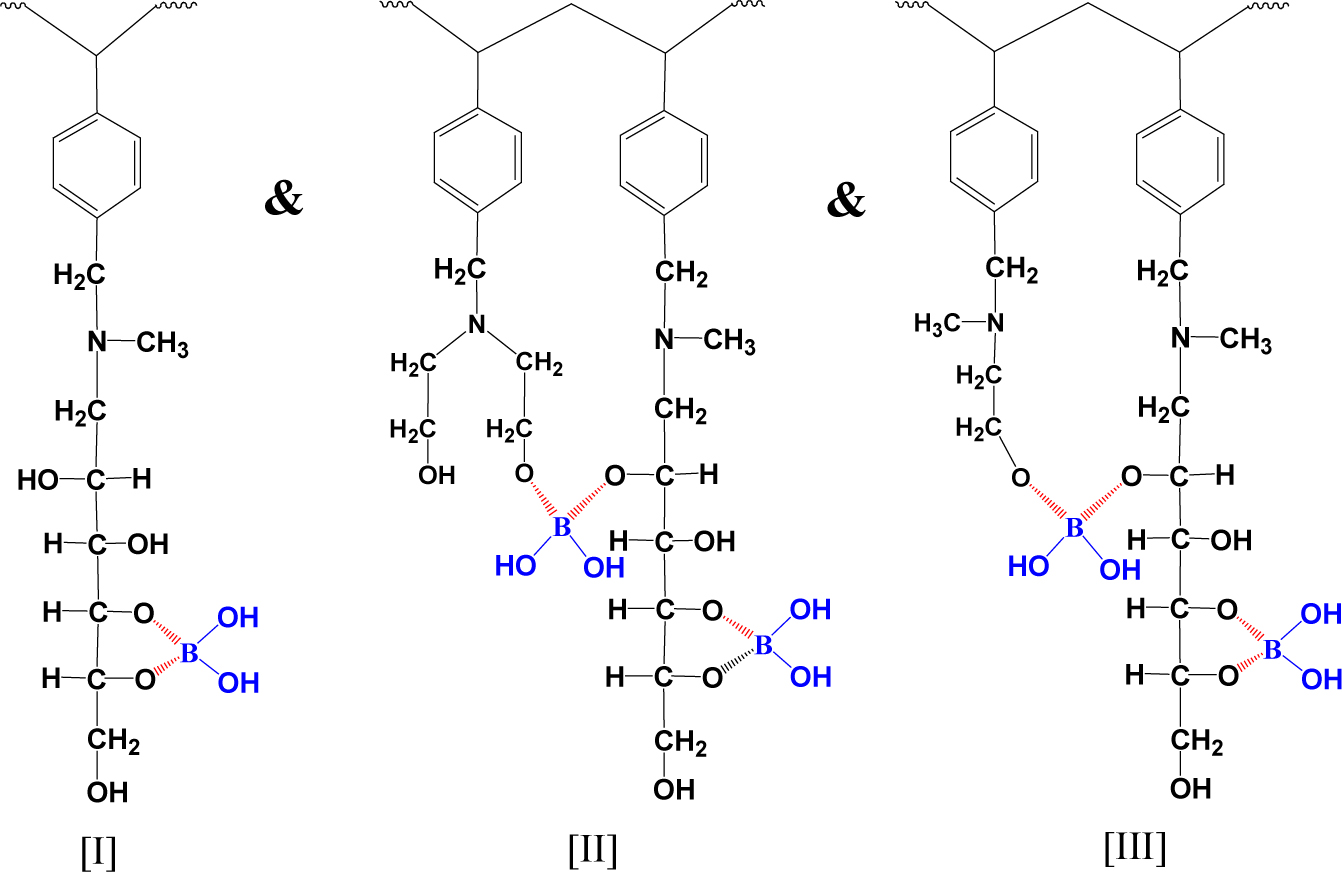
합성된 다양한 킬레이트
수지들은 배위결합을 하려는 보론 이온과 배위자 역할을 하는 글루카민 사이의 배위결합 형성으로 보론 이온에 대한 선택적 흡착이 이루어지는 것으로
알려져 있다. 이러한 배위 착물의 안정성은 사용되는 diol 구조의 유형에 따라 달라지는데 이를 도식적으로 Figure 7에 나타내었다.
합성된 킬레이트 수지의
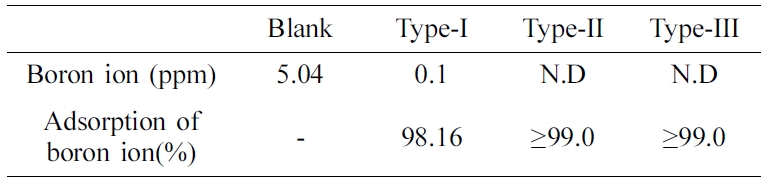
최대 흡착능력을 비교하기 위하여 일부러 고농도의 보론 이온(200 ppm)을 사용하여 흡착실험을 진행하였지만 실제 해수 중에는 3~7 ppm 정도의 보론 이온이 함유되어 있다. 따라서 실제
조건에 부합되는 보론 이온 농도의 용액(5.04 ppm, 20 mL)에 합성된 각각의 킬레이트 수지를 0.2 g씩 넣고 약 12시간 동안 흡착평형에 도달하도록 한
후 보론 이온 용액 여액을 취하여 ICP 분석을 하여 보론 이온 농도 및 흡착률을 측정하여 Table 6에 나타내었다. 실제로 해수 또는 일반수에
포함되어 있는 저농도의 보론 이온에 대한 흡착 실험 결과 합성된 킬레이트 수지 모두 국내 음용수 규정(1.0 ppm 이하) 및 국제보건기구(WHO) 권고 기준인
0.5 ppm을 충분히 만족시키는 것을 확인하였다.
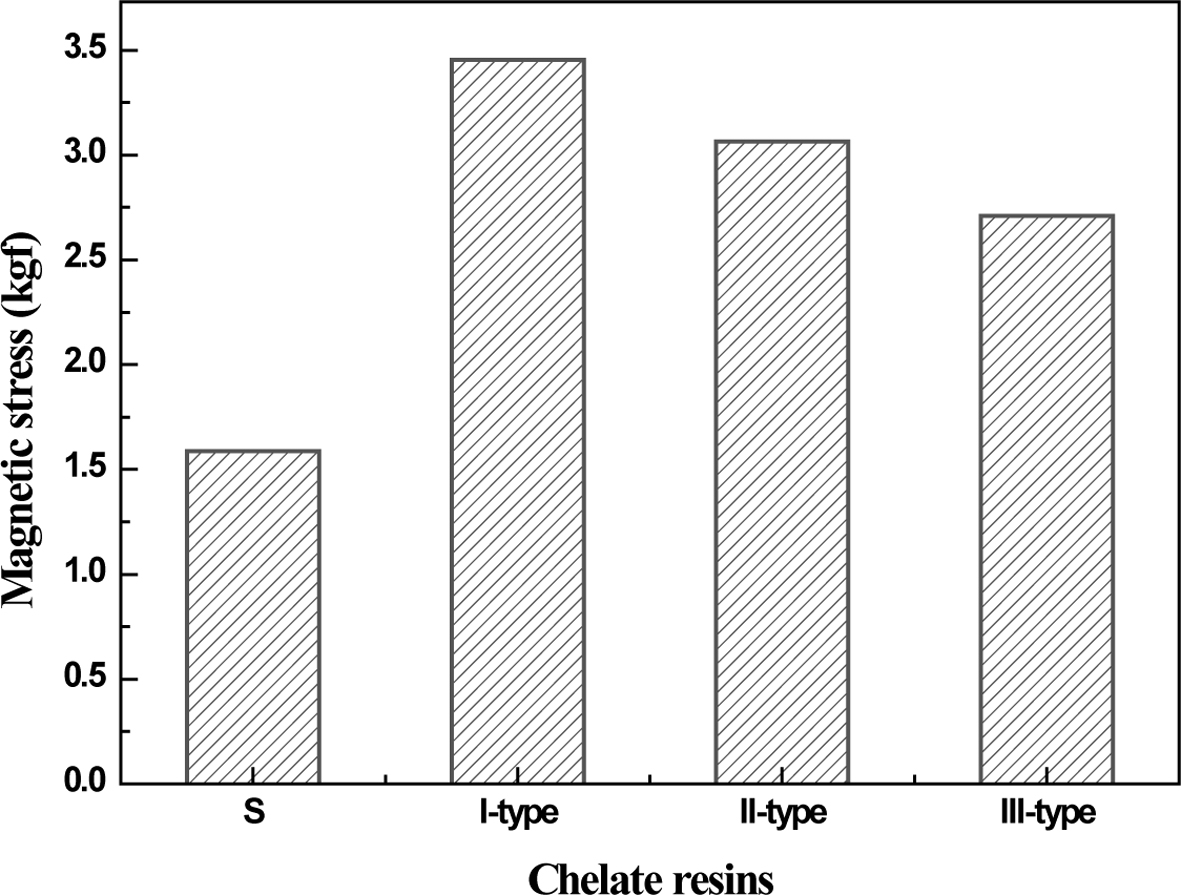
킬레이트 수지의 기계적 강도. 합성된 보론흡착용 킬레이트 수지의 기계적 강도 변화를
확인하기 위해서 관련 산업계에서 주로 사용하는 push-pull gauge를 사용하여 압착에 의해 구상의 수지가 파괴되는 강도를 측정하였고 그
결과를 Figure 8에 나타내었다. 각 단계별 반응이 진행됨에 따라 poly(St-co-DVB) 킬레이트 수지의 기계적 강도가 변화되기는
하였지만 산업적으로 널리 적용되고 있는 흡착용 수지시료(CRB03)에 비하여 합성된 킬레이트 수지 모두 월등히 우수한 기계적 강도를 유지하였다.
|
Figure 2 Variation of (a) surface area; (b) intrusion volume of poly(St-co-DVB) chelate resins depending on crosslinking agent content. |
|
Figure 3 IR spectra of (a) poly(St-co-DVB); (b) chloromethylated poly(St-co-DVB); (c) glucamine-containing poly(St-co-DVB); (d) DEA-glucamine-containing poly(St-co-DVB); (e) MEA-glucaminecontaining poly(St-co-DVB). |
|
Figure 4 Solid state 13C NMR spectra of (a) poly(St-co-DVB); (b) chloromethylated poly(St-co-DVB); (c) glucamine-containing poly (St-co-DVB); (d) DEA-glucamine-containing poly(St-co-DVB); (e) MEA-glucamine-containing poly(St-co-DVB). |
|
Figure 5 Boron ion adsorption characteristics of poly(St-co-DVB) chelate resin depending on crosslinking agent content. |
|
Figure 6 Boron ion adsorption characteristics of various poly(Stco-DVB) chelate resins. |
|
Figure 7 Schematic presentation of coordination complex forming between boron ion and various chelate resins (Type I, II, and III). |
|
Figure 8 Variations in magnetic stress of commercial sample (CRB03), glucamine-containing chelate resin (Type-Ⅰ), DEA-glucamine-containing chelate resin (Type-Ⅱ), and MEA-glucaminecontaining chelate resin (Type-Ⅲ). |
|
Table 6 Boron Ion Adsorption Characteristics of Various Poly(St-co-DVB) Chelate Resins |
가교제 함량을 단량체
총량 대비 5.0, 7.5, 10.0 및 15.0 wt%로 변화시키며 poly(St-co-DVB) 가교수지를 합성하였다. 이러한 기본 가교수지에
대해 염화메틸화 반응과 글루카민 도입반응을 혼합용매 및 상분리 방지용 상용화 용매의 혼합 상태에서 반응시킴으로써 반응단계를 간소화하고 반응효율성을
향상시킨 새로운 합성방법을 개발하였다.
이러한 방법을 적용하고 분자설계에 기반한 단계별 반응을 통하여 보론 흡착용 킬레이트 수지를 합성하였다. 이러한 보론 흡착용 킬레이트 수지의 합성방법은
흡착 대상인 보론에 대해 킬레이트 결합을 하는 관능기를 가교수지의 내부에 효과적으로 도입할 수 있어 가교수지의 기계적 물성 및 다공성 구조를 유지하면서
보론 흡착능력을 현저히 향상시키는 우수한 효과를 나타내었다. 또한 아미노알코올기의 추가 도입 반응을 통하여 보론 흡착용 킬레이트 수지 내에 미치환된
염화메틸기를 최소화할 뿐만 아니라 킬레이트 수지 내의 하이드록시기 함량이 증가하게 되어 보론 이온 흡착 특성을 효과적으로 향상시킬 수 있었다.
- 1. I. S. Kim and B. S. Oh, J. KSEE, 30, 1197 (2008).
-

- 2. A. Bick and G. Oron, Desalination, 178, 233 (2005).
-

- 3. J. Wolska and M. Bryiak, Desalination, 310, 18 (2013).
-

- 4. A. A. Oladipo and M. Gazi, React. Func. Polym., 190, 23 (2016).
-

- 5. Z. Guan, J. Lv, P. Bai, and X. Guo, Desalination, 383, 29 (2016).
-

- 6. Guidlines for Drinking-Water Quality, Fourth Edition, WHO, Geneva (2011).
- 7. N. Hilal, G. T. Kim, and C. Somerfield, Desalination, 273, 23 (2011).
-

- 8. L. Wang, T. Qi, Z. Gao, Y. Zhang, and J. Chu, React. Funct. Polym., 67, 202 (2007).
-

- 9. M. Busch, C. Marston, and C. Prabakaran, Proceedings of European Desaliantion Society Conference on Desalination and Environment, Santa Margherita, Italy, May 2005.
- 10. D. Kavak, J. Hazard. Mater., 163, 308 (2009).
-

- 11. M. O. Simonnot, C. Christophe, N. Miguel, R. Christophe, M. Sardine, and H. Jauffret, Water Res., 34, 109 (2000).
-

- 12. N. Kabay, S. Sarp, M. Yuksel, Ö. Arar, and M. Bryjak, React. Funct. Polym., 67, 1643 (2007).
-

- 13. S. Jung and M. J. Kim, JKIRR, 25, 3 (2016).
- 14. C. Yan , W. Yi, P. Ma, X. Deng, and F. Li, J. Hazard. Mater., 154, 564 (2008).
-

- 15. N. Kabay, S. Sarp, M. Yuksel, M. Kitis, H. Koseoğlu, Ö. Arar, M. Bryjak, and R. Semiat, Desalination, 223, 49 (2008).
-

- 16. S. H. Cho and K. C. Kim, J. KSEE, 18, 333 (1996).
-

- 17. T. S. Hwang, J. H. Lee, and M. J. Lee, Polym. Korea, 25, 451 (2001).
- 18. I. H. Park, Y. K. Bang, K. M. Kim, and H. J. Joo, Polym. Korea, 27, 330 (2003).
- 19. B. Y. Jung, S. H. Kang, J. C. Lee, and T. S. Hwang, Polym. Korea, 30, 45 (2006).
- 20. Y. K. Bang, C. H. Pack, T. J. Lee, Y. J. Choi, and H. I. Kim, Polym. Korea, 42, 409 (2018).
-

- 21. S. Savaskan, N. Besirli, and B. Hazer, J. Appl. Polym. Sci., 59, 1515 (1996).
-

- 22. I. C. Poinescu and C. D. Vlad, Eur. Polym. J., 33, 1515 (1997).
-

- 23. J. H. Mohr, R. Swart, and C. G. Huber, Anal. Bioanal. Chem., 400, 2391 (2011).
-

- 24. S. Samatya, N. Kabay, and A. Tuncel, J. Appl. Polym. Sci., 126, 1475 (2012).
-

- Polymer(Korea) 폴리머
- Frequency : Bimonthly(odd)
ISSN 0379-153X(Print)
ISSN 2234-8077(Online)
Abbr. Polym. Korea - 2023 Impact Factor : 0.4
- Indexed in SCIE
 This Article
This Article
-
2020; 44(3): 334-341
Published online May 25, 2020
- 10.7317/pk.2020.44.3.334
- Received on Jan 29, 2020
- Revised on Feb 27, 2020
- Accepted on Mar 3, 2020
 Services
Services
Shared
 Correspondence to
Correspondence to
- Hyung-Il Kim
-
Department of Industrial Chemistry, Chungnam National University, Daejeon 34134, Korea
- E-mail: hikim@cnu.ac.kr
- ORCID:
0000-0001-6975-1126









 Copyright(c) The Polymer Society of Korea. All right reserved.
Copyright(c) The Polymer Society of Korea. All right reserved.