- Evaluation of the NOx Gas Adsorption Removal of the Amine-modified Vinylbenzyl Chloride-Styrene-Divinylbenzene Terpolymer by XPS Analysis
Gayeong Yun*, Kwon Mo Koo*, Dong Yeob Lee*, and Yangsoo Kim*,**,†

*Department of Nanoscience & Engineering, Inje University, Gimhae 50834, Korea
**High Safety Vehicle Core Technology Research Center, Inje University, Gimhae 50834, Korea- XPS 분석을 활용한 아민으로 개질된 Vinylbenzyl Chloride-Styrene-Divinylbenzene 삼원 공중합체의 NOx 가스 흡착 제거 평가
*인제대학교 나노융합공학부, **인제대학교 고안전차량핵심기술연구소
Nitrogen oxide (NOx)
is one of the highly toxic acid gases. In this study, EDA-VBC-S-DVB compound,
which is an amine modified terpolymer, was used as a NOx gas
adsorption removing material and it was prepared by changing the amount of
crosslinking agent in order to evaluate the NOx gas adsorption
capacity. Adsorption experiment was carried out with the variation of
adsorption time and NOx gas supply capacity. The NOx gas
adsorption capacity was quantitatively estimated by the application of XPS
analysis and it increased with the amount of crosslinking agent and the NOx
gas supply capacity. EDA-VBC-S-DVB compound prepared in this study showed 12.96
mL·h for the critical point of the NOx gas supply capacity, 1.2182
mmol/g for the maximum value of the NOx gas adsorption capacity, and
392% for the maximum value of the NOx gas relative adsorption
capacity
NOx 가스는 발생원이 다양하며 높은 독성을 갖는 산성가스 중 하나이다. 본
연구에서는 삼원 공중합체에 아민그룹을 개질시킨 EDA-VBC-S-DVB를 NOx 가스 흡착 제거 물질로 사용하였으며 가교반응에 따른 흡착성능을 비교분석하기 위해 가교제
첨가량을 변화시키면서 제조하였다. NOx 가스 공급용량을 변화시키며 흡착실험을 수행하였으며 XPS 정량분석을 통해 EDA-VBC-S-DVB의 NOx 가스 흡착용량을 평가하였다. 가교제 첨가량과 NOx 가스 공급용량에 따라 NOx 가스
흡착용량이 증가하였으며 본 연구에서 제조한 EDA-VBC-S-DVB의 경우 NOx 가스 공급용량 임계치는 12.96 mL·h, NOx 가스 흡착용량 최대치는 1.2182 mmol/g,
NOx 가스 상대 흡착용량은 392%를 보여주었다
The amine-modified
terpolymer was used as a NOx gas adsorption removing material. The
NOx gas adsorption capacity was quantitatively estimated by the
application of x-ray photoelectron spectroscopy analysis and it increased with
adsorption time and NOx gas supply capacity. The amine-modified terpolymer showed 12.96
mL¡¤h for the critical point of the NOx gas supply capacity, 1.21 mmol-NO gas/g-adsorbent for the
maximum value of the NOx gas adsorption capacity, and 392% for the
maximum value of the NOx gas relative adsorption capacity.
Keywords: XPS analysis, NOx gas, adsorption removal, vinylbenzyl chloride-styrene-divinylbenzene terpolymer
본 연구는
2017년도 중소벤처기업부의 기술개발사업(과제번호 S2489015) 지원에 의한 연구임.
최근 세계적으로 산업화
및 도시화가 진행되면서 CO2, SOx, NOx 등의 산성 가스에 의한 환경문제 해결이 중요하게
논의되고 있다. 산성 가스는 대기, 토양, 해양 등 자연 환경에 매우 폭넓은 범위에 걸쳐 심각한 오염을 초래하고 있으며 이를 방지하기 위한 수많은
연구 노력이 이루어지고 있다. 특히 질소산화물 NOx 가스는 화석연료의 연소 과정과 디젤 엔진 자동차 배기가스 등에서 발생하며
광화학 스모그, 산성비, 미세먼지, 지표면 오존 등을 유발시킴으로써 대기환경 문제의 핵심 원인으로 알려져 있다. 또한 질소산화물은 인체에 해로운
영향을 끼치며 주로 폐 및 호흡기 질환의 원인으로 작용하기 때문에 이를 친환경적 방법을 통하여 선택적으로 제거하는 것이 필요하며 이를 위한 다양한
재료 개발도 요구된다.
일반적으로 NOx
가스를 제거하기 위한 대표적인 방법으로써 선택적 촉매 환원(selective catalytic reduction, SCR)에 대한 연구가 이루어져
왔다. SCR 방법은 암모니아, 요소 등의 환원 촉매를 이용하여 NOx 가스를 질소(N2)와 수증기(H2O)로
환원시키는 방법이다. SCR 방법은 높은 NOx 가스 제거효율을 나타내지만 효과적으로 NOx 가스를 제거하기
위하여 200 oC 정도의 고온이 요구되며,1,2 설비의 관리 및 유지에 소홀할 경우 쉽게 오염되어 사용이 어렵다는 단점을 갖고 있다. SCR 방법 이외에도 활성탄, 다공성 실리카, 금속-유기
구조체(metal-organic framework, MOF) 등이 NOx 가스 흡착 제거에 우수한 성능을 가진 재료로 알려져
있다.3-7 활성탄은 탄소질의 다공성 재료로써 높은 표면적을 가지며
기본적으로 활성탄의 표면에서 van der Waals 힘에 의해 물리적으로 흡착반응이 일어나며, 또한 금속산화물을 활성탄에 함침시켜 활성탄 표면을
개질시킴으로써 NOx 가스 흡착 제거 성능을 향상시키는 연구가 보고되었다.3,4 그러나 이들은 열 및 수분에
대한 안정성이 낮기 때문에 산업환경에서 흡착제로써 적용하기에 어려움이 있다. 다공성 실리카 또한 NOx 가스 흡착 제거 성능을
개선시키기 위하여 습식 함침법 또는 실란 커플링제를 이용하여 아민(amine) 기능성 그룹을 실리카 표면에 도입하는 연구들이 보고되었다.5
NOx 가스를 흡착 제거하기 위한 다양한 연구 중에서 NOx 가스 흡착 물질로써 고분자 재료를
응용하는 연구보고들이 주목받고 있다.8-10 고분자 재료는 친환경적이고 빠른 제조가 가능하며 산업
환경에 적용될 때 상대적으로 안정하고 재활용이 가능할 뿐만 아니라 낮은 밀도이면서 가공이 쉽다는 장점을 갖고 있다. 특히 가교된 고분자 재료를
이용할 경우 그들의 다공성 표면과 높은 표면적으로 인해 흡착 용량과 흡착 속도를 최대화하는 것이 가능하다고 알려져 있다. Diaf 등은8,9
다양한 아민 화합물을 사용하여 개질 처리된 선형 및 가교 고분자를 제조하여 이들을 대상으로 NOx 등의 유해성 산성 가스 흡착
성능을 thermogra-vimetric analyzer(TGA)를 사용하여 분석하였다. 또한 Vinodh 등은10
세가지 종류의 과가교된 다공성 고분자를 제조하여 NOx 가스 흡착 물질로 사용하였으며 고압 TGA를 가스 흡착 라인에 설치하여
흡착 성능을 분석하였다.본 연구에서는
Diaf 등의8 연구를 바탕으로 하여 자유라디칼 중합 공정을 통해 가교된 vinylbenzyl
chloride-styrene-divinylbenzene(VBC-S-DVB) 삼원 공중합체를 제조하였으며 이를 NOx 가스
흡착 제거용 소재로써 사용하였다. 공중합체의 NOx 가스에 대한 선택적 흡착 능력을 향상시키기 위하여 ethylenediamine(EDA)를 사용하여
아민 그룹을 공중합체에 도입한 EDA-VBC-S-DVB 화합물을 Figure 1과 같이 제조하였으며, 또한 NOx 가스 흡착용량을
최대화시킬 수 있는 방안으로 가교제로 사용된 DVB의 첨가량 변화를 시도하였다. EDA-VBC-S-DVB 화합물을 사용한 NOx 가스
흡착 제거 실험은 Figure 2와 같이 특수 제작된 아크릴 챔버 내에서 NOx 가스 흡착 조건을 변화시키면서 수행하였다.
X-ray photo-electron spectroscopy(XPS)를 사용하여 흡착 전 및 흡착 후 시료의 스펙트럼 피크 분석을 수행함으로써 흡착용량을
정량화하는데 성공하였다.
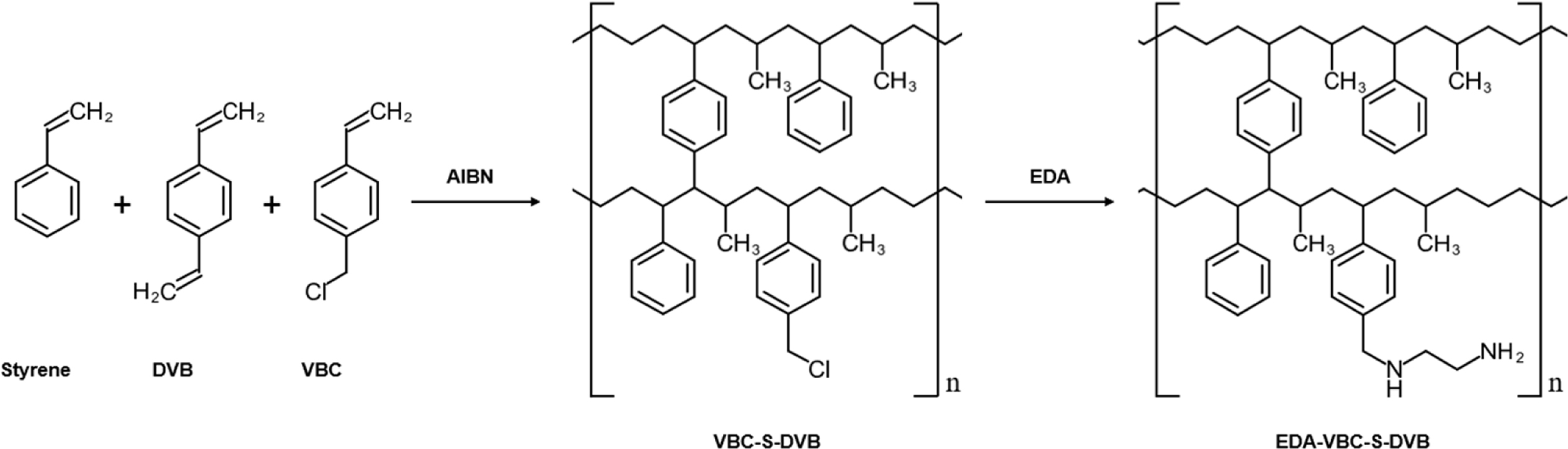
|
Figure 1 Preparation flow of VBC-S-DVB and EDA-VBC-S-DVB.8 |
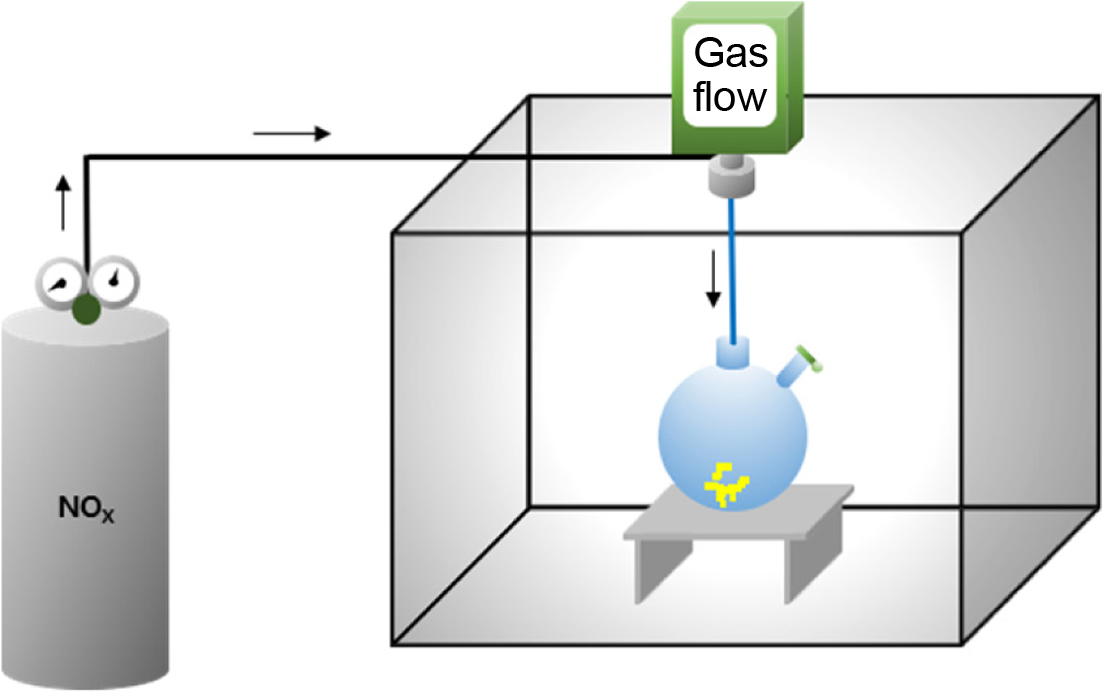
|
Figure 2 Gas chamber for NOx gas adsorption test. |
재료. 본 연구에서는 styrene(≥99%, Aldrich), 4-vinylbenzyl chloride(VBC, ≥90%, Aldrich),
divinylbenzene(DVB, ≥90%, Aldrich), a,a'-azobisisobutyronitrile(AIBN,
≥99%, Junsei), ethylenediamine(EDA, ≥99%, Aldrich) 등을 사용하였으며,
toluene을 용매로 사용하였다.
Styrene, DVB, VBC 등은 사용하기 전에 inhibitor remover column을 사용하여 정제하였으며, AIBN, EDA는 별도의 정제 과정 없이
사용하였다.
VBC-S-DVB
공중합체 제조. VBC-S-DVB 공중합체는 DVB 첨가량 변화에 따라
두 종류(VBC-S-DVB-1 및 VBC-S-DVB-2)를 제조하였다. 공중합체를 제조하기 위하여 반응 플라스크에 VBC 49.7 mmol, styrene 60.5 mmol, toluene 54 mL 등과 DVB 30.33 mmol(VBC-S-DVB-1) 또는 60.66 mmol(VBC-S-DVB-2)를 함께 넣고 교반함으로써
반응용액을 준비하였다. 중합반응 개시제인 AIBN 0.12 mmol을 toluene 5 mL에 용해시킨 혼합용액을 주사기를 사용하여 반응용액이 담긴 반응 플라스크에 주입하였으며, 80 oC에서 2시간 동안 교반한 후 toluene 50 mL를 반응 플라스크에 추가하여 투입하였고 이어서 반응온도는
80 oC로 유지한 상태에서 5시간 동안 연속적으로 반응을 수행하였다. 반응 종료 후 반응 혼합액을 과량의 메탄올이
담긴 비이커에 넣고 강하게 교반하였고 세척 및 여과 작업을 3회에 걸쳐 반복함으로써 백색의 고체 생성물을 회수하였다. 반응 고체 생성물을
100 oC에서 24시간 동안 진공 건조하여 VBC-S-DVB 공중합체를 제조하였다.
EDA-VBC-S-DVB
화합물 제조. VBC-S-DVB 공중합체 1.75 g을 toluene 50 mL에 재분산하여 현탁용액을 준비하였다. EDA 35 mL과 toluene 40 mL를 함께 넣고 교반하여 얻어진 혼합용액이 담긴 둥근
플라스크에 VBC-S-DVB 공중합체 현탁용액을 한 방울씩 천천히 첨가하여 최종적으로 혼합용액을 준비하였다. 혼합용액을 40 oC에서 48시간 동안 교반한 후 이어서 80 oC로 가열하고 4시간 동안 추가하여 교반하였다. 얻어진 반응 생성물을 과량의 증류수가 담긴 비이커에 넣어 강하게
교반하고 세척 및 여과 작업을 3회에 걸쳐 반복함으로써 황색의 고체 생성물을 회수하였으며 100 oC에서 24시간 동안 진공 건조하여 EDA-VBC-S-DVB 화합물을 제조하였다.
NOx 가스 흡착실험. NOx 가스 흡착실험은 상온의 가스
챔버(Figure 2) 내에서 수행하였으며 흡착 대상 NOx 가스로서 1800 ppm의 일산화질소(NO) 가스를 이용하였다.
밸브가 부착된 일정 부피(100 또는 500 mL)의 Schlenk 플라스크에 일정량의 EDA-VBC-S-DVB 화합물 고체시료를 넣고 밸브가 열린 상태에서
NO 가스를 평균 2.0 L/min의 유량으로 10분 동안 주입한 후 밸브를 닫고
밀봉한 상태에서 일정 시간(48 또는 72시간) 동안 유지하였다.
화합물 특성 분석. Fourier-transform infrared
spectroscopy (FTIR) (VARIAN, 640-IR)을 사용하여 화합물들의 화학 구조 분석을 수행하였으며 가교제(DVB) 첨가량 변화에
따른 VBC-S-DVB 삼원 공중합체의 가교밀도를 확인하기 위하여 팽윤 시험(swelling test)을 수행하였다. Field
emission scanning electron microsope(FE-SEM) (HITACHI, S-4300SE)를 사용하여 다공성 고분자의
표면 상태를 확인하였으며, NO 가스 흡착 실험을 종료한 후 EDA-VBC-S-DVB 화합물에 남아 있는 NO 가스에 대한 정성 및 정량 분석을
위하여 X-ray photo-electron spectroscopy(XPS) (Thermo Fisher Scientific, K-ALPHA+
XPS system)을 사용하였다.
Figure 3은
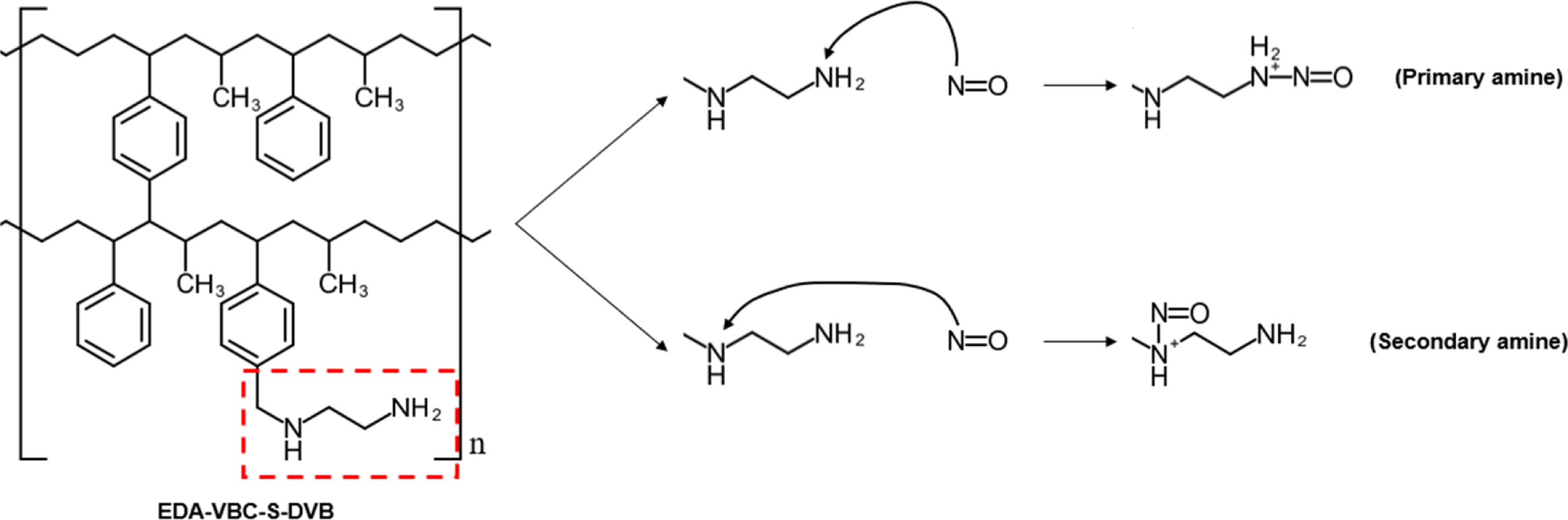
EDA-VBC-S-DVB 화합물의 NO 가스에 대한 화학적 흡착 메커니즘을 보여주고 있다. VBC-S-DVB 화합물에 EDA가 치환되면서 2차
아민이 생성되므로 1차 아민과 2차 아민 두 군데 장소에서 NO 가스의 화학적 흡착 반응이 일어날 수 있다. NO 가스가 1차 및 2차 아민과
반응하면서 아민/NO 화합물이 생성되며,8 이때 NO 가스와 반응한 EDA의 질소 원자는 1차 또는 2차 암모늄 이온의 형태로
전환된다.
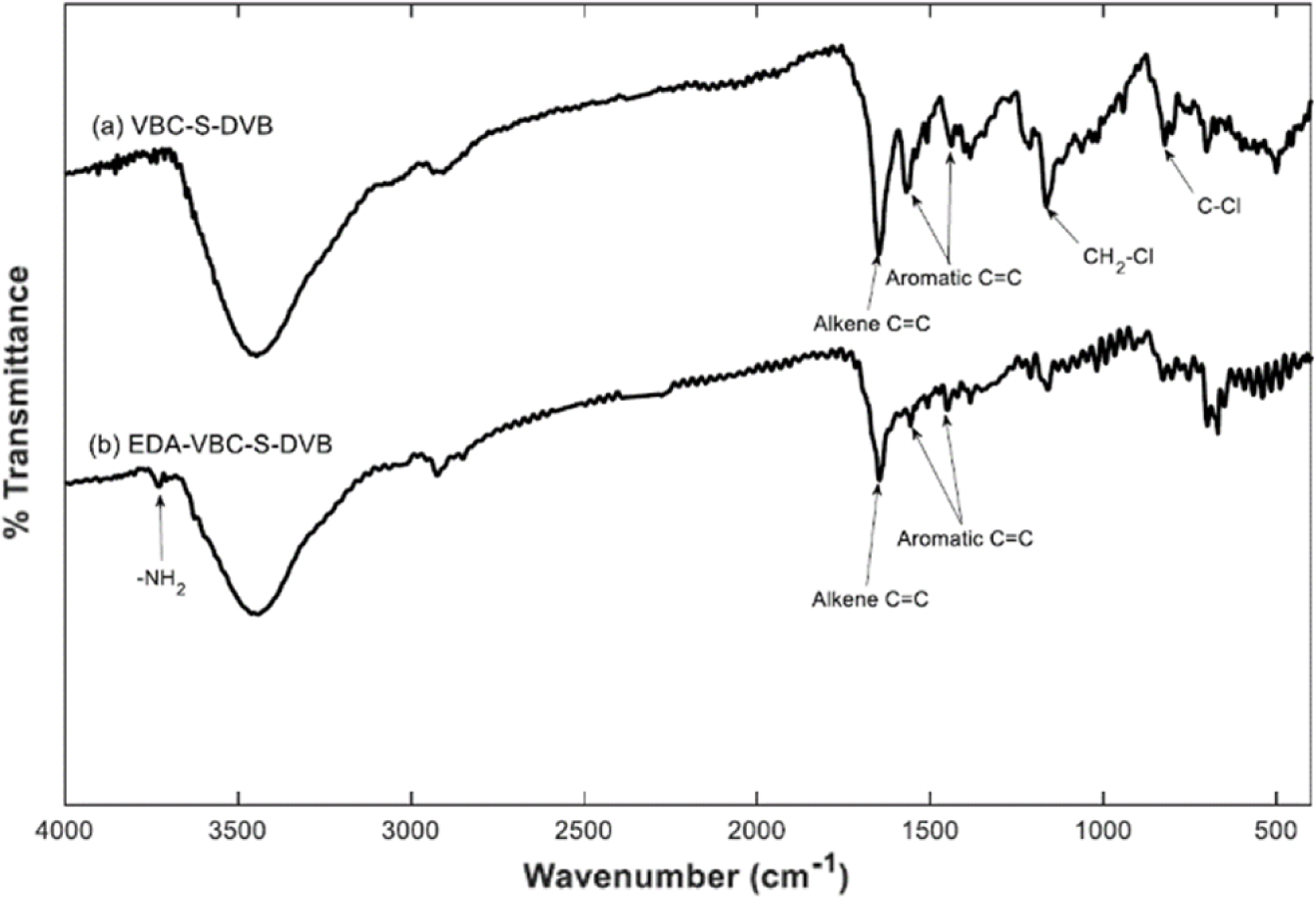
Figure 4는
VBC-S-DVB 공중합체와 EDA-VBC-S-DVB 화합물의 FTIR 스펙트럼이다. VBC-S-DVB 공중합체를 구성하는 세 가지 단량체(VBC,
Styrene, DVB)들은 모두 화학 구조 내에 벤젠 고리 및 alkene C=C 결합을 포함하고 있다. VBC-S-DVB 삼원 공중합체에 대한
FTIR 스펙트럼(Figure 4(a))의 경우 1580 cm-1 및 1450 cm-1에서 벤젠 고리에 의한 두 개의
aromatic C=C 피크와 1645 cm-1에서 alkene C=C 피크들을 보여주고 있으며, 또한 VBC에 포함되어 있는
CH2-Cl 및 C-Cl 그룹이 1160 cm-1와 701 cm-1에서 각각 확인되고 있다.
Alkene C=C 결합은 DVB 내 잔류한 이중결합에 의한 피크로써 DVB 내 두 개의 이중결합(비닐 그룹)은 반응성 차이를 가지며 두 번째
이중결합은 약 50% 정도 반응하지 않고 잔류할 가능성을 가진다고 알려져 있다.8,11 Figure 4(b)는
VBC-S-DVB 삼원 공중합체에 EDA를 사용하여 반응 처리한 EDA-VBC-S-DVB 화합물의 FTIR 스펙트럼이다. VBC-S-DVB에
EDA가 반응 처리될 때 VBC의 말단 -Cl 그룹이 떨어져 나가면서 EDA가 치환되며 EDA-VBC-S-DVB 화합물의 FTIR 스펙트럼에서
CH2-Cl과 C-Cl 피크가 사라지면서 3700 cm-1에서 EDA에 의한 -NH2 비대칭 신축 피크가 나타났으며12
따라서 VBC-S-DVB 공중합체에 EDA가 성공적으로 반응 결합되었다는 것을 확인할 수 있다.
Figure 5는
EDA-VBC-S-DVB-2 화합물의 SEM 이미지를 보여주고 있다. DVB에 의한 가교반응에 의하여 EDA-VBC-S-DVB-2 표면이 다공성을
나타내며 유사한 형태를 가진 1.6~2 μm의 직경을 갖는 많은 기공들이 생성된 것을 확인할 수 있다.13 본 연구에서
DVB는 가교제로 사용되며 DVB 첨가량 증가에 따라 가교밀도가 증가한다. EDA-VBC-S-DVB 화합물의 가교 상태와 NO 가스 흡착 용량의
관계를 확인하기 위하여 팽윤 실험을 수행하였으며 DVB 첨가량 변화에 따른 EDA-VBC-S-DVB 화합물의 팽윤비와 가교밀도를 실험적으로 분석하였다.
팽윤 실험은 용매로써 ethylene glycol을 사용하였으며 어두운 곳에서 48시간 동안 수행하였다. EDA-VBC-S-DVB의 팽윤비를 실험적으로
결정하기 위하여 관계식(식 (1))을 사용하였다.
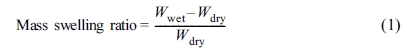
위 관계식에서 Wwet은
팽윤된 시료의 질량이며 Wdry는 팽윤된 시료를 진공 건조한 후 얻어진 시료의 질량이다. DVB의 첨가량을
30.33 mmol(EDA-VBC-S-DVB-1) 및 60.66 mmol (EDA-VBC-S-DVB-2)로 변화시킨 2 종의 시료를
사용하였다.
EDA-VBC-S-DVB-1 시료와 EDA-VBC-S-DVB-2 시료의 팽윤비는 각각 53.07%와 7.67%로 나타났으며 DVB 첨가량을 2배로
증가시킴에 따라 팽윤비가 약 7.5배 감소되었음을 확인할 수 있었다. Flory-Rehner 이론을 바탕으로 시료들의 가교밀도를 계산할 경우,
DVB 첨가량 변화에 따라 2.98× 10-3 mol/cm3(EDA-VBC-S-DVB-1)에서 4.80×10-3 mol/cm3(EDA-VBC-S-DVB-2)로 증가하는 것을 확인하였다.
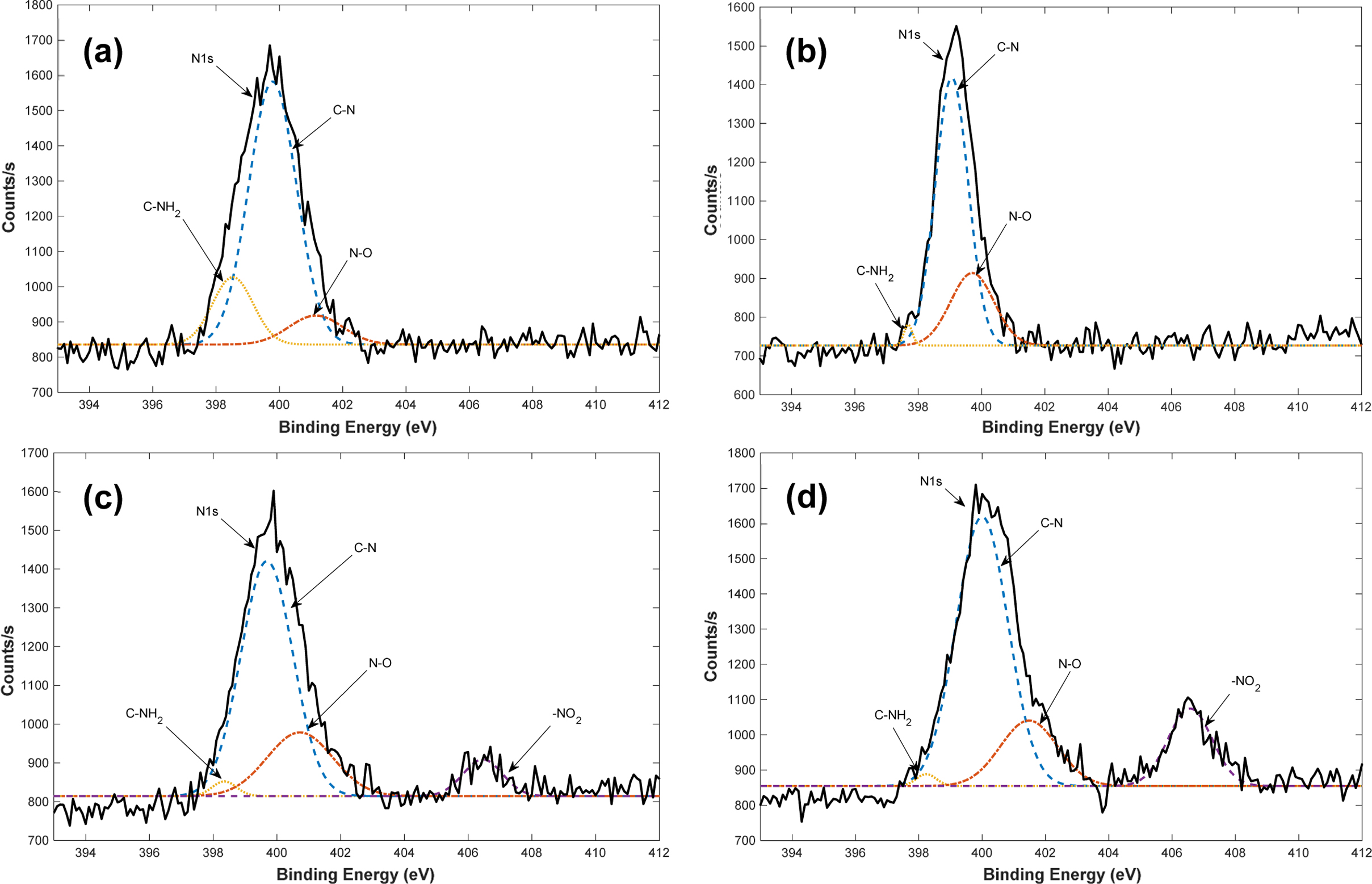
Figure 6은
NO 가스 흡착 조건에 따른 EDA-VBC-S-DVB-1 화합물에 남아 있는 NO 가스의 흡착량 변화를 확인하기 위한 XPS N1s 스펙트럼 분석
결과이다. 흡착 실험은 밀폐된 Schlenk 플라스크에서 수행하였으며 NO 가스 흡착 조건은 플라스크 부피와 흡착 시간을 100 mL-48시간,
100 mL-72시간, 500 mL-48시간 등과 같이 3가지로 변경하였다. Figure 6(a)는 NO 가스를 흡착시키기 전
EDA-VBC-S-DVB-1 시료에 대한 XPS 요소 피크 분석결과이다. C-N 피크는 399.8 eV에서 나타나며 이는 EDA 처리에 따라
VBC-S-DVB 공중합체에 형성된 C-N 그룹에 의한 피크이며, 또한 398.5 eV에서 나타나는 C-NH2 피크도
EDA 처리에 따라 나타난 피크이다.
N-O 피크가
401.1 eV에서 나타나며 이는 시료 보관 과정에서 대기 중 산소에 의한 산화반응으로 인한 피크이다.14 Figure
6(b)는 NO 가스를 100 mL Schlenk 플라스크에 완전히 충전시킨 후
48시간 동안 흡착 실험을 수행한 후 EDA-VBC-S-DVB-1 시료에 대한 XPS 요소 피크 분석결과이다. XPS 스펙트럼에서 나타나는
C-N, C-NH2, N-O 등의 특성 피크들은 Figure 6(a)에서 나타나는 흡착 실험 수행 전 시료와 동일한 위치에서
나타난다. N-O 피크의 경우 흡착 전 시료에 비하여 세기가 증가되었음을 확인할 수 있는데 이는 NO 가스 흡착에 의해 시료 내 N-O 결합이
차지하는 부분이 많아졌기 때문이다. Figure 6(c)는 NO 가스를 100 mL Schlenk 플라스크에 완전히 충전시킨 후
72시간 동안 흡착 실험을
수행한 시료에 대한 XPS 요소 피크 분석결과이다. 흡착 전 시료에 대한 Figure 6(a)와 비교하였을 때 추가적으로 406.4 eV에서 -NO2 피크가 생성되었으며15
이는 흡착 시간이 증가함에 따라
NO 가스의 흡착과 아울러 NO의 산화반응(NO+ 1/2O2®NO2)이 동시에 일어나는데 따른 결과이며 아울러 N-O 피크의
세기가 상당히 증가한 것을 확인할 수 있다. Figure 6(d)는 NO 가스를 500 mL Schlenk 플라스크에 완전히 충전시킨 후
48시간 동안 흡착 실험을 수행한 시료에 대한 XPS 요소 피크 분석결과이다. N-O 피크의 세기가 증가하였고 Figure 6(c)와 같이
-NO2 피크가 나타났으며 NO 가스 흡착 반응과 동시에 일어나는 NO 가스 산화반응이 흡착 시간뿐만 아니라 시료가 노출되는
NO 가스의 공급 부피에도 큰 영향을 미치는 것으로 나타났다.
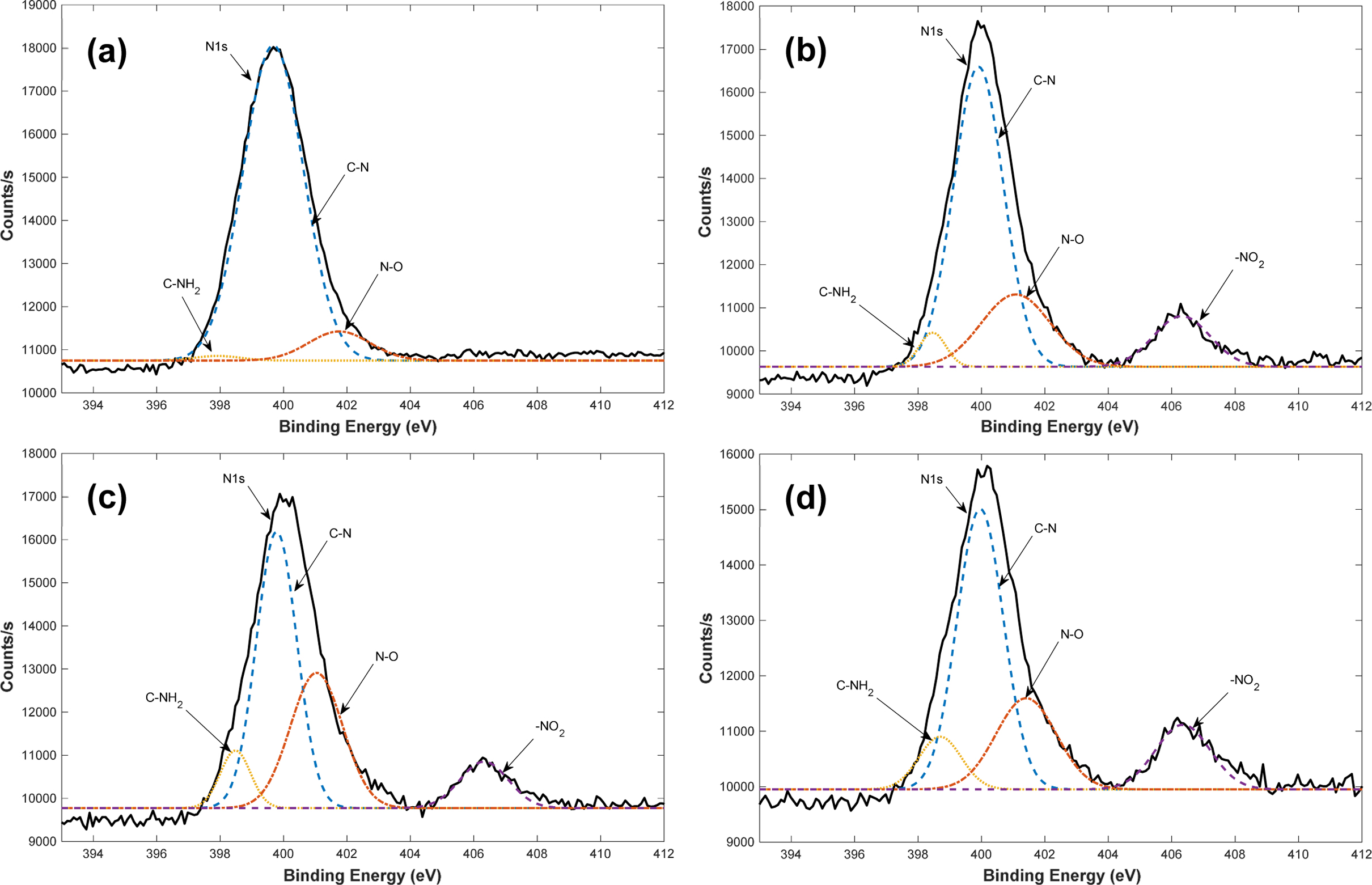
Figure 7은
NO 가스 흡착 조건에 따른 EDA-VBC-S-DVB-2 화합물에 남아 있는 NO 가스의 흡착량 변화를 확인하기 위한 XPS N1s 분석 결과이며,
NO 가스 흡착 조건은 EDA-VBC-S-DVB-1 화합물에 대한 흡착 실험과 동일하게 변경하였다. XPS 스펙트럼에서 나타나는 C-N, C-NH2,
N-O 및 -NO2 등의 특성 피크들은 EDA-VBC-S-DVB-1 화합물에 대한 분석결과인 Figure 6과 동일한 위치에서 나타났으며 각 특성 피크의
세기가 변화하는 것을 확인하였다. Figure 7(a)~(d) 모두에서 399.9 eV 부근의 C-N 피크가 가장 넓은 부분을 차지하고 있으며 NO 가스 흡착에 따른 결과인
N-O와 -NO2 피크 역시 상당히 넓은 면적을 차지하고 있음을 보여주었다. 가교제로 사용된 DVB의 첨가량 증가에 따라 나타나는
N-O와 -NO2
피크들을 비교하였을 때(즉, Figure 6과 Figure 7 비교), 가교제 첨가량이 증가함에 따라 모든 NO 가스 흡착 조건에서 피크의 세기 및 면적이 증가하는 것을 확인할
수 있었다.
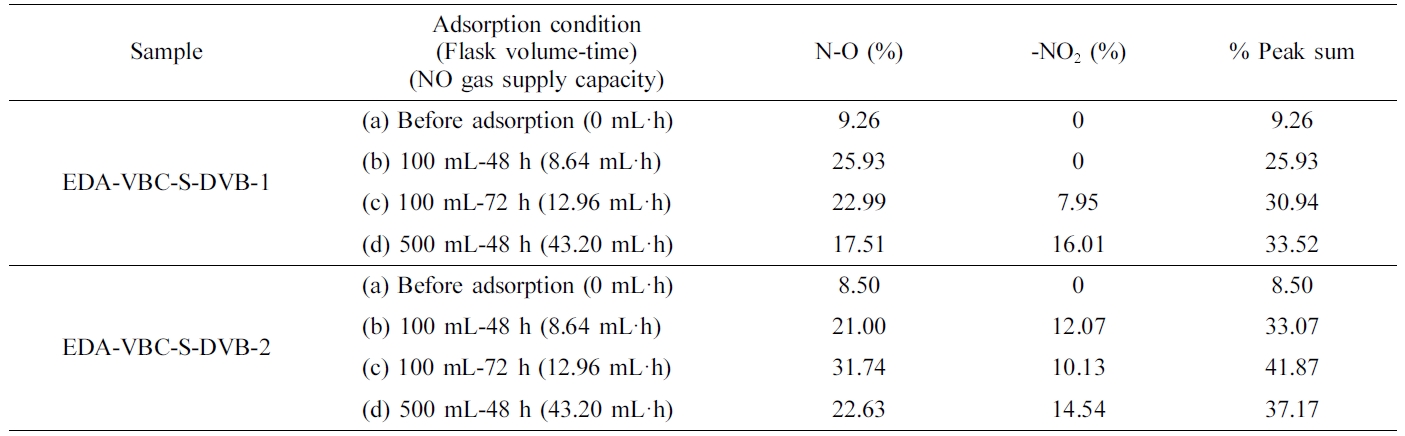
Table 1은
Figure 6 및 Figure 7의 XPS 분석을 바탕으로 각 요소 피크를 분석하여 얻어진 N-O 피크와 -NO2 피크의
면적(%) 수치이다. 흡착 조건이 변화함에 따라 특성 피크들의 면적이 달라지는 것을 확인하였으며 % peak sum 수치는 N-O와 -NO2
피크의 면적(%)의 합을 나타낸다. EDA-VBC-S-DVB-1 시료에 비하여 EDA-VBC-S-DVB-2 시료에 대한 수치가 수행한 모든 흡착
조건에서 증가하였으며 이는 가교밀도가 증가됨에 따라 NO 가스 흡착 성능이 향상된다는 것을 의미한다.
본 연구에서는
NO 가스 흡착 공정의 변수로써 특정 부피의 Schlenk 플라스크에 채워진 NO 가스(1800 ppm)의 실제 공급 부피, 흡착 시간 2개의
변수를 선정하였으며 이들 두 변수를 곱하여 얻은 수치를 EDA-VBC-S-DVB 시료에 노출된 NO 가스의 공급용량(mL·h)으로 정의하였다.
XPS 피크 분석을 수행하여 얻은 면적(%) 수치를 이용하여 흡착된 NO 가스의 몰 수를 계산하였으며, 관계식(식 (2))을 통하여 NO 가스 흡착용량(mmol/g)을
도출하였다. Adsorbed NO gas는 흡착된 NO 가스의 몰 수(mmol)이며, madsorbent은 흡착실험에 사용한 시료의 질량(g)이다. 실험에 사용한
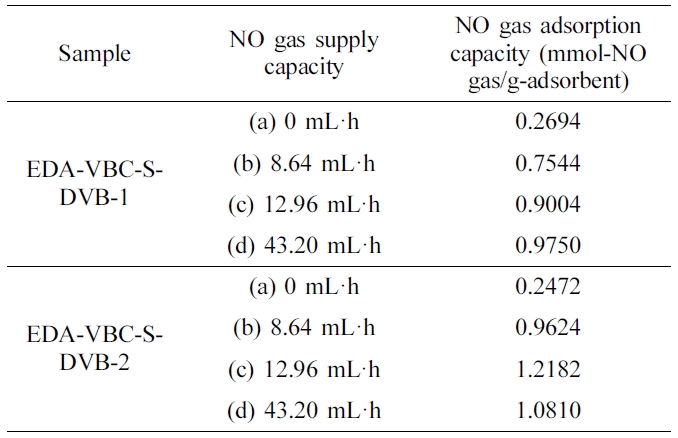
모든 흡착조건에 대한 NO 가스 흡착용량을 Table 2에 나타내었다.
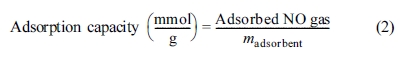
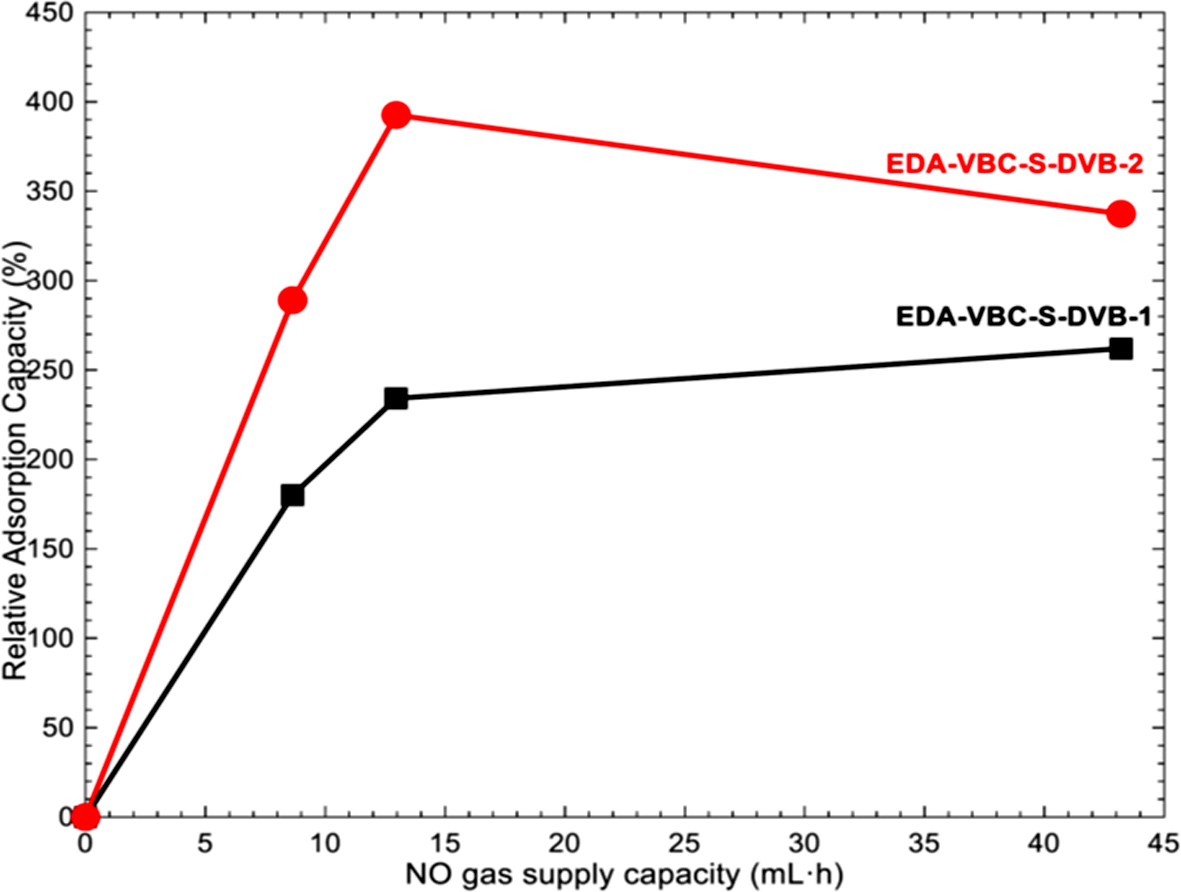
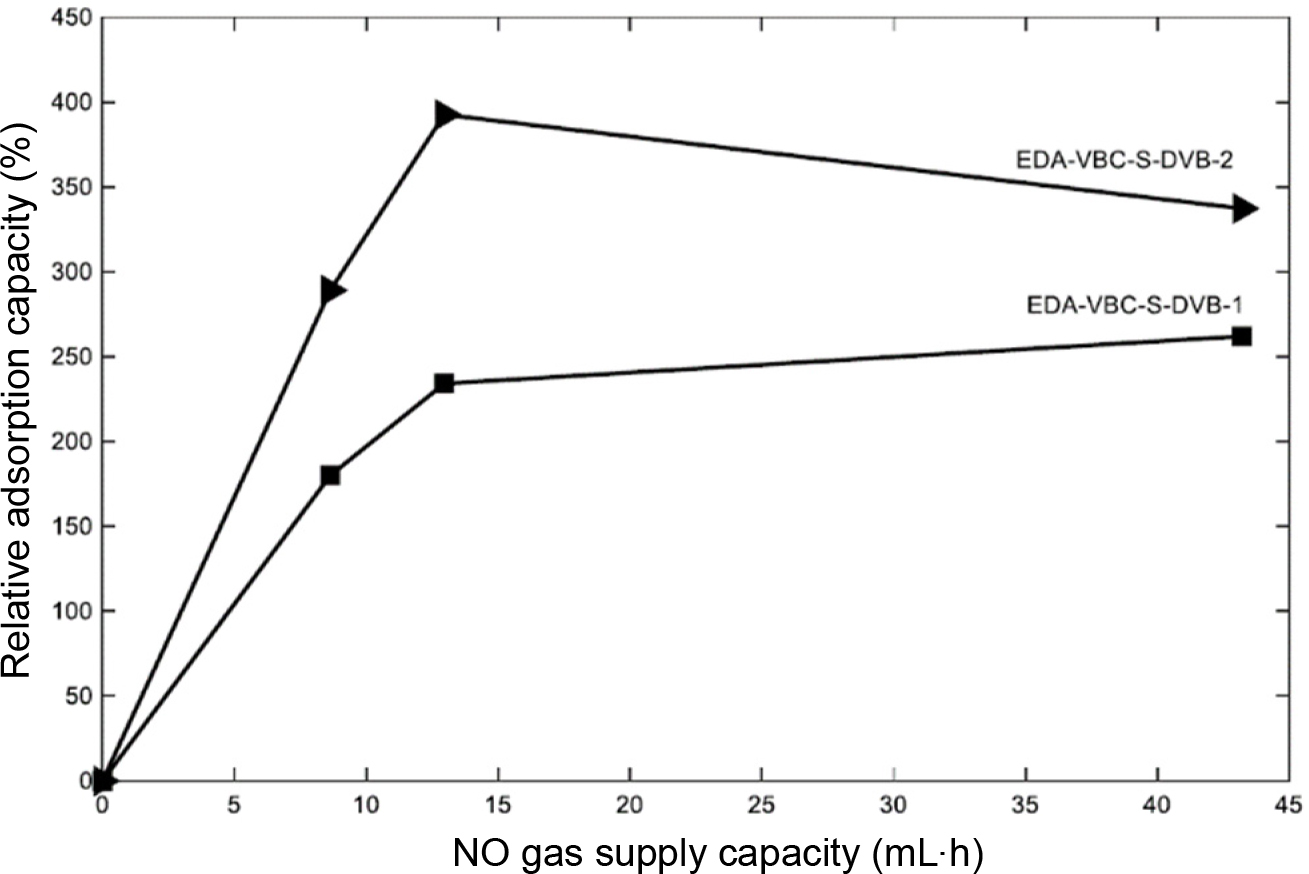
Figure 8은
NO 가스 공급용량 변화에 따른 시료의 상대적 NO 가스 흡착용량 변화를 나타낸 그래프이다. 그래프에서 x-축은 시료에 노출된 NO 가스 공급용량이며 y-축은 관계식(식 (3))으로부터 계산된 흡착 시료가 나타내는 상대 흡착용량이다.
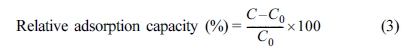
위 관계식에서 C0는 시료에 노출된 NO 가스 공급용량이 0 mL·h일 때 시료가 나타내는 NO 가스 흡착용량(mmol/g)이며, C는 시료에 노출된 NO 가스의 특정 공급용량 수치에 대하여
시료가 나타내는 NO 가스 흡착용량(mmol/g)이다. EDA-VBC-S-DVB-1와 EDA-VBC-S-DVB-2 시료 모두 시료에 노출된
NO 가스 공급용량이 증가함에 따라 상대 NO 가스 상대 흡착용량이 증가하였으며, 모든 흡착조건 변화에 대하여 EDA-VBC-S-DVB-2 시료가
EDA-VBC-S-DVB-1 시료보다 우수한 흡착 성능을 보여주었다. 이는 앞에서 언급했던 바와 같이 DVB 첨가량 증가에 따라 가교밀도가 증가하며
다공성을 나타내는 EDA-VBC-S-DVB 시료의 표면적이 증가한데 따른 결과이다. 노출된 NO 가스 공급용량이 어느 정도 수치값 이상에 도달하면
시료가 나타내는 NO 가스 상대 흡착용량은 최대 평형치를 보여주는 현상이 나타남을 확인할 수 있다. 따라서 EDA-VBC-S-DVB 시료가 갖는
NO 가스 흡착용량은 특정 가교밀도에 따라 노출된 NO 가스 공급용량에 대한 임계점이 존재한다는 것을 알 수 있다. 본 연구에서 제조한
EDA-VBC-S-DVB 두 종류 화합물의 경우 NO 가스 공급용량 임계점 수치는 공통적으로 12.96 mL·h를 보여 주었으며 NO 가스에 대한 흡착 용량
최대치는 1.2182 mmol-NO gas/g-adsorbent 그리고 NO 가스 상대 흡착용량은 392%를 나타내었다. Diaf 등은9
제조한 고분자의 경우 다양한 아민 화합물에 대하여 NO2 가스는 약 14 wt%와 NO 가스는 약 3.8 wt%의 최대 흡착 성능을 나타내며,
dipropylamine을 개질제로 사용한 고분자의 경우 아민 1 mol 당 최대 약 1.59 mol의 NO2 가스가 흡착된다고 보고하였다. 또한 Vinodh 등은10
제조한 과가교 고분자가 최대 13 wt%의 NOx 흡착률을 나타낸다고
보고하였다.
|
Figure 3 Adsorption mechanism of EDA-VBC-S-DVB for NO gas. |
|
Figure 4 FTIR spectra of (a) VBC-S-DVB; (b) EDA-VBC-S-DVB. |

|
Figure 5 SEM micrograph of EDA-VBC-S-DVB-2. |
|
Figure 6 XPS N1s spectrum of EDA-VBC-S-DVB-1 under the various adsorption conditions: (a) Before adsorption; (b) 100 mL-48 h; (c) 100 mL-72 h; (d) 500 mL-48 h. |
|
Figure 7 XPS N1s spectrum of EDA-VBC-S-DVB-2 under the various adsorption conditions: (a) Before adsorption; (b) 100 mL-48 h; (c) 100 mL-72 h; (d) 500 mL-48 h. |
|
Figure 8 Relative adsorption capacity of EDA-VBC-S-DVB depending on the NO gas supply capacity. |
|
Table 1 Area Analysis for the Characteristic Peaks in XPS
Spectra of EDA-VBC-S-DVB-1 and EDA-VBC-S-DVB-2 |
본 연구에서는
EDA-VBC-S-DVB의 NO 가스 흡착 성능을 알아보기 위한 실험을 수행하였다. 자유 라디칼 중합공정을 통해 성공적으로 삼원 공중합체
VBC-S-DVB를 제조하였으며 가교제 첨가량에 따라 두 종류의 시료를 준비하였다. 삼원 공중합체에 아민그룹을 도입하기 위하여 EDA를 사용하여 EDA-VBC-S-DVB 화합물을 제조하였으며
FTIR 분석을 수행함으로써 VBC-S-DVB에 아민 기능성 그룹이 결합되었음을 확인하였다. 가교제로 이용한 DVB의 첨가량을 변화시켜 팽윤 실험을
진행하였으며 각 시료의 질량 팽윤비 및 가교밀도를 계산하였다. DVB 첨가량이 30.33 mmol에서 60.66 mmol로 증가함에 따라 질량
팽윤비는 53.07%에서 7.67%로 약 7.5배 감소하였으며, 가교밀도는 2.98×10-3 mol/cm3에서 4.80×10-3 mol/cm3으로 증가함을 확인하였다.
SEM 분석을 통해 EDA-VBC-S-DVB-2 화합물의 표면에 가교반응에 의한 기공들이 생성되었으며 이들이 높은 표면적을 제공한다는 것을 확인하였다.
NO 가스에 대한 EDA-VBC-S-DVB 화합물의 흡착용량(mmol/g)을 분석하기 위하여 XPS 분석을 수행하였으며 NO 가스 공급용량의 임계치
12.96 mL·h에서 EDA-VBC-S-DVB 화합물이 나타내는
NO 가스에 대한 흡착용량의 최대치는 1.2182 mmol-NO gas/g-adsorbent이었으며 NO 가스 상대 흡착용량은 392%를 나타내었다.
- 1. J. Han, J. Meeprasert, P. Maitarad, S. Nammuangruk, L. Shi, and D. Zhang, J. Phys. Chem. C, 120, 1523 (2016).
-

- 3. D. Meng, Q. Xu, Y. Jiao, Y. Guo, Y. Guo, L. Wang, G. Lu, and W. Zhan, Appl. Catal. B: Environ., 221, 652 (2018).
-

- 5. S. Sumathi, S. Bhatia, K. T. Lee, and A. R. Mohamed, J. Hazard. Mater., 176, 1093 (2010).
-

- 7. F. Gao, X. Tang, H. Yi, B. Zhang, S. Zhao, J. Wang, T. Gu, and Y. Wang, Ind. Eng. Chem. Res., 57, 16593 (2018).
-

- 9. F. Rezaei and C. W. Jones, Ind. Eng. Chem. Res., 52, 12192 (2013).
-

- 11. G. W. Peterson, J. J. Mahle, J. B. DeCoste, W. O. Gordon, and J. A. Rossin, Angew. Chem. Int. Ed., 55, 6235 (2016).
-

- 13. X. Liu, Y. Li, Y. Ban, Y. Peng, H. Jin, H. Bux, L. Xu, J. Caro, and W. Yang, Chem. Commun., 49, 9140 (2013).
-

- 15. A. Diaf, J. L. Garcia, and E. J. Beckman, J. Appl. Polym. Sci., 53, 857 (1994).
-

- 17. A. Diaf and E. J. Beckman, React. Polym., 25, 89 (1995).
-

- 19. R. Vinodh, D. K. Kim, Y. Hwang, and H. G. Yeo, Int. J. Bio-sci. Bio-technol., 5, 85 (2013).
-

- 21. A. G. Mikos, C. G. Takoudis, and N. A. Peppas, Polymer, 28, 998 (1987).
-

- 23. T. Ramya, G. R. Ramkumaar, and S. Gunasekaran, Int. J. Neurorehabil., 1, 135 (2014).
- 25. S. Liu, D. Chen, J. Zheng, L. Zeng, J. Jiang, R. Jiang, F. Zhu, Y. Shen, D. Wu, and G. Ouyang, Nanoscale, 7, 16943 (2015).
-

- 27. G. Ruiz-Soria, A. P. Paz, M. Sauer, D. J. Mowbray, P. Lacovig, M. Dalmiglio, S. Lizzit, K. Yanagi, A. Rubio, A. Goldoni, P. Ayala, and T. Pichler, ACS Nano, 8, 1375 (2014).
-

- 30. M. Raicopol, C. Andronescu, R. Atasiei, A. Hanganu, and L. Pilan, J. Electrochem. Soc., 161, G103 (2014).
-

- Polymer(Korea) 폴리머
- Frequency : Bimonthly(odd)
ISSN 0379-153X(Print)
ISSN 2234-8077(Online)
Abbr. Polym. Korea - 2023 Impact Factor : 0.4
- Indexed in SCIE
 This Article
This Article
-
2020; 44(1): 30-37
Published online Jan 25, 2020
- 10.7317/pk.2020.44.1.30
- Received on Aug 22, 2019
- Revised on Oct 11, 2019
- Accepted on Oct 27, 2019
 Services
Services
Shared
 Correspondence to
Correspondence to
- Yangsoo Kim
-
*Department of Nanoscience & Engineering, Inje University, Gimhae 50834, Korea
**High Safety Vehicle Core Technology Research Center, Inje University, Gimhae 50834, Korea - E-mail: cheykim@inje.ac.kr
- ORCID:
0000-0002-5746-571X









 Copyright(c) The Polymer Society of Korea. All right reserved.
Copyright(c) The Polymer Society of Korea. All right reserved.