- Adsorption Kinetics Under Dry and Wet Conditions of TEDA Doped ACF for CH3I Adsorption
Joo Young You, Sang Sun Choi, Woo Jeong Lee, Joon Hyuk Lee*, and Soon Hong Lee†

Department of Environmental Engineering, Anyang University, Anyang 14028, Korea
*Department of Chemical Engineering, Hanyang University, Seoul 04763, Korea
- TEDA 첨착 활성탄소섬유에 기반한 건조 및 습윤상태에서의 방사성 아이오딘 흡착특성연구
안양대학교 환경공학과, *한양대학교 화학공학과
: Radioactive isotopes of iodine has been reported as
deleterious for living organisms. With the rapid development of nuclear
industry and the prevalence around the globe, there is an urgent need to
control the possibility of iodine-release. Within the paper, we observed the
adsorption experiments of triethylenediamine doped activated carbon fiber
(T-ACF) onto CH3I. T-ACF revealed 11.97% decrease in specific
surface area when compared to ACF, but showed transition of C=C or C-H bond to
C-N bond. In terms of the maximum adsorption capacity (qmax),
T-ACF was found to have 30.55 and 5.56% more qmax when
compared to ACF under dry and wet conditions, respectively. Given that,
post-introduced amine groups after the triethylenediamine (TEDA) treatment composed a preferable environment on
the carbonaceous surface for CH3I adsorption. Lastly, adsorption
experiments suggested that all the samples favored the Langmuir model in both
dry and wet conditions
원자력 시설에서 자연환경으로 유출될 수 있는 방사성 물질
중 아이오딘은 인체에의 위해도가 널리 보고된 바 있으므로 이에 대한 안전한 저감연구가 필요하다. 본
연구에서는 기존 흡착제 대비 높은 비표면적 및 흡착 용이성으로 각광받고 있는 활성탄소섬유(ACF)를
대상으로 triethylenediamine(TEDA) 첨착을 하고 그에 따른 기기분석 및 흡착실험을
진행하였다. TEDA를 첨착한 활성탄소섬유(T-ACF)는
일반 ACF 대비 11.97%의 비표면적 감소를 나타내었으나, C=C 또는 C-H의 표면 관능기가 C-N으로 치환됨 또한 확인되었다. 이러한 amine 그룹은 아이오딘의 흡착에 유리하게 작용될 수 있으며, 흡착시험
결과 역시 T-ACF가 일반 ACF 대비 건조상태 및 습윤상태에서
각각 30.55 및 5.56% 증가함을 확인하였다. 마지막으로, 흡착등온식에서는 모든 샘플들이 건조상태 및 습윤상태에서 Freundlich 식보다는 Langmuir 식에 더 적합함을 확인할
수 있었다
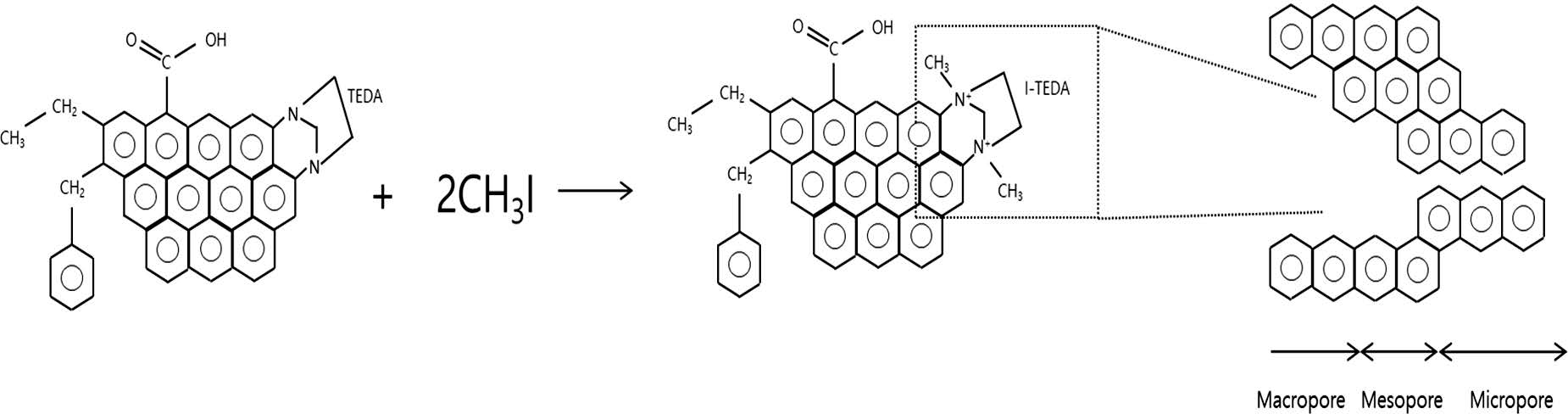
Activated carbon fibers were doped by TEDA in order to
generate functional groups. Adapting Langmuir and Freundlich kinetics,
increased amine groups were found to be preferable in radioactive iodine
adsorption.
Keywords: activated carbon fiber, radioactive materials, methyl iodide, adsorption, surface functional groups
본 연구는 에너지기술평가관리원(2017152 0000300)의
지원으로 수행되었음.
기체방사성 물질은
비록 양이 적을지라도 환경의 보호 및 작업종사자의 안전성 확보 측면에서 보다 완벽한 처리기술이 요구되고 있다.1 특히 원자력시설에서
발생하는 기체 방사성 물질은 화학적 성분이 다양하며, 각 성분의 특성에 적합한 각각의 처리방법이 요구되기 때문에 처리공정이 복잡하며 처리기술 또한
다양하다.2 원자력 시설의 사고 시에는 기체방사성 물질이 다량 발생할 뿐만 아니라 대상물질이 운전조건에 따라 고온 또는 고습도로
변화되어 처리공정도 이에 상응할 수 있도록 설계되어야 한다. 이 중 특히 방사성 아이오딘(I131)은 발생량이 비교적 많을
뿐 아니라 인체 및 자연환경에 미치는 위해도가 크므로 이의 발생원, 형태 그리고 제거방법 등에 대한 많은 연구가 수행되고 있다.3
대표적인 방사성 아이오딘은
핵분열물질이 핵분열될 때 발생하는 생성물 중 하나로 열중성자(thermal neutron)에 의해서 우라늄이 핵 분열될 때 생성되는 전체 핵분열생성물
중 약 2.8%를 차지하는 방사성 동위원소 중 하나이다.4,5 분자성 아이오딘은 방사능 준위가 높고 기체로 존재하는
화학종이므로 체내 흡수성이 높기 때문에 원전사고 초기확산에의 특별한 유의가 요구되는 핵종이다.6-8 일반적으로 아이오딘은 사용
후 핵연료 내에서 세슘의 아이오딘화합물(CsI)로 존재하며 연료외부로 방출된다. 특히 방출 초기점이 냉각수 내부일 가능성이 높기 때문에, 냉각수에
용해된 아이오딘 이온이 휘발성 분자 아이오딘(I2)으로의 산화를 억제시키는 방법이 제시된 바 있다. 나아가, 냉각수의 pH와
산화환원 상태(redox condition)를 조절하는 방법이 현장에서 활발하게 사용되고 있다. 그러나 상기와 같은 방법은 냉각수의 온도가 상승한다거나
방사선에 노출된 환경에서 아이오딘의 휘발도가 상승하여 원자로격납건물 내부대기로 방출될 수 있는 한계 또한 상존한다. 이외에도, 아이오딘은 유기물질과
쉽게 반응하여 유기아이오딘을 형성하면서 휘발도가 상승하기 때문에 유기물질과의 접촉을 억제하는 방법들 또한 연구되고 있다.9,10
대기 중으로 방출된
아이오딘을 제거하는 방법으로는 흡착물질인 활성탄소(activated carbon, AC) 및 제올라이트(zeolite)처리가 일반적이다.11,12 이
중 AC의 경우, 활성화 시 비표면적과 기공 구조를 조절할 수 있고 재생 및 장기사용의 이점이 있어 흡착제로의 활용이 용이하다.13,14 그러나
불균일한 기공형성 때문에 흡착속도와 흡착성능 간 상관성이 낮은 경우가 있고, 흡착설비에의 적용 시 대상 흡착제의 무게와 부피를 고려하여 설계해야 하는 단점이 있다. 제올라이트의
경우, open-pore 형태로
미세기공이 일정하게 형성되어 있어 초기 흡착성능에는 뛰어나지만 재생 및 장기사용의 경우 open-pore가 작아지므로 지속적인 흡착제로의 성능을 발휘하지 어렵다.15 이를 극복하기 위해 흡착제의 흡착성능을 개선하기 위해
많은 연구가 진행 중에 있다. 최근 높은 비표면적과 빠른 흡착속도를 가지는 활성탄소섬유(activated carbon fiber, ACF)가 주목받고
있으며, 과거에도 TEDA를 첨착하여 아이오딘을 흡착한 논문이 있다.16-18 ACF는 주로 20 Å 이하의 micro-pore가 균일하게 분포하여 빠른 흡착속도를
가지며, 높은 비표면적으로 인한 우수한 흡착성능 및 관능기가 상대적으로 잘 형성되어 원하는 제거대상 물질에 흡착성능을 향상시킬 수 있다.19,20 또한
섬유형태로서의 가공 또한 뛰어나 여러 분야에의 적용이 활발하게 이루어지며, 본 연구에서는 효율적인 기체방사성 아이오딘의 흡착인자를
확인하기 위해 pyrolyzed fuel oil(PFO)를 섬유화하여 pitch계 ACF를 제조하였다. 그 후에
triethylenediamine(TEDA)를 ACF에 첨착하여 물리적 특성 및 기공특성을 기기분석하였으며, 건조 및 습윤 조건 하에서의 흡착성능을
TEDA 첨착하지 않은 탄소계 흡착제와 비교분석했다. 마지막으로, 이를 Langmuir 및 Freundlich 식을 통해 샘플에 대한 아이오딘 흡착능을 평가하였다.
Pitch계 활성탄소섬유 제조. 전구체인 PFO는 현대오일뱅크에서 공급받아 이를 토대로
pitch계 ACF를 제조하였다. Pitch를 섬유형태로 방사하기 위해서는 고점도의 pitch가 요구되므로, 휘발성 유분을 제거하기 위한 전처리를
선진행하였다.21 전처리는 N2 분위기에서 150 rpm으로 교반하였고, 340 oC에서 6시간 동안 열처리를 진행하였다. 전처리 후 고점도의 pitch를 섬유형태로 가공하기 위해 용융방사를
실시하였다. 용융방사는 N2
분위기에서 방사온도 180 oC에서 0.76 mm의 노즐을 0.3 bar의 압력으로 진행하였으며, 이에 따른 토출량은 0.2 g/min이다. 용융방사 후 제조된 pitch 섬유는
탄화 시 고온에 의해 융해되는 특성을 지닌 열가소성 소재이다. Pitch 섬유를 열경화성으로 전환하기 위한 안정화 과정을 진행하였다.22
안정화 과정은 열풍순화식 가열로에서 air 분위기 하 승온속도 8.5 oC/min으로
30분 간 온도를 상승시켜
255 oC에서 3시간 동안 진행하였다.
탄화 및 활성화 과정은
탄화로에서 N2 가스를 4 L/min으로 주입하며 진행하였으며, 승온속도 14.6 oC/min으로 온도를 상승시킨 뒤, 최종 탄화온도를 880 oC로 3시간 유지하였다. 880 oC 도달 후, 탄소는
H2O와 반응하여 섬유표면의 기공을 형성한다는 연구가 있어 활성화 가스로 H2O를 수증기 형태로 0.3 mL/min으로 주입한 뒤 활성화 과정을 거쳐 ACF를
제조하였다.23 제조된 ACF와 대조군인 AC에 10 wt%의 TEDA를 첨착하였다. ACF와 AC를 10 wt%의 TEDA에 담지하여 3시간 동안 방치 후, 드라이오븐에서
6시간 동안 건조시켜서 T-ACF 및 T-AC를 각각 제조하였다.24
기기분석. 비표면적 측정장치(BET, Micromeritics사,
ASAP 2460)를 도입하여 제조된 샘플의 표면에 생성된 비표면적, 미세기공표면적, 외부표면적 등을 분석하였다. 샘플의 전처리는 100 oC에서 24시간 동안 수분을 제거하였으며, 액체질소를 이용하여 77 K에서 P/P0(상대압력)에
따른 비표면적을 분석하였다. 여기에서, 비표면적은 BET 식을 이용하여 측정하였으며 이는 식 (1)과 같다.25

식 (1)에서 A는
흡착제의 표면적, Vm은 단분자층 흡착에 필요한 기체부피, V0는 흡착기체의 몰
부피(0 oC에서 22.4 L), Na는 아보가드로 수, Am은 기체분자의
단면적이다. 미세기공 표면적 및 외부 비표면적은 t-Plot 식을 이용하였으며, 이는 식 (2)와 같다.26,27

샘플의 형상변화를
관찰하기 위해 주사전자현미경(SEM, Hitachi사, S-3000H)을 이용하였다. SEM의 배율은 ×1000 및 ×100000으로 분석하였다. SEM 분석 전 모든 샘플은
금코팅 전처리 후 진행하였다. 마지막으로 TEDA 첨착 전후의 샘플 표면관능기 변화를 분석하기 위해 X선 광전자 분광법(XPS,
KRATOS사, AXIS NOVA)을 활용하였다.
흡착능 분석. 아이오딘화메틸(CH3I)을 통해 샘플들의
흡착특성을 기체 크로마토그래피(GC, DANI 사, Master GC)에 기반한 회분식 흡착실험을 통해 분석하였다. 20 mL vial에 각각 CH3I
500 ppm을 주입 후 제조된 샘플의 양적 비교를 위해
0.1~0.5 g의 중량변화를 준 뒤, CH3I가
휘발될 수 있도록 30 oC에서 150 rpm의 속도로 항온진탕기에서 16시간 동안 진탕하였다. 흡착평형에 도달했을 때 남아있는 CH3I의 농도를 측정하였다. 건조
및 습윤 상태의 샘플비교를 위해 각 샘플을 두 조건으로 분류하였으며, 이에 따른 결과를 각각 Langmuir 식과 Freundlich 식에 적용하여
흡착등온선을 구하여 흡착평형인자를 분석하였다. 본 연구에서 사용된 Langmuir 식과 Freundlich 식은 각각 (3), (4)와 같다.28,29

상기
Langmuir 식에서 Ce는 평형조건에 도달한 평형농도 (mg/L)이며, qmax는
Langmuir 식에서 흡착제의 단위무게 당 최대흡착량(mg/g)이며 b는 상수를 나타낸다. Freundlich 식에서의 KF
및 n은 모두 상수를 나타낸다.
샘플의 물리적 특성. 각 샘플의 BET 결과 값을 Table 1에 나타내었다.
TEDA 첨착을 하지 않은 샘플인 AC와 ACF의 BET 값은 각각 980과 1420 m2/g이였으며, TEDA 첨착을
진행한 T-AC와 T-ACF는 751, 1250 m2/g으로 측정되었다. 여기에서, ACF에 기반하여 제조된 샘플들이 AC에 기반하여
제조된 샘플 대비 micropore의 비중이 높은 것으로 나타났다. 이는 ACF 제조과정에서 이루어지는 고온의 탄화 및 섬유형태의 특성으로 인한
것으로 보인다. 일반적으로 pitch계 ACF의 경우, 전구체인 PFO의 특성 상 정제과정에서 불순물이 제거되기 때문에 C 함량이 높다고 보고된
바 있다.30 방사 후 공정을 거치게 되면, ACF 결정 내 안정하지 못한 탄소가 일산화탄소 혹은 이산화탄소로 방출되면서 카복실기(-COOH),
카보닐기(=C=O) 등과 같은 표면 관능기를 형성한다. 이와 같은 활성화 반응이 연속적으로 발생됨에 따라 미세기공과 비표면적이 증가하게 된다.31
여기에서, TEDA 첨착 시료인 T-AC와 T-ACF의 경우 AC 및 ACF 대비 각각 229, 170 m2/g의 비표면적 감소가 나타났다. 이는 첨착과정에서
pore 결정구조가 약한 일부 micropore가 무너지면서 mesopore로 변하였거나, TEDA 입자에 의해 micropore를 막아버리기
때문으로 판단된다.32
제조된 샘플의
TEDA 첨착에 따른 형상변화를 관찰하기 위해 SEM 분석을 진행하였다. Figures 1(a)와 1(c)는 첨착하지 않은 AC와 ACF의 형상을 나타낸다.
여기에서, AC의 경우, ACF 대비보다 많은 용적의 mesopore가 관측되었다. 이는 상기에서 고찰한 바와 같이 대상 샘플의 물리적 특성에
기인한 것으로 보인다. TEDA를 첨착한 AC 및 ACF의 형상을 Figures 1(b)와 1(d)에서 확인한 결과, TEDA가 T-AC 대비
T-ACF에 보다 원활한 첨착이 진행된 것을 확인할 수 있었다. T-ACF의 경우, macropore 형상이 주를 이루는 과립활성탄 기반의
T-AC보다 TEDA 첨착이 보다 용이하게 이루어진 것으로 보이며, TEDA 첨착으로 인한 관능기의 형성은 XPS를 통해 확인할 수 있었다.
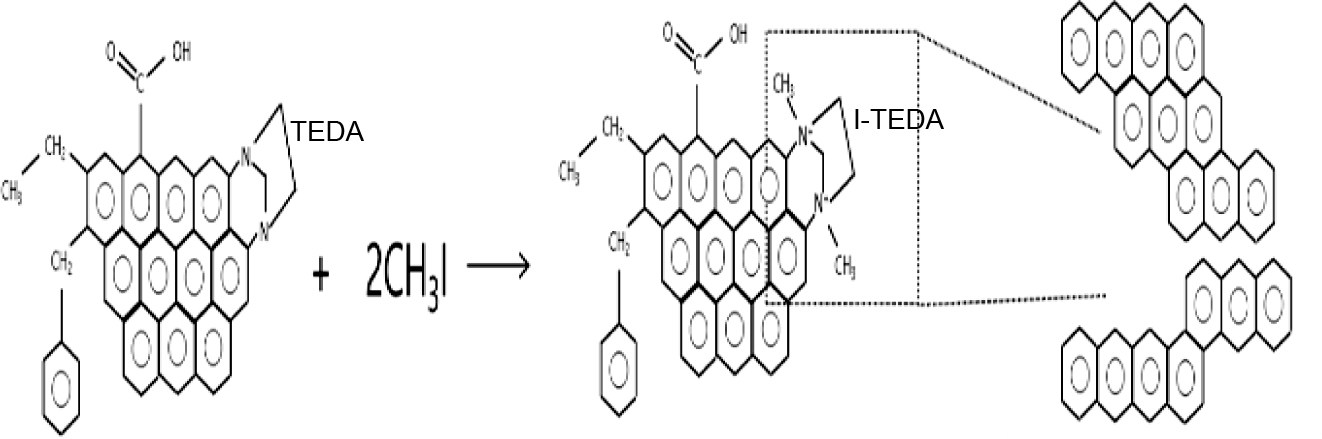
샘플의 화학적 특성. 제조된 샘플표면의 화학적 특성변화를 확인하고자 XPS
분석을 실시하였다(Figure 2). ACF와 AC는 284.5 eV와 532 eV 부근에서 각각 C1s와 O1s 피크가 나타나는 것을 확인할 수 있었고,
TEDA 첨착샘플의 경우 399 eV 부근에서 N1s 피크가 나타난 것을 확인할 수 있었다.33 이는 제조된 샘플표면의 C=C 또는 C-H 결합들이
분해되어 C=O 또는 -COOH와 같은 표면 관능기들이 새롭게 형성된 것으로 판단된다. T-AC와 T-ACF는 AC와 ACF에 비해 C1s 피크
값이 낮아지는 경향이 나타났으며, 이는 TEDA 영향에 의한 C=C 또는 C-H 결합이 C-N 결합으로 치환되면서 결합에너지가 낮아지는 것으로
보인다. TEDA 첨착을 통한 amine 관능기의 생성은 흡착대상인 CH3I의 흡착에 유리한 환경을 조성할 것으로 보인다.34
O1s 피크 역시 TEDA 첨착 후 상대적으로 532.5 eV 값이 감소하고 533 eV 값이 증가하였다. 일반적으로
산소포함 관능기들은 섬유표면의 극성요소 및 계면 결합력을 증가시켜 흡착능의 향상에 기여한다고 알려져 있다. 따라서 최적의 TEDA 농도와 첨착시간 등의 선정이 이루어진다면 흡착 대상에 부합하는 표면 관능기의 선별적
도입이 가능할 것으로 판단된다.
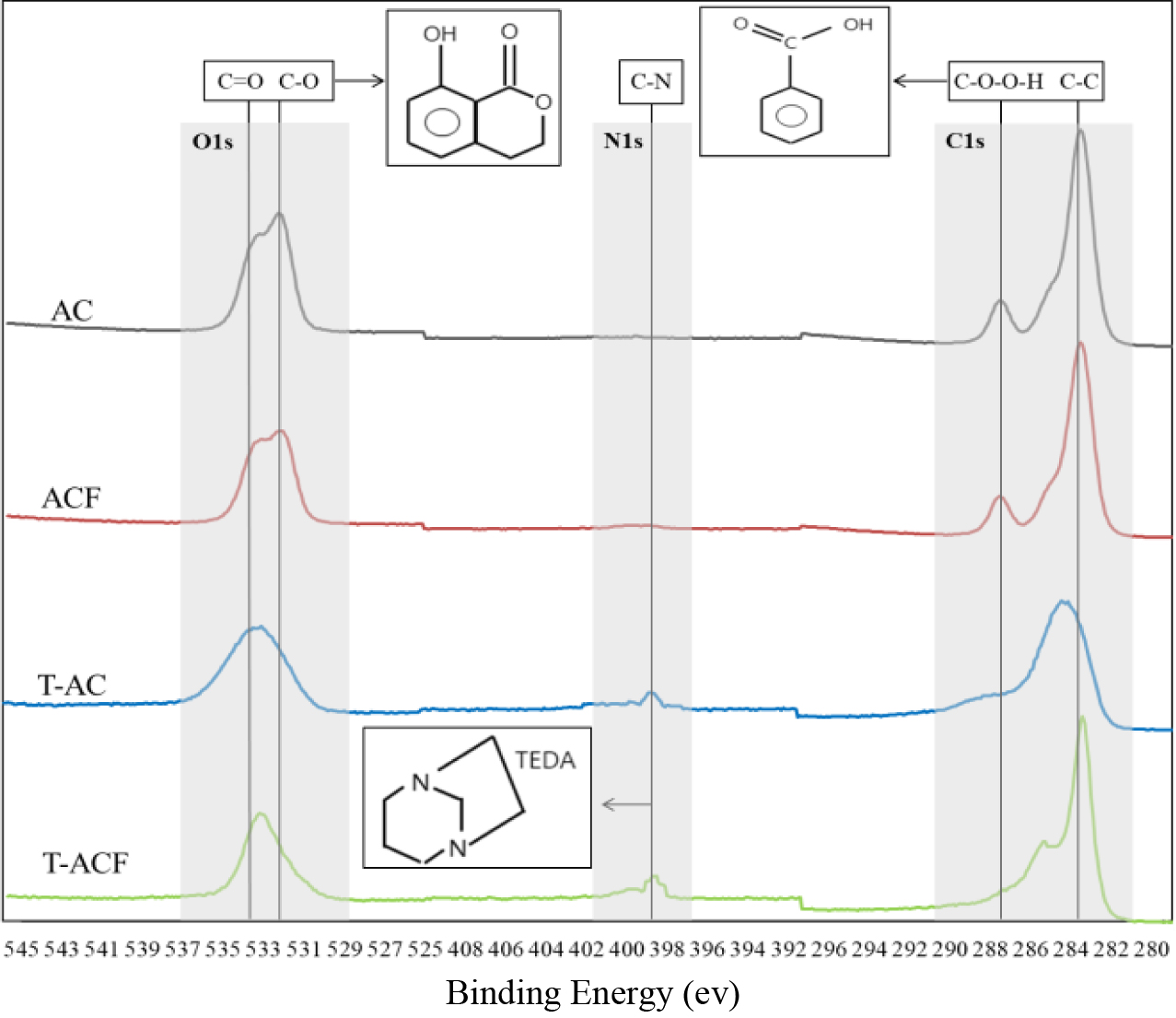
샘플의 CH3I 흡착능 평가. 제조된 샘플의 흡착특성을 분석하기 위해 건조 및 습윤상태에서의
CH3I 500 ppm에 대한 흡착능 평가를 진행하였다. 여기에서, 흡착제의 양을 0.1 g으로 하여 시간에 따른 제거율 그래프를 Figure
2에 나타냈다. 건조상태에서의 CH3I 제거는 AC와 ACF가 초기 빠른 흡착을 나타냈지만, 물리적 흡착이 끝난
13시간 이후부터는 T-AC와 T-ACF가 더 많은 CH3I를 흡착하는 것을 확인할 수 있었다(Figure 3(a)). 이는
초기 흡착에는 micropore에 의한 물리적 흡착이 진행되지만, 물리적 흡착이 끝나는 시점부터는 amine 관능기에 기반한 화학적 흡착이 이루어지기
때문으로 보인다. 습윤상태에서는 AC와 ACF가 2시간까지 20%의 흡착이 이루어진 뒤, 흡착평형에 도달하였다(Figure 3(b)). 반면, T-AC와 T-ACF의 경우 약 14시간까지 흡착이
더 오래 지속되는 것을 확인할 수 있었다. 이와 같은 습윤상태에서의 흡착시간 차이는 AC와 ACF 내 micropore가 습윤상태인 수분 내 극성이
무극성인 샘플표면에의 CH3I 흡착을 방해한 것으로 보인다. 그러나 T-AC와 T-ACF의 경우 상기와 같이 화학적 흡착이
추가적으로 발생하기 때문에 보다 높은 흡착능을 보인 것으로 사료된다.35
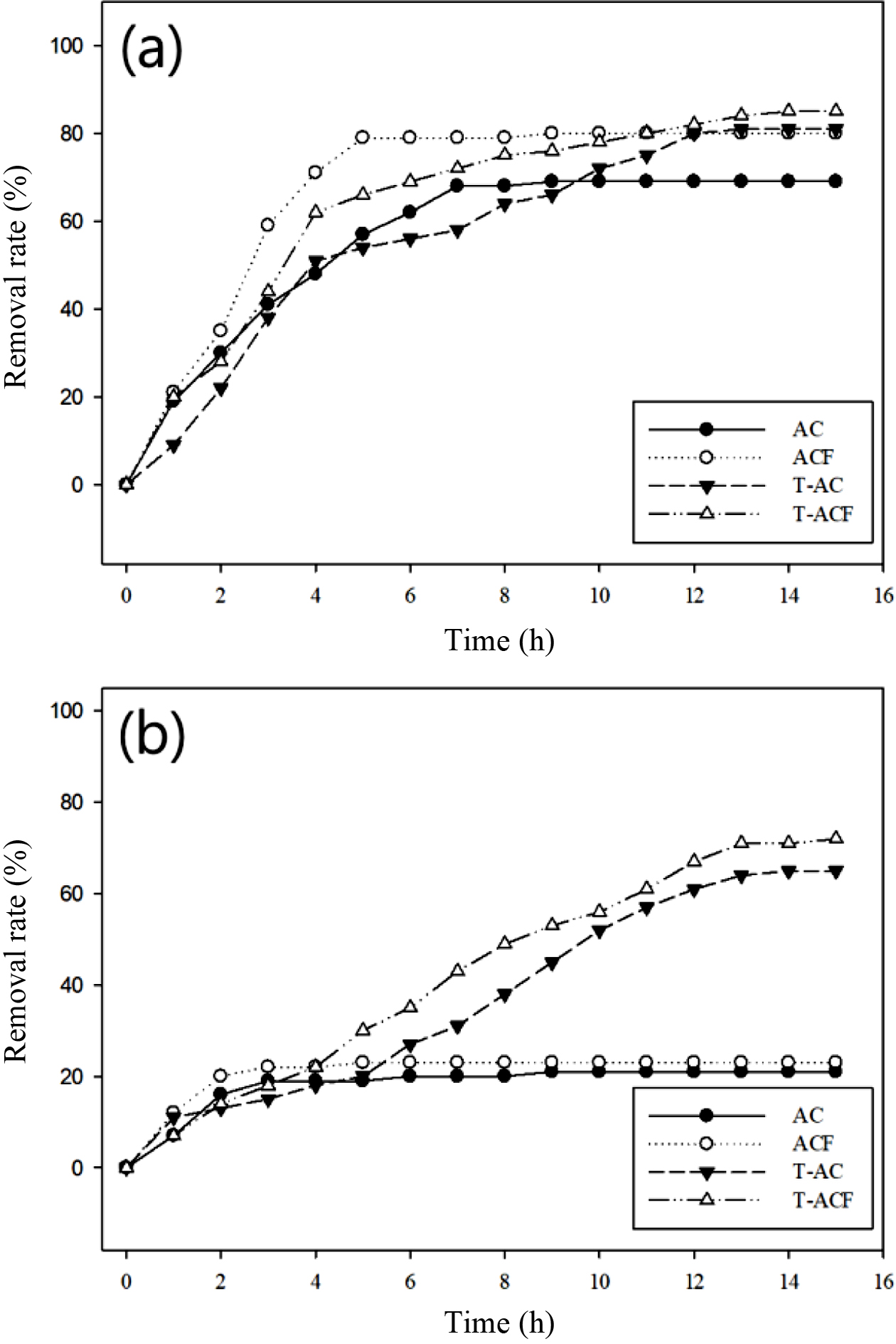
각 샘플별 최대 흡착량을
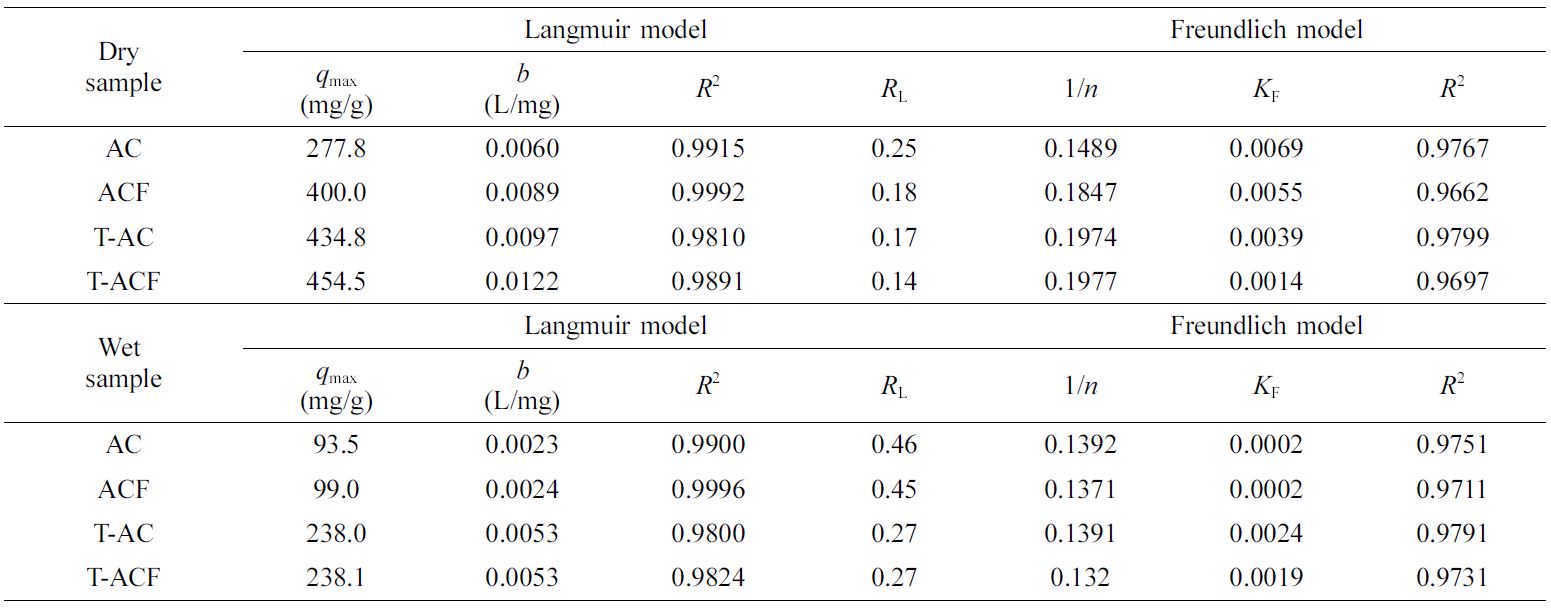
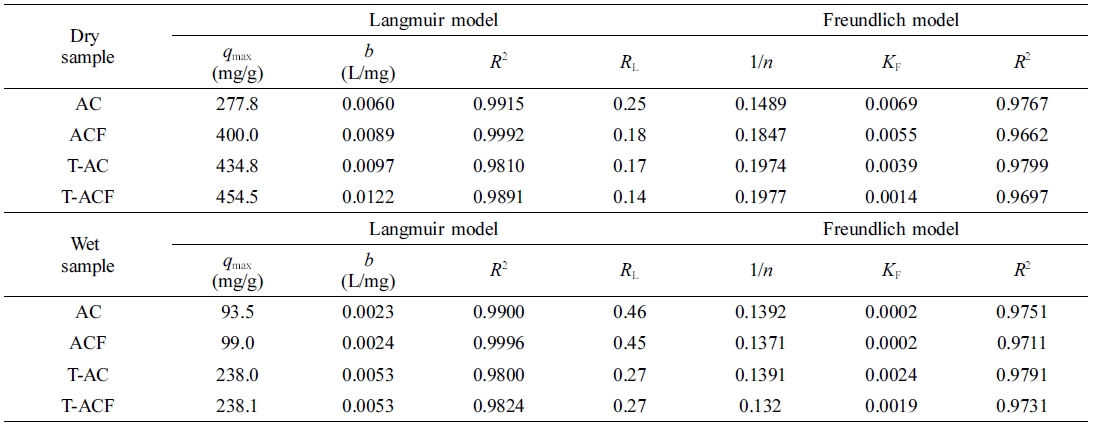
알아보기 위해 Langmuir와 Freundlich 식을 도입하였다. 샘플의 양을 0.1~0.5 g로 변화하여 얻은 데이터를 Figure 4 및 Table 2에
나타내었다. 이론적 최대 흡착량(qmax)의 경우, TEDA를 첨착한 T-AC와 T-ACF가 AC와 ACF 대비
높은 결과값을 도출하였다. 건조상태인 AC와 ACF의 qmax는 각각 277.8, 400.0 mg/g였으며, 이 때의 T-AC와 T-ACF의 qmax는
각각 434.8, 454.5 mg/g로 나타났다. 습윤상태인 경우 AC와 ACF의 qmax는
각각 93.5, 99.0 mg/g였으며, 이 때의 T-AC와 T-ACF의 qmax는
각각 238.0, 238.1 mg/g로 나타났다.

식 (5)는
Langmuir 식에 기반하여 만드는 식이며, RL 값의 경우, 0일 경우 비가역 반응이며 0 < RL < 1일 경우는 흡착에 유리한 반응이다. 여기에서, RL
값이 1 이상일 경우에는 흡착이 잘 이루어지지 않는 것으로 알려져 있다.36 상기 흡착실험에서 계산된 RL
값은 평균 0.27으로 (0 < RL < 1), 이를 토대로 CH3I의 흡착이 균일하게
이루어지는 것으로 판단된다. 일반적으로 Freundlich 식의 1/n 값이 1보다 클 경우, 다단흡착이라고 정의할 수 있다.37
본 실험결과, 1/n의 값이 1보다 작게 나타났기 때문에 CH3I의 흡착은 단층흡착으로 볼 수 있다. 마지막으로,
모든 샘플에서의 R2 값이 Freundlich 식보다 Langmuir 식에서 높은 것을 근거로 본 연구에서의
CH3I 흡착은 Langmuir 식에 더 적합함을 알 수 있었다.38
|
Figure 1 SEM images of each sample with magnification range from ×1000 to ×100000: (a) AC; (b) T-AC; (c) ACF; (d) T-ACF. |

|
Figure 2 XPS survey spectra of each sample. |
|
Figure 3 CH3I removal rate as a function of time of (a) dry sample; (b) wet sample. |
|
Figure 4 CH3I adsorption using the Langmuir isotherm (a) dry sample; (b) wet sample and the Freundlich isotherm (c) dry sample; (d) wet sample. |
본 연구에서는
ACF에 TEDA를 첨착시킨 T-ACF를 제조하여 대조군인 AC, ACF 및 T-AC와의 물리화학적 변화 및 CH3I 흡착능을
고찰하였으며 이에 따른 제시결과는 다음과 같이 정리될 수 있다.
1. 샘플에 대한 물리적 분석결과, ACF가 1420 m2/g으로 가장 큰 비표면적을 나타내었다.
ACF에 기반한 T-ACF의 경우에도 T-AC 대비 상대적으로 높은 비표면적을 보였다. ACF 샘플들이 AC 샘플 대비 상대적으로
micropore가 많이 분포하므로 TEDA 역시 ACF 샘플들에서 보다 높은 첨착이 이루어진 것으로 보인다.
2. 샘플에 대한 화학적 분석결과, TEDA 첨착은 C-N 결합을 증가시키는 것으로 확인되었다. 탄소계 표면 내
amine 기의 증가는 CH3I의 흡착에 유리한 조건을 형성할 수 있다. 샘플 내 표면 관능기 변화를 통해 TEDA 첨착이
성공적으로 이루어졌음을 확인할 수 있었다.
3. 샘플에 대한 CH3I 흡착능 평가를 통해 TEDA 첨착은 qmax의 값과 유의한 상관관계가 있음이 입증되었다. 여기에서, 전 샘플에서 Langmuir 식이
Freundlich 식보다 적합한 것으로 나타났다.
- 1. K. Beaugelin-Seiller, R. Gilbin, S.Reygrobellet, and J. Garnier-Laplace, Environ. Pollut., 249,189 (2019).
-

- 2. K. Minami, T. Funabashi, K. Honda, A.Takahashi, K. Sakurai, R. Kanai, and T. Kawamoto, Water Res., 154,28 (2019).
-

- 3. E. A. Abdel-Galil, R. S. Hassan, and M. A. Eid, Appl.Radiat. Isotopes, 148, 91(2019).
-

- 4. E. Aneheim, D. Bernin, and M. R. S. Foreman, Nucl.Eng. Des., 328, 228 (2018).
-

- 5. M. R. S. J. Foreman, Cogent Chem., 1,1049111 (2015).
-

- 6. K. Kosaka, M. Asami, N. Kobashigawa, K. Ohkubo, H.Terada, N. Kishida, and M. Akiba, WaterRes., 46, 4397 (2012).
-

- 7. K. Hirose, J. Environ. Radioact., 111,13 (2012).
-

- 8. H. Amano, M. Akiyama, B. Chunlei, T. Kawamura, T.Kishimoto, T. Kuroda, and Y. Watanabe, J. Environ. Radioact., 111,42 (2012).
-

- 9. X. Li, G. Chen, J. Ma, and Q. Jia, Sep. Purif.Technol., 210, 995 (2019).
-

- 10. D. K. Harijan, V. Chandra, T. Yoon, and K. S. Kim, J.Hazard. Mater., 344, 576 (2018).
-

- 11. J. Huve, A. Ryzhikov, H. Nouali, V. Lalia, G. Augé,and T. J. Daou, RSC Adv., 8, 29248 (2018).
-

- 12. C. M. González-García, J. F. González, and S. Román, FuelProcess. Technol., 92, 247 (2011).
-

- 13. J. Gamby, P. L. Taberna, P. Simon, J. F. Fauvarque,and M. Chesneau, J. Power Sources, 101, 109 (2001).
-

- 14. A. Dąbrowski, P. Podkościelny, Z. Hubicki, and M.Barczak, Chemosphere, 58, 1049 (2005).
-

- 15. C. J. Jacobsen, C. Madsen, J. Houzvicka, I. Schmidt,and A. Carlsson, J. Am. Chem. Soc., 122, 7116 (2000).
-

- 16. M. Kumita, N. Yamawaki, K. Shinohara, H. Higashi, A.Kodama, N. Kobayashi, and Y. Otani, Int. J. Refrig., 94, 127(2018).
-

- 17. X. Xi and D. D. L. Chung, Carbon, 145,734 (2019).
-

- 18. S. Kato, Y. Minowa, M. Murata, Y. Harada, and N.Ishizaki, Jpn J. Health Phys., 21, 9 (1986).
-

- 19. H. M. Lee, L. K. Kwac, K. H. An, S. J. Park, and B. J.Kim, Energy Convers. Manag., 125, 347 (2016).
-

- 20. X. Zhao, X. Ma, and P. Zheng, Chemosphere, 202,298 (2018).
-

- 21. J. S. Hwang, C. H. Lee, K. H. Cho, M. S. Kim, C. J.Kim, S. K. Ryu, and B. S. Rhee, Korean Chem. Eng. Res., 33, 551(1995).
-

- 22. H. A. El Akrami, M. F. Yardim, and E. Ekinci, Fuel,79, 497 (2000).
-

- 23. B. K. Choi, L. K. Kwac, K. E. Yoon, M. K. Seo, and S.J. Park, Textile Sci. Eng., 51, 174 (2014).
-

- 24. R. Lascola, D. A. Knight, R. Mohtadi, P.Sivasubramanian, and R. Zidan, Int. J. Hydrog. Energ., 38, 13368(2013).
-

- 25. A. Ebadi, J. S. S. Mohammadzadeh, and A. Khudiev, Adsorption,15, 65 (2009).
-

- 26. R. Ghezini, M. Sassi, and A. Bengueddach, Micropor.Mesopor. Mater., 113, 370 (2008).
-

- 27. G. Leofanti, M. Padovan, G. Tozzola, and B.Venturelli, Catal. Today, 41, 207 (1998).
-

- 28. A. Kumar, S. Kumar, S. Kumar, and D. V. Gupta, J.Hazard. Mater., 147, 155 (2007).
-

- 29. W. Qu, T. Yuan, G. Yin, S. Xu, Q. Zhang, and H. Su, Fuel,249, 45 (2019).
-

- 30. E. Raymundo-Pinero, D. Cazorla-Amorós, A.Linares-Solano, J. Find, U. Wild, and R. Schlögl, Carbon, 40, 597(2002).
-

- 31. J. Li, D. H. Ng, P. Song, C. Kong, Y. Song, and P.Yang, Biomass Bioenergy, 75, 189 (2015).
-

- 32. C. M. González-García, J. F. González, and S. Román, FuelProcess. Technol., 92, 247 (2011).
-

- 33. K. Ho, S. Moon, H. C. Lee, Y. K. Hwang, and C. H. Lee,J. Hazard. Mater., 368,550 (2019).
- 34. A. Zengin and T. Caykara, Mater. Sci. Eng. C,32, 1107 (2012).
-

- 35. H. Chun, J. Kang, and B. Han, Phys. Chem. Chem.Phys., 18, 32050 (2016).
-

- 36. J. J. Lee, Korean Chem. Eng. Res., 53,64 (2015).
-

- 37. G. Ciobanu, M. Harja, L. Rusu, A. M. Mocanu, and C.Luca, Korean J. Chem. Eng., 31, 1021 (2014).
-

- 38. M. U. Dural, L. Cavas, S. K. Papageorgiou, and F. K.Katsaros, Chem. Eng. J., 168, 77 (2011).
-

- Polymer(Korea) 폴리머
- Frequency : Bimonthly(odd)
ISSN 0379-153X(Print)
ISSN 2234-8077(Online)
Abbr. Polym. Korea - 2023 Impact Factor : 0.4
- Indexed in SCIE
 This Article
This Article
-
2019; 43(6): 846-851
Published online Nov 25, 2019
- 10.7317/pk.2019.43.6.846
- Received on Jun 18, 2019
- Revised on Aug 16, 2019
- Accepted on Aug 16, 2019
 Services
Services
Shared
 Correspondence to
Correspondence to
- Soon Hong Lee
-
Department of Environmental Engineering, Anyang University, Anyang 14028, Korea
- E-mail: leesh@anyang.ac.kr
- ORCID:
0000-0002-9585-3836









 Copyright(c) The Polymer Society of Korea. All right reserved.
Copyright(c) The Polymer Society of Korea. All right reserved.