- Preparation and Characterization of Absorbent Materials on Glass-Web Fibers for Removal of Mercury Ion
In-Soo Kang, Tae Jin Lee, Myung Jo Seo*, Sang Yeon Hwang**, No-Kuk Park†
 , and Seung Woo Lee†
, and Seung Woo Lee† 
School of Chemical Engineering, Yeungnam University, 280 Daehak-ro, Gyeongsan, Gyeongbuk 38541, Korea
*Micro-one Inc., 368 Yeongok-road, Ibjang-myeon, Seobuk-gu, Cheonan-si, Chungnam 31026, Korea
**Institute for Advanced Engineering (IAE), 175-28, Goan-ro 51beon-gil, Baegam-myeon, Cheoin-gu, Yongin, Gyeonggi-do 17180, Korea- 유리 망사 섬유를 지지체로 하는 수은 제거용 흡착체의 제조와 특성 평가에 대한 연구
영남대학교 화학공학부, *㈜마이크로원, **고등기술연구원
Absorbent materials for mercury removal were prepared using (3-aminopropyl)trimethoxysilane (APTMS) and trimethoxy(octyl)silane (TMOS) on the surface of glass web fiber. Surfaces of the absobent materials were characterized by attenuated total reflectance Fourier transform infrared (ATR-FTIR) and X-ray photoelectron spectroscopy (XPS). The elements of the modified surface in the absorbent materials were well accordance with those of APTMS or TMOS. Adsorption of mercury ion from mercury-contaminated water using the prepared absobent materials was studied. Quantitative measurement of mercury ion was carried out on inductively coupled plasma-optical emission spectroscopy (ICP-OES). The ability of mercury ion removal from mercury-contaminated water is in the sequence of APTMS-modified glass web > TMOS-modified glass web > pristine glass web. This sequence has relationship with chemical structure of APTMS and TMOS which were used for modification of glass web.
수은 이온의 제거를 위한 흡수체를 glass web을 지지체로 하고 그 표면을 (3-aminopropyl)trimethoxysilane (APTMS)와 trimethoxy(octyl)silane(TMOS)로 처리하여 제조하였다. 제조된 흡수체의 표면은 희석 총 반사율 적외선 분광법과 X-선 광전자 분광법을 이용하여 표면 처리 전의 glass web과 비교 분석하였다. APTMS와 TMOS는 지지체의 표면에 반응을 통하여 고정화되어짐을 확인하였다. 수은 이온의 제거 능력을 비교하기 위하여 glass web과 APTMS와 TMOS를 표면에 가지는 glass web을 유도 결합 플라즈마 방출 분광기 분석을 통하여 실험하였으며, 실험 결과 APTMS 표면 처리 glass web > TMOS 표면 처리 glass web > glass web의 순서로 중금속 수은 이온을 제거할 수 있음을 확인하였다. 이러한 순서는 glass web의 표면 처리에 이용된 APTMS와 TMOS의 화학 구조와 연관성을 가진다.
Absorbent materials for mercury removal were prepared using (3-aminopropyl)trimethoxysilane (APTMS) and trimethoxy(octyl)silane (TMOS) on the surface of glass web fiber. The ability of mercury ion removal from mercury-contaminated water is in the sequence of APTMS modified glass web > TMOS-modified glass web > pristine glass web.
Keywords: absorbent materials, mercury ion, Fourier transform infrared spectroscopy, X-ray photoelectron spectroscopy, inductively coupled plasma-optical emission spectroscopy
본 연구는 2016년도 산업통상자원부(MOTIE)의 재원으로 한국에너지기술평가원(KETEP)의 지원을 받아 수행한 연구 과제입니다(20161120200170).
수질오염과 대기오염 문제는 급격한 산업화와 무분별한 발전에 뒤따라 꾸준히 대두됐으며, 특히 중금속에 의한 수질 및 대기 오염은 광업, 정유 공장, 발전소, 제지 산업 및 비료 산업 등에서의 폐기물의 유출로 인해 심각한 환경문제로 주목받고 있다.1-4 중금속 물질은 유기 오염 물질과는 다르게 분해가 되지 않으며 낮은 농도에서도 독성이 매우 강하여 인체에 장애 및 질병을 유발시킬 수 있다. 인체에 유해한 영향을 미치는 다양한 중금속 중에서 수은은 생물학적 조직에 축적될 수 있기 때문에 가장 치명적인 오염 물질 중 하나로 간주된다.2,5 수은은 금속원소, 무기 수은 및 유기 화합물 등 3가지 형태로 존재할 수 있으며, 이 중 무기 수은은 주로 광산에서의 채굴 작업과 공장에서의 연소 등으로 발생하여 호흡기를 통해 체내에 유입되며, 유기 수은은 섭취를 통해 체내로 유입되어 신장 및 중추신경 장애 등을 유발한다.
우리나라의 경우 1980년대 말까지 석탄 연료를 주원료 원으로 사용한 관계로 미국 환경보호국이 제시하고 있는 폐수에 대한 배출 한계인 10.0 g/L와 음용수에 대한 최대 허용 농도인 1.0 g/L을 초과하는 수십 g/L 수준의 고농도 수은이 검출되었으며 지금도 발전 시설, 폐기물 소각장과 여러 산업 공정을 통하여 수은이 배출되는 것으로 보고되고 있다.6-8 다양한 경로로 대기로 배출되는 수은은 대기 오염 문제뿐만 아니라 토양과 수질 오염으로까지 확대되어 여러 가지 환경 및 인체에 유해성을 일으킬 수 있는 것으로 알려져 있다. 따라서 폐수와 음용수에서 수은을 효과적으로 제거하는 것은 매우 중요한 문제라 할 수 있다.
폐수에서 수은을 제거하기 위하여 이온교환, 역삼투, 침전법, 흡착법, 전착(electrodeposition), 미생물을 이용한 생물학적 처리법 및 화학적 침전 등의 다양한 방법이 사용되고 있는데,1,2,9-12수은 제거 방법 중 침전법과 생물학적 처리법은 낮은 효율과 부산물인 슬러지 발생 등의 단점이 있다.13 이러한 단점을 극복하기 위하여 주로 흡착법이 사용된다. 흡착법은 공정적인 측면에서 매우 단순하며 저비용으로 수은 이온을 제거할 수 있어서 가장 널리 사용되고 있다. 흡착법에 사용되는 흡착체에서 흡착을 관장하는 흡착제로는 주로 작용기로 -SH(thiol), -NH2(amine)과 아세틸렌 등의 작용기를 가지는 물질들이 사용되며, 이들을 고정화시킬 수 있는 담지체를 합성하여 수은 이온 제거에 관한 연구가 많이 진행되었다.14-16 수은 제거를 위한 흡착체 합성을 위한 담지체로는 활성 탄소(activated carbon), 화학적으로 처리된 multi-walled carbon nanotube(MWCNT) 및 그래핀(graphene), 실리카, 고분자 레진(polymer resin), 다공성 물질 등을 이용하여 흡착제를 고정화하는 연구가 주로 진행되었다.17-22 이들 흡착체를 제조하는 담지체 중 활성 탄소와 다공성 물질에 담지된 흡착제를 사용하여 수은을 제거하는 방법이 가장 널리 사용되고 있지만, 이들은 비용적인 측면에서 가격이 높으며 유독 물질을 사용한다는 단점이 있다.
본 연구에서는 상업적인 측면을 고려하여 쉽게 구할 수 있는 유리섬유의 한 종류인 glass web을 사용하여 흡착체를 제조하여 수은 이온 제거 실험을 진행하였다. 흡착 성능의 비교를 위하여 amine 작용기를 말단에 가지는 (3-aminopropyl) trimethoxysilane(APTMS)와 알킬 그룹만을 가지는 trimethoxy (octyl)silane(TMOS)로 표면을 처리한 glass web을 제조하여 전자 주사 현미경(scanning electron microscope; SEM), 푸리에 변환 적외선(Fourier transform infrared, FTIR) 분광법과 X-선 광전자 분광법(X-ray photoelectron spectroscopy; XPS)을 이용하여 수은 이온 제거에 관한 연구를 수행하였다.
재료. 메탄올, 아세톤, APTMS, TMOS 등은 Sigma-Aldrich에서 구매하여 정제 없이 사용하였으며, glass web은 ㈜보우에서 제공받아 세척 없이 사용하였다.
Glass Web 흡수체의 제조. 10.0 cm×10.0 cm의 크기로 glass web을 자른 후 표면 개질을 위한 첫 번째 과정으로 glass web의 표면에 수산화기(-OH)를 도입하기 위하여 piranha 용액(황산:과산화수소수 = 2:1(v/v))에서 10분을 처리하고 탈이온수(DI water)를 이용하여 충분히 세척하였다. 이후 APTMS와 TMOS로 glass web 표면을 개질하기 위하여 각각 3 wt%의 APTMS와 TMOS 메탄올 용액에 12시간 동안 담가 놓았다(Figure 1(c) 참조). 표면 개질을 마친 APTMS로 개질된 흡수체와 TMOS로 개질된 흡수체를 메탄올과 아세톤을 이용하여 초음파 세척을 하여 미반응 APTMS와 TMOS를 제거하였다.
분석 및 특성평가. 흡수체의 지지체로 사용된 galss web의 표면은 전자 주사 현미경(SEM, Hitachi S4800)을 이용하여 관찰하였다. 또한 흡수제로 사용된 APTMS와 TMOS의 지지체 표면에 표면 개질된 정도를 확인하기 위하여 제조된 흡수체를 희석 총 반사율 분광법(ATR, attenuated total reflectance spectroscopy, golden gate diamond)을 포함한 FTIR(BOMEM DA8)로 2000-800 cm-1의 파장 범위 내에서 분석하였다. 흡수체의 표면은 XPS를 이용하여 분석하였다. XPS 측정 시 챔버의 압력은 1×10-9 torr, X-선 광원으로는 단색화된 Al-Ka(hυ = 1486.7 eV)를 사용하여 분석하였으며, 측정에 사용된 spot 크기는 400 μm를 사용하였다.
제조된 흡착체의 수은 제거 능력을 확인하기 위하여 배치 흡착법을 사용하였다. HgCl2를 탈이온수에 용해하여 수은 함유 용액을 제조한 후, 제조된 흡착체를 1.0 cm×1.0 cm 크기로 잘라 수은 함유 용액에 담근 후 150 rpm, 25 oC에서 2시간 동안 항온 처리기에서 교반하여 수은 이온과 흡착체의 흡착제와 반응을 시켰다. 흡착체를 수은 함유 용액에서 제거한 후 ICP-OES 분석을 이용하여 초기의 수은 함유 용액에서 남아 있는 수은 농도를 측정하였다.
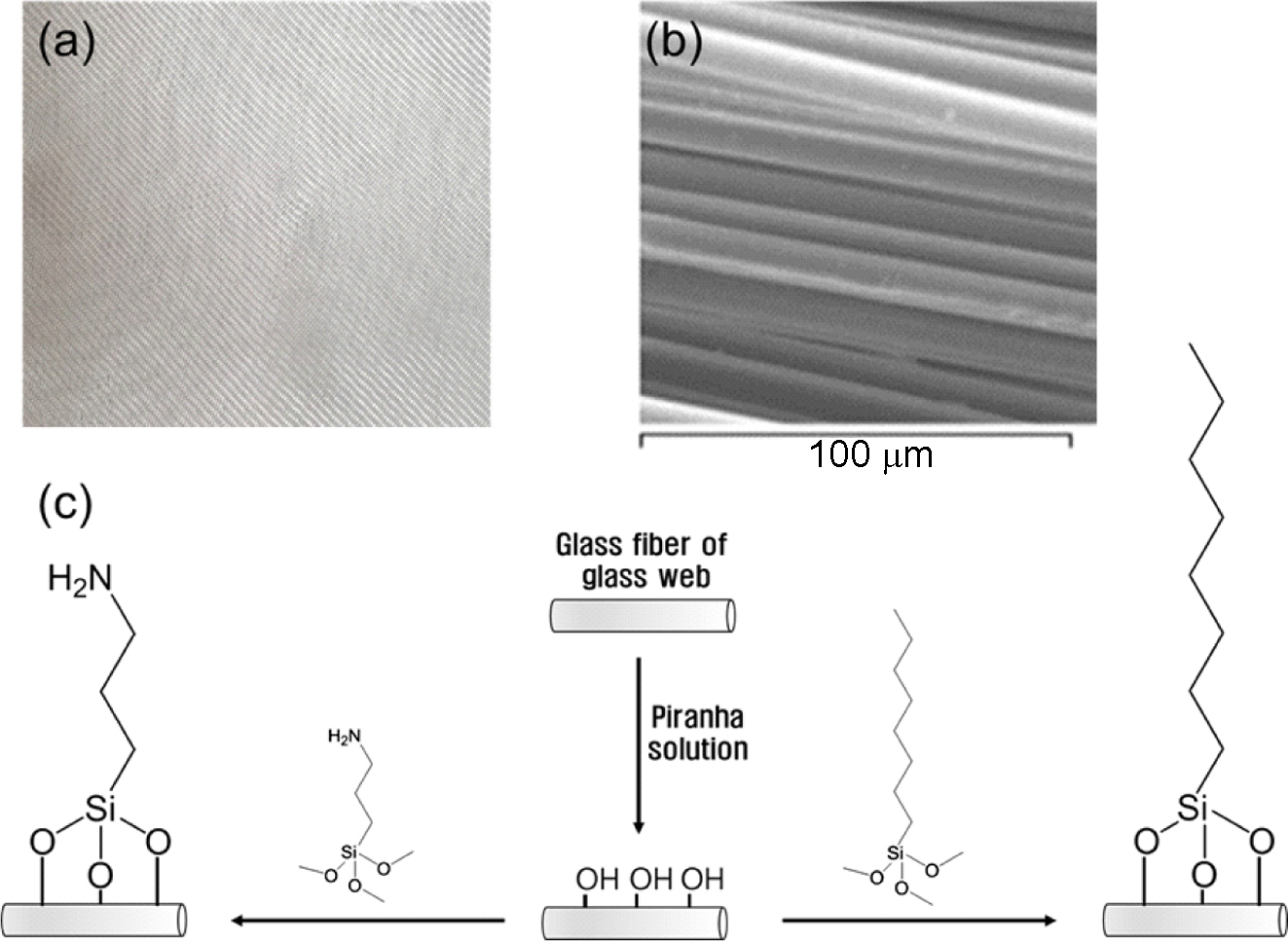
|
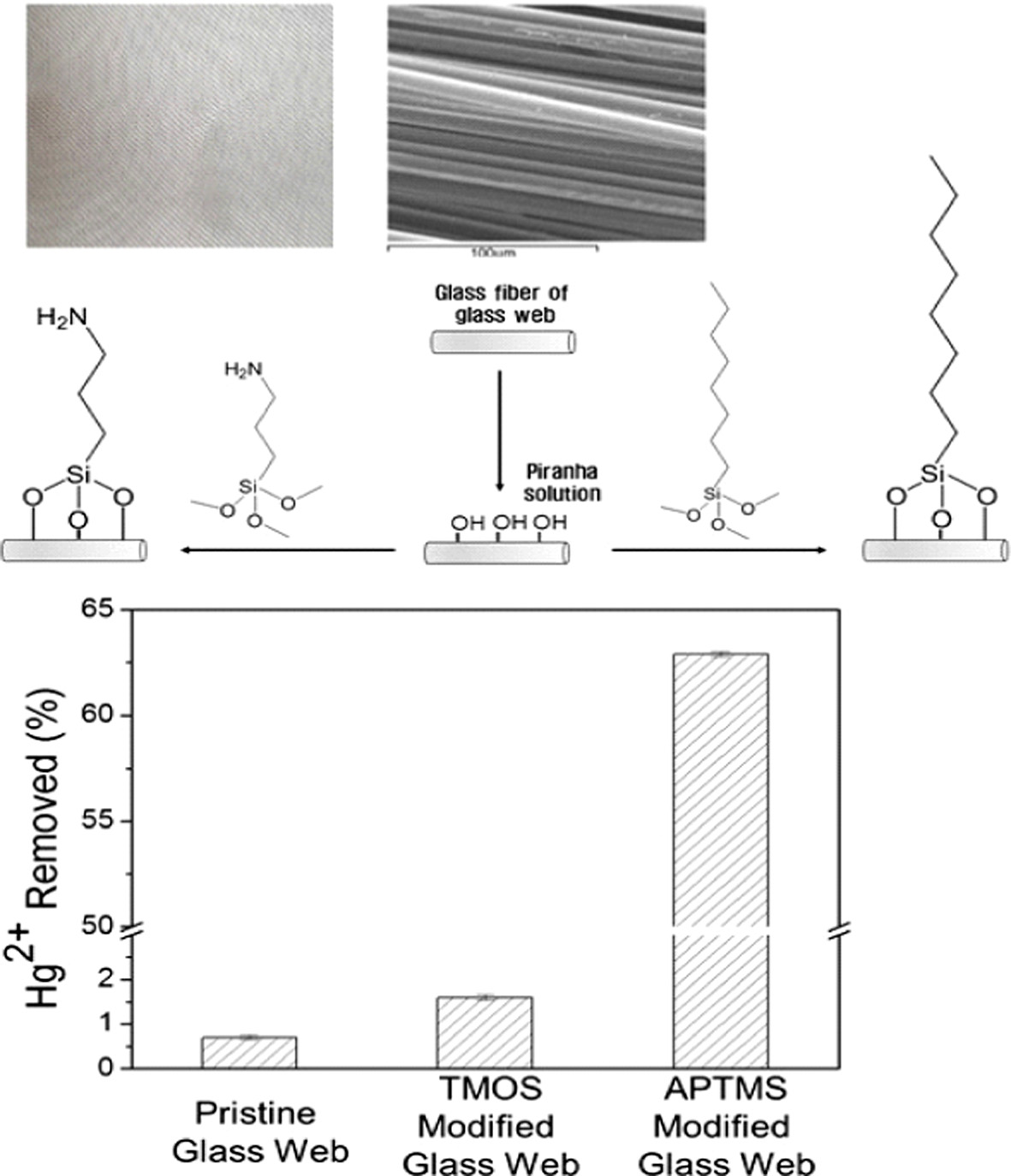
Figure 1 (a) Optical microscope image of the glass web; (b) Scanning electron microscope image of the glass web; (c) Surface modification of the glass web. |
Glass web의 광학현미경과 전자 주사 현미경을 이용하여 관찰한 결과를 각각 Figure 1(a)와 (b)에 나타내었다. Figure 1(b)와 같이 glass web을 구성하는 섬유의 두께는 대략 10 μm인 것을 확인하였다.
Figure 2에 pristine glass web과 APTMS 및 TMOS로 표면을 개질한 glass web을 ATR-FTIR로 측정한 spectrum들을 나타내었다. Pristine glass web에서 유리섬유의 특징적인 Si-O-Si 신축 진동(stretching vibration)에 해당하는 800-1200 cm-1의 사이에 나타나며 최대 흡수는 900 cm-1에서 피크의 형태로 나타남을 확인할 수 있다.23-25 APTMS와 TMOS로 표면을 개질한 glass web에서는 Si-O-Si 신축 진동을 보이며 1100 cm-1에서 shoulder 형태의 밴드가 나타나는 것을 확인하였으며 이는 실란 화합물들의 반응 때문에 생성된 Si-O 피크라 판단된다.23-25 특징적으로 pristine glass web에서는 관찰되지 않던 메틸렌 그룹(-CH2-) stretching에 해당하는 피크가 2900 cm-1 근처에서 나타나는 것을 확인할 수 있다. 또한 APTMS와 TMOS로 표면 처리한 glass web에서는 1458과 1379 cm-1에서 약한 피크가 관찰되는데 이는 각각 Si-C와 C-H의 진동에 의해서 나타나는 것을 확인하였다.26,27 특히, APTMS로 표면을 처리한 glass web에서는 1647 cm-1에서 pristine glass web과 TMOS로 표면 처리된 glass web에서는 보이지 않는 특징인 -NH2의 bending에 의한 피크가 관찰됨을 확인할 수 있다.28
ATR-FTIR로 측정된 pristine glass web과 APTMS 및 TMOS로 표면을 개질한 glass web의 보다 면밀한 표면 조성 분석을 위하여 XPS를 측정하였으며, 그 결과로 얻어진 spectrum 들을 Figure 3에 나타내었다. Figure 3(a)와 같이 pristine glass web에서 Si 2p, C 1s 및 O 1s에 해당되는 결합에너지가 각각 107.09, 288.97과 544.98 eV에 나타난다. 이러한 결과는 glass web이 실리콘, 탄소 및 산소로 이루어짐을 의미한다.29 또한 APTMS로 표면을 개질한 glass web에서는 탄소의 조성이 증가하는 것을 확인할 수 있는데 이는 APTMS의 propylene 그룹의 메틸렌에 의해 증가한 것이다. 그리고 APTMS의 -NH2에 의해 나타나는 N 1s에 해당하는 결합 에너지 피크가 402.06 eV에 나타나는 것을 확인할 수 있다. TMOS로 표면을 개질한 glass web에서는 pristine glass web과 APTMS로 표면을 개질한 glass web보다 탄소의 조성이 더 증가하는 것을 확인할 수 있는데 이는 TMOS가 가지는 octyl 그룹의 메틸렌과 메틸에 의해 증가한 것이다.
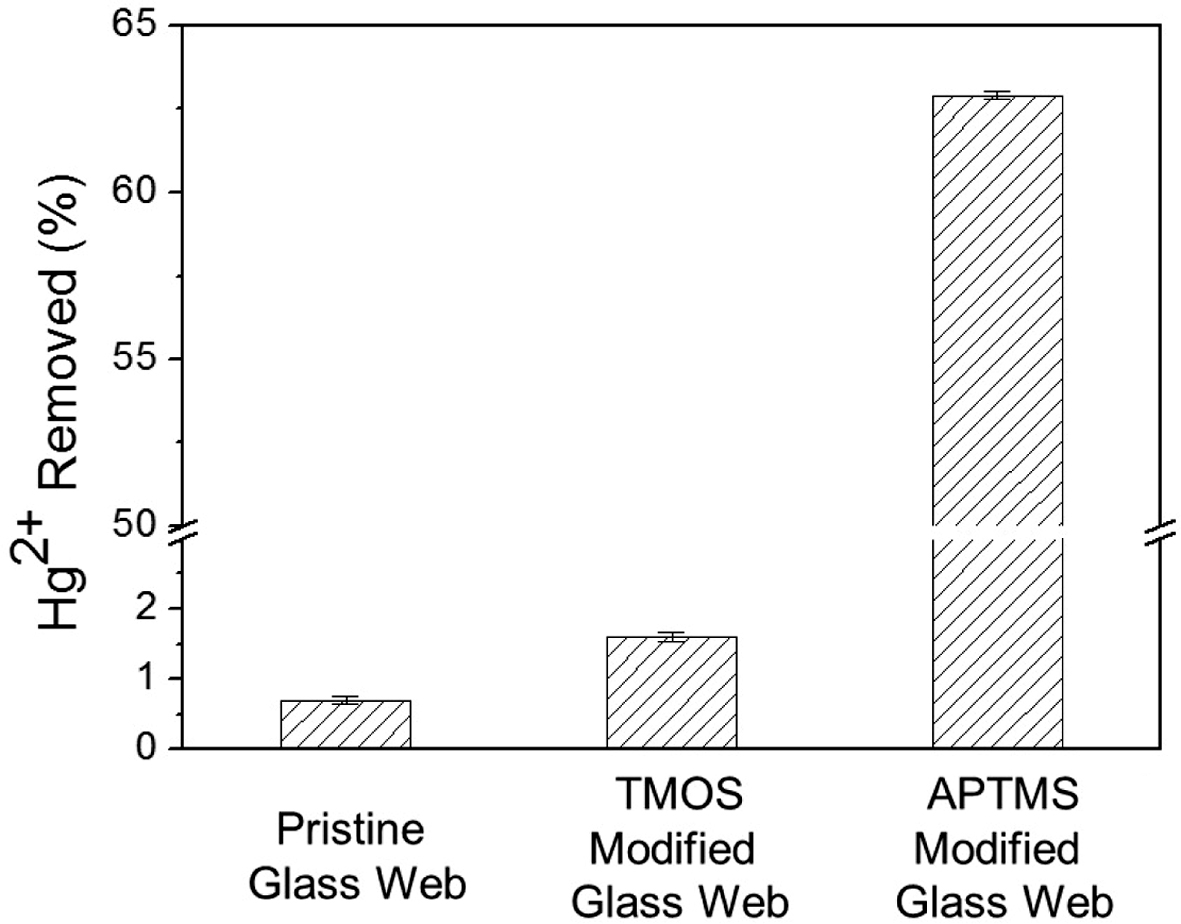
제조된 흡착체의 수은 제거 능력을 ICP-OES 분석을 통하여 잔존 수은 농도를 측정하였으며, 측정된 결과를 Figure 4에 나타내었다. 측정 결과 pristine glass web은 수은 이온을 0.7% 제거할 수 있는 것을 확인하였다.
APTMS 및 TMOS로 표면을 개질한 glass web은 각각 60.3와 1.6%의 수은 이온을 제거할 수 있음을 확인했다. 이러한 결과는 TMOS의 알킬 그룹은 수은 이온과 특정한 결합을 생성할 수 없지만, APTMS를 흡수제로 사용하는 경우 전자가 풍부한 질소 원자의 비공유 전자쌍이 수은 이온에 전자를 제공하여 결합을 형성하기 때문이라 추정된다.
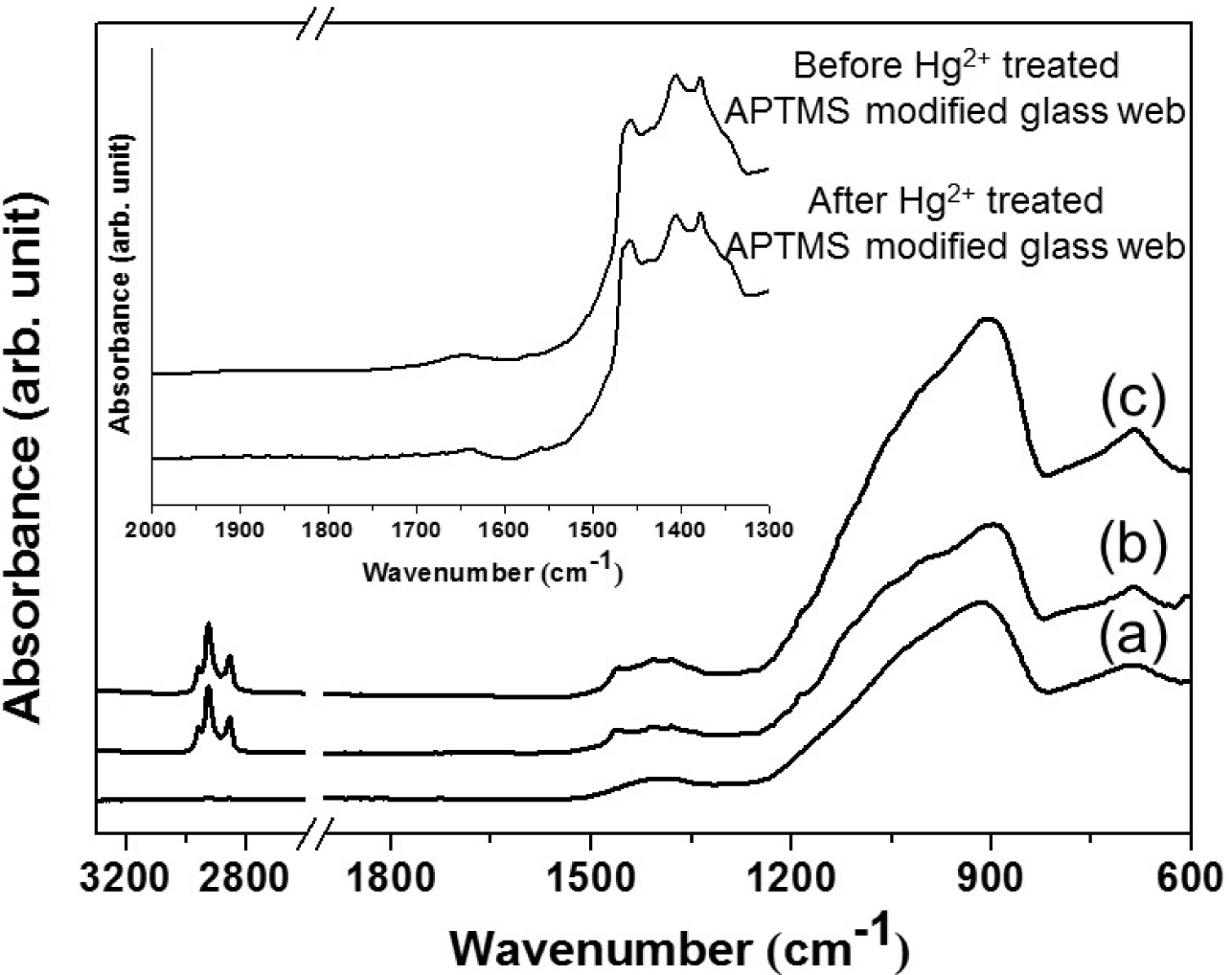
수은 이온 제거 실험 후의 흡수체들에 대하여 ATR-FTIR을 측정하였으며, 그 결과를 Figure 5에 나타내었다. 수은 함유 용액에서 반응을 마친 후 측정한 흡수체들의 ATR-FTIR spectrum은 pristine glass web과 TMOS로 표면을 개질한 glass web에서는 Figure 2의 수소 이온 제거 이전의 spectrum과 차이가 없음을 알 수 있다. 하지만, APTMS로 표면이 개질된 흡수체의 spectrum에서는 수은 이온 제거 이전에 1647 cm-1에서 나타나는 -NH2의 bending에 의한 피크가 수은 이온 제거 이후에는 낮은 파수인 1634 cm-1로 이동하는 현상을 관찰할 수 있다. 이러한 변화는 -NH2에 있는 질소 원자의 비공유 전자쌍이 수은 이온에 전자를 제공하여 결합을 형성하기 때문이라 추정되며, 이는 수은 이온의 제거 실험 결과와도 일치된다고 판단된다.6,30
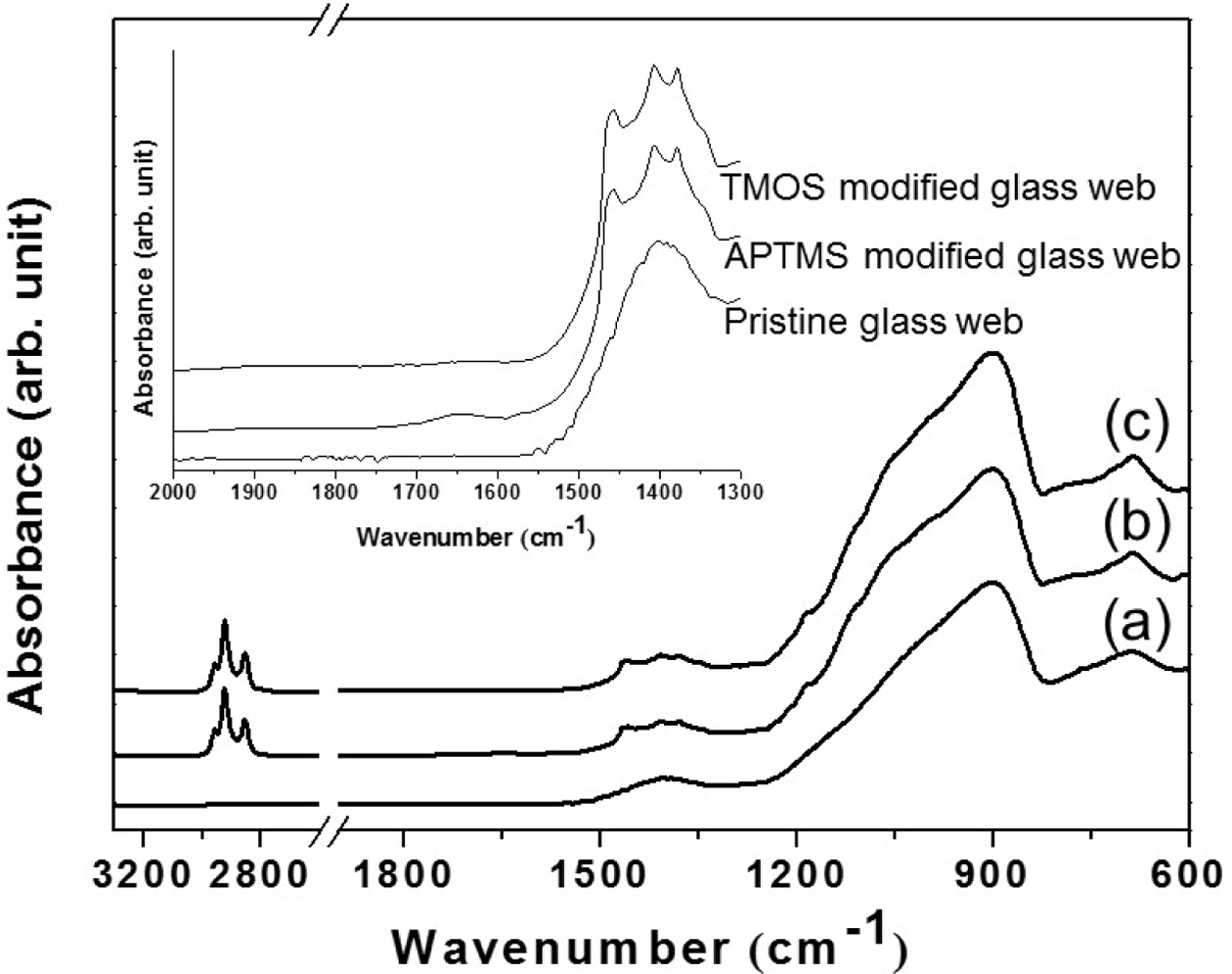
|
Figure 2 ATR-FTIR spectra of (a) pristine glass web; (b) APTMS- modified glass web; (c) TMOS-modified glass web. The inset shows a magnification of ATR-FTIR in the range of 2000-1300 cm-1. |
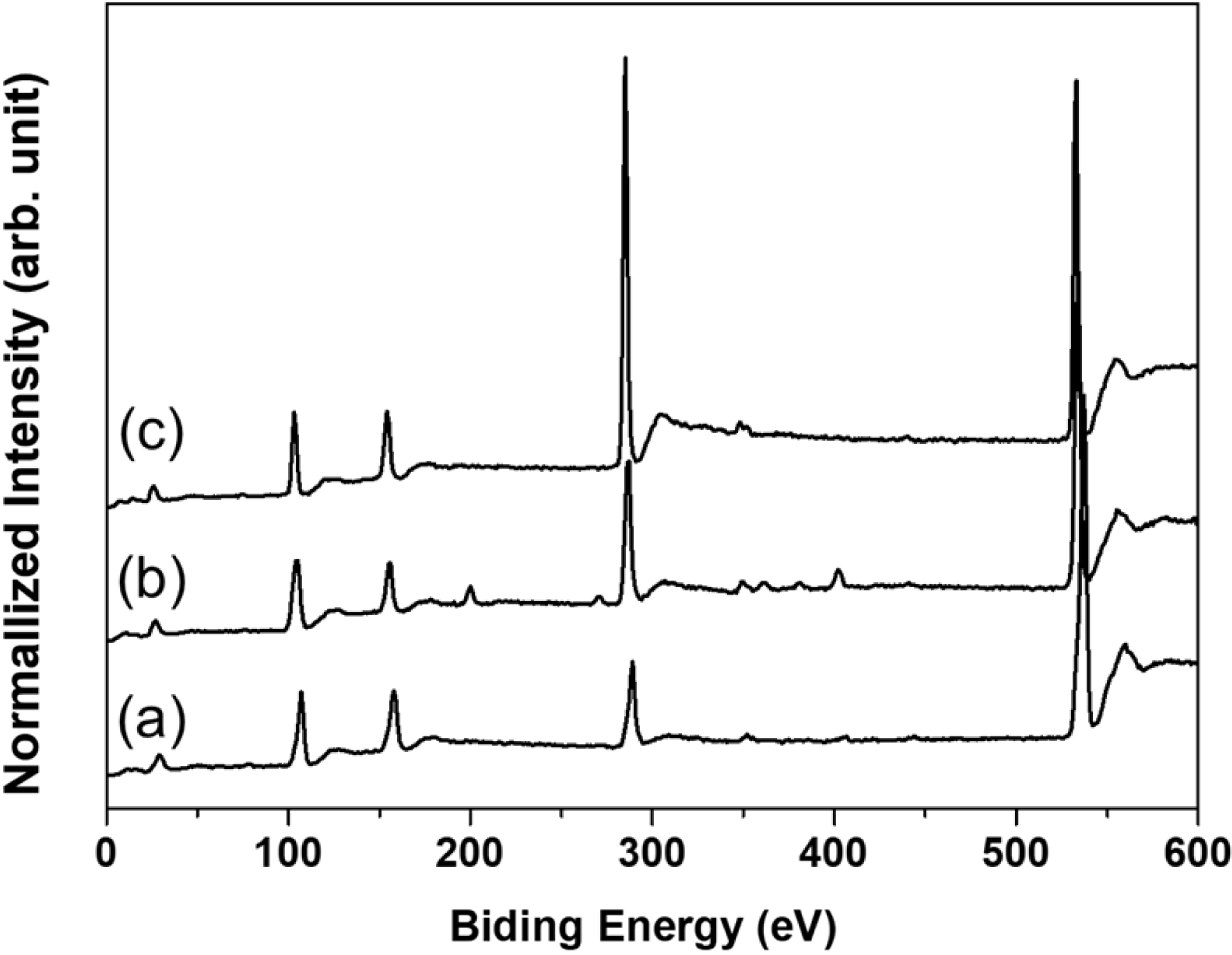
|
Figure 3 XPS spectra of (a) pristine glass web; (b) APTMS-modified glass web; (c) TMOS-modified glass web. |
|
Figure 4 Quantitative analysis of mercury ion removal using pristine glass web, APTMS-modified glass web, and TMOS-modified glass web. |
|
Figure 5 ATR-FTIR spectra of (a) pristine glass web; (b) APTMS- modified glass web; (c) TMOS-modified glass web after treatment in the mercury contaminated water. The inset shows a comparison of APTMS-modified glass web before and after Hg2+ treatment. |
본 연구를 통해 해로운 중금속인 수은 이온을 제거하기 위하여 glass web에 말단에 아민 그룹을 가지는 APTMS와 알킬 그룹을 가지는 TMOS를 흡수제로 표면에 가지는 흡수체를 습식 방법에 따라 제조하였다. 제조된 흡수체의 표면에 APTMS와 TMOS가 고정화되었는지는 ATR-FTIR과 XPS 분석을 통하여 확인하였으며, APTMS의 아민 그룹과 TMOS의 알킬그룹이 glass web의 유리섬유에 잘 고정화된 것을 확인할 수 있었다. 수은 이온의 제거 능력을 비교하기 위하여 glass web과 APTMS와 TMOS를 표면에 가지는 glass web을 ICP-OES 분석을 통하여 실험하였으며, 실험 결과 APTMS 표면 처리 glass web > TMOS 표면 처리 glass web > glass web의 순서로 중금속 수은 이온을 제거할 수 있음을 확인하였다. 또한 수은 이온과 반응한 후 ATR-FTIR을 측정한 결과 분자 수준에서 APTMS 표면 처리 glass web은 변화가 있음을 확인할 수 있었으며, 이는 수은 이온의 처리 능력과 관계가 있음을 확인하였다.
- 1. M. Ahmaruzzaman, Adv. Colloid Interface Sci., 166, 36 (2011).
-

- 2. J. M. Choi, D. Jeong, E. Cho, B.-H. Jun, S. Park, J.-H. Yu, M. N. Tahir, and S. Jung, J. Ind. Eng. Chem., 35, 376 (2016).
-

- 3. M. McNutt, Science, 341, 1430 (2013).
-

- 4. W. F. Fitzgerald and T. W. Clarkson, Environ. Health Perspect., 96, 159 (1991).
-

- 5. J. H. Pavlish, M. J. Holmes, S. A. Benson, C. R. Crocker, and K. C. Galbreath, Fuel Process. Technol., 85, 563 (2004).
-

- 6. S. Huang, C. Ma, Y. Liao, C. Min, P. Du, and Y. Jiang, J. Nanomater., 2016, Article ID 7245829 (2016).
-

- 7. J. Wang, B. L. Deng, H. Chen, X. R. Wang, and J. Z. Zheng, Environ. Sci. Technol., 43, 5223 (2009).
-

- 8. F.-S. Zhang, J. O. Nriagu, and H. Itoh, Water Res., 39, 389 (2005).
-

- 9. H. Bessbousse, T. Rhlalou, J. F. Verchere, and L. Lebrun, J. Membr. Sci., 325, 997 (2008).
-

- 10. F. Veglio and F. Beolchini, J. Hydrometeorol., 44, 301(1997).
-

- 11. P. Miretzky and A. F. Cirelli, J. Hazard. Mater., 167, 10 (2009).
-

- 12. P. C. Mishra and R. K. Patel, J. Hazard. Mater., 168, 319 (2009).
-

- 13. A. Saeed, M. Iqbal, and M. W. Akhtar, J. Hazard. Mater., 117, 65 (2005).
-

- 14. L, Bois, A. Bonhomme, A. Ribes, B. Pais, G. Raffin, and F. Tessier, Colloids Surf., A, 221, 221 (2003).
-

- 15. J. Brown, R. Richer, and L. Mercier, Micropor. Mesopor. Mater., 37, 41 (2000).
-

- 16. M. Algarra, V. Jimenez, E. R.-Castellon, A. Jimenez-Lopez, and J. Jimenez-Jimenez, Chemosphere, 59, 779 (2005).
-

- 17. T. Budinova, N. Petrov, J. Parra, and V. Baloutzov, J. Environ. Manage., 88, 165 (2008).
-

- 18. J. D. Merrifield, W. G. Davids, J. D. MacRae, and A. Amirbahman, Water Res., 38, 3132 (2004).
-

- 19. S. A. Wasay, S. Barrington, and S. Tokunaga, Water Air Soil Pollut., 116, 449 (1999).
-

- 20. K. Hristovski, A. Baumgardner, and P. Westerhoff, J. Hazard. Mater., 147, 265 (2007).
-

- 21. A. Vaseashta, M. Vaclavikova, S. Vaseashta, G. Gallios, P. Roy, and O. Pummakarnchana, Sci. Technol. Adv. Mat., 8, 47 (2007).
-

- 22. Y. C. Sharma, V. Srivastava, V. K. Singh, S. N. Kaul, and C. H. Weng, Environ. Technol., 30, 583 (2009).
-

- 23. F. N. Mutua, P. Lin, J. K. Koech, and Y. Wang, Mater. Sci. Appl., 3, 856 (2012).
-

- 24. A. J. Bonon, M. Weck, E. A. Bonfante, and P. G. Coelho, Mater. Sci. Eng. C, 69, 905 (2016).
-

- 25. V. M. Maldonado, L. S. A. Torres, F. H. Barceló-Santana, R. D. Vanegas-Lancón, M. E. Plata-Rodríguez, and V. M. Castaño, J. Appl. Polym. Sci., 126, 289 (2012).
- 26. M. Baranowsaka, A. J. Slota, P. J. Eravuchila, M. Alba, P. Formentin, J. Pallaes, J. F-Borrull, and L. F. Marsal, J. Colloid Interface Sci., 452, 180 (2015).
-

- 27. A. S. Zakirov, R. Navamathavan, Y. J. Jang, A. S. Jung, C. K. Choi, and K.-M. Lee, J. Korean Phys. Soc., 50, 1809 (2007).
-

- 28. G. Giani, S. Fedi, and R. Barbucci, Polymers, 4, 1157 (2012).
-

- 29. H. H. Kyaw, S. H. Al-Harthi, A. Sellai, and J. Dutta, Beilstein J. Nanotechnol., 6, 2345 (2015).
-

- 30. Y. Nuhoglu and E. Malkoc, Bioresour. Technol., 100, 2375 (2009).
-

- Polymer(Korea) 폴리머
- Frequency : Bimonthly(odd)
ISSN 0379-153X(Print)
ISSN 2234-8077(Online)
Abbr. Polym. Korea - 2023 Impact Factor : 0.4
- Indexed in SCIE
 This Article
This Article
-
2019; 43(5): 793-797
Published online Sep 25, 2019
- 10.7317/pk.2019.43.5.793
- Received on Jul 1, 2019
- Revised on Jul 30, 2019
- Accepted on Aug 5, 2019
 Services
Services
Shared
 Correspondence to
Correspondence to
- No-Kuk Park, and Seung Woo Lee
-
School of Chemical Engineering, Yeungnam University, 280 Daehak-ro, Gyeongsan, Gyeongbuk 38541, Korea
- E-mail: nokukpark@gmail.com, leesw1212@ynu.ac.kr
- ORCID:
0000-0002-6089-8970, 0000-0001-7523-5371









 Copyright(c) The Polymer Society of Korea. All right reserved.
Copyright(c) The Polymer Society of Korea. All right reserved.