- Preparation of Antioxidant Hydrogel Contact Lenses via Copolymerization of Dopamine Monomer
Department of Chemistry, Dankook University, Chungnam 31116, Korea
*Department of Chemistry, Chosun University, Gwangju 61452, Korea- 도파민 단량체 공중합을 기반으로 하는 항산화 콘택트렌즈 제조
단국대학교 화학과, *조선대학교 화학과
In this work, we prepared antioxidant hydrogel contact lenses through the copolymerization of a synthesized dopamine monomer, 2-hydroxyethyl methacrylate (HEMA), ethylene glycol dimethacrylate (EGDMA) and 2-methacryloyloxyethyl phosphorylcholine (MPC). Three contact lenses were made by varying the weight ratio (0.1%, 0.3%, 0.5%) of dopamine monomer at a 5 wt% of MPC. The prepared lenses exhibited visible light transmittance values higher than 90%. In addition, they exhibited high water contents of about 50% and low contact angles (55o-63o), which indicated excellent hydrophilicity. The antioxidant activities were evaluated using 2,2-diphenyl-1-picrylhydrazyl (DPPH) radical scavenging assay. The antioxidant lenses removed most of DPPH radicals within 1 h. The measured antioxidant activities are comparable to 98% of ascorbic acid. Consequently, the prepared antioxidant contact lenses showed excellent antioxidant activities, although a small amount of dopamine group was employed.
도파민 단량체를 합성한 후, 2-hydroxyethyl methacrylate(HEMA), ethylene glycol dimethacrylate(EGDMA), 2-methacryloyloxyethyl phosphorylcholine(MPC)과의 공중합을 통해 항산화 콘택트렌즈를 제조하였다. 렌즈 합성 시, 도파민 무게%를 0.1, 0.3, 0.5%로 조절하였고, MPC는 5%로 고정하여, 3종의 렌즈를 준비하였다. 제조된 렌즈들은 90% 이상의 가시광선 투과율을 보였다. 50% 정도의 함수율과 낮은 접촉각(55o-63o)을 통해 렌즈 친수성이 향상됨을 알 수 있었다. 라디칼 소거 분석법을 이용하여 항산화 특성을 확인한 결과, 0.1% 도파민 그룹을 포함하는 렌즈의 경우에도 반응 1시간만에 소거율이 90%까지 증가함을 알 수 있었다. 본 결과는 아스코빅산의 항산화 기능대비 98%에 해당하는 것으로, 제조된 콘택트렌즈의 우수한 항산화 능력을 나타낸다.
Antioxidant hydrogel contact lenses could be prepared by combining poly(2-hydroxyethyl methacrylate) with antioxidant dopamine group. The dopamine-based contact lenses showed an excellent radical scavenging capability, which is comparable to that of ascorbic acid.
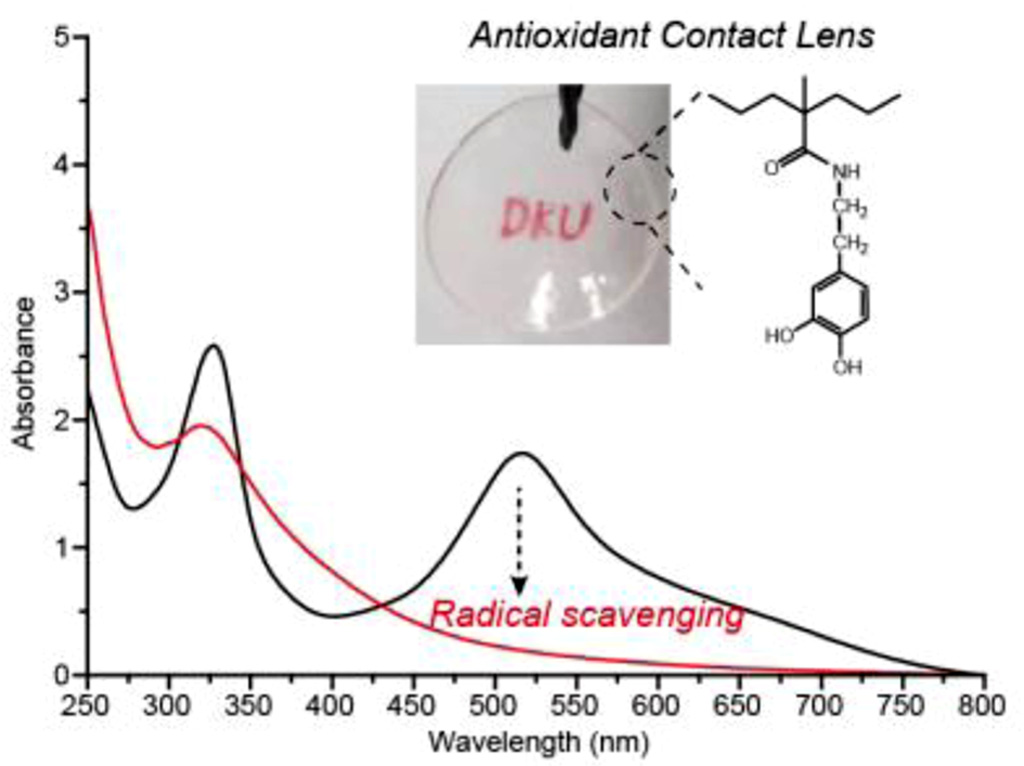
Keywords: hydrogel, contact lenses, antioxidant, dopamine, radical scavenging assay
Poly(2-hydroxyethyl methacrylate) (polyHEMA)로 이루어진 가교 고분자는 함수율, 기계적 물성, 생체 적합성이 뛰어나기 때문에, 수화젤 콘택트렌즈(hydrogel contact lens) 소재로 사용되고 있다.1 수화젤 콘택트렌즈는 시력교정 및 미용 목적 영역으로 확대되고 있고, 최근에는 광변색, 청색광 차단, 단백질 비흡착과 같은 유용한 기능성을 구현할 수 있는 수화젤 렌즈 개발에 관한 연구들이 진행되고 있다.
최근 전자 기기의 장시간 사용에 따른 안구 내 히드록실 라디칼, 수퍼옥사이드 라디칼, 일중항산소와 같은 활성 산소 종들의(reactive oxygen species, ROS)의 생성, 축적이 야기되고, 이는 안구 질환의 원인이 될 수 있다. 과산화 음이온 라디칼로 알려진 활성 산소 종들은 상처 치유 과정에서 중요한 역할을 수행하는 것으로 알려져 있으나,2-4 자외선, 청색광 노출과 같은 조건 하에서 활성 산소 농도가 비이상적으로 증가될 경우, 정상 세포마저도 손상시켜, 염증반응을 야기시킨다.5 따라서 렌즈를 장시간 착용하게 되면, 렌즈 근처에서 생성되는 활성산소가 안구에 축적되고, 시력을 담당하는 황반 주변 세포가 파괴될 수 있다.
항산화 물질 중, 폴리페놀 계열 물질들은 매우 우수한 항산화 특성을 나타내는 것으로 잘 알려져 있다. 일례로, 갈릭산 및 도파민 화합물들의 경우, 방향족 고리에 위치해있는 하이드록시 그룹이 자유 라디칼 반응을 차단함으로써, 활성 산소의 유해성을 방어할 수 있다.6,7 따라서 활성 산소를 효과적으로 제거할 수 있는 항산화 폴리페놀 물질을 수화젤 콘택트렌즈에 도입하는 기능성 렌즈 제조는 매우 흥미로운 연구분야라 할 수 있다. 그러나 항산화 콘택트렌즈가 폴리페놀 물질과 수화젤 고분자와의 물리적 혼합을 통해 제조될 경우, 사용 시간이 경과함에 따라 항산화 물질의 방출로 인한 기능 저하 문제를 피할 수 없다.8,9 실제로, 항산화 케프세틴을 polyHEMA와 혼합하여 항산화 수화젤을 제조한 연구결과가 보고된 바 있으나,10 물질 유출의 문제점이 지적된 바 있다. 따라서 지속적인 항산화 기능을 유지하기 위해서는 항산화 물질을 수화젤 구조 내부에 화학적으로 고정시킬 필요가 있다. 최근 본 연구팀의 경우, polyHEMA 수화젤에 키토산 네트워크를 물리적 가교를 통해 도입한 후, 화학반응을 통해 폴리페놀 일종인 갈릭산을 도입하여 항산화 polyHEMA 수화젤 물질을 제조하였다.11 본 방법은 항산화 물질을 화학적으로 고정시켜 유출의 문제를 해결할 수 있으나, 수화젤 제조 후 다단계의 공정 과정이 필요하다는 한계가 있다. 콘택트렌즈 제조는 일반적으로 용매가 없는 조건인 벌크 상에서 공중합을 통해 이루어지기 때문에, 항산화 물질을 단량체로 합성한 후, 공중합에 적용시킬 경우, 기존 콘택트렌즈 제조 공정의 변형 없이, 항산화 기능성을 콘택트렌즈에 안정적으로 도입할 수 있을 것으로 예상된다. 그럼에도 불구하고, 현재까지 폴리페놀 계열의 항산화 물질을 수화젤 콘택트렌즈에 공중합을 통해 도입된 사례는 보고된 바 없다.
이러한 연구 배경을 토대로, 본 논문에서는 폴리페놀의 일종인 도파민 화합물에 중합기를 도입하여 도파민 단량체를 합성하였고, 이후 수화젤 콘택트렌즈 제조에 사용되는 단량체들과의 공중합을 통해 도파민이 화학적으로 결합되어 있는 수화젤 콘택트렌즈를 개발하였다. 본 연구에서는 도파민 단량체의 중량%를 0.1%(렌즈 1), 0.3%(렌즈 2), 0.5%(렌즈 3)로 변화시켰으며, 모든 렌즈 시료에 대해 단백질 비흡착 및 렌즈 착용감 향상을 위해 생체적합성이 뛰어난 2-methacryl-oyloxyethyl phosphorylcholine(MPC)의 중량%를 5%로 고정하여 공중합을 수행하여, 3종의 항산화 콘택트렌즈를 제조하였다. 제조된 시료들의 함수율, 접촉각, 평균 가시광선 투과율 등과 같은 렌즈 특성 및 항산화 능력을 비교 분석하였다.
재료. 본 연구에 사용된 시약들인 2-hydroxyethyl meth-acrylate(HEMA), dopamine hydrochloride, ethylene glycol dimethacrylate(EGDMA), 2,2-azobis(2-methylpropionitrile) (AIBN), 2,2-diphenyl-1-picrylhydrazyl(DPPH), Na2B4O7·10H2O, methacrylic anhydride, 2-methacryloyloxyethyl phosphoryl-choline(MPC)를 Sigma-Aldrich사로부터 구입하여 정제없이 사용하였다.
도파민 단량체 합성.12 10 g의 Na2B4O7·10H2O와 5 g의 Na2CO3을 탈염수 200 mL를 이미 넣은 500 mL 플라스크에 첨가한 후, 1시간 동안 초음파로 처리한다. 이후, 질소를 충전시킨 후, 5 g의 dopamine hydrochloride를 넣고 30분간 교반한다. 본 용액과 따로, 4 mL의 methacrylic anhydride를 21 mL의 tetrahydrofuran(THF)에 넣어 용액을 제조한다. 0도에서, dopamine을 함유하는 용액에 methacrylic anhydride을 함유하는 용액을 천천히 가한 후, 1 M NaOH용액을 이용하여 pH를 9로 유지하면서, 12시간 동안 교반한다. 이후, 6 N HCl 용액을 이용하여, pH를 1-2로 만들고, 1시간 동안 교반한다. 다음으로, ethyl acetate로 추출하고, hexane으로 재결정하여 도파민 단량체를 정제한다. 수율: 80%. 1H NMR (500 MHz, DMSO-d6, d, ppm): 8.64 (s, 2H, -OH), 7.92 (t, 1H, -NHC=O), 6.43-6.64 (m, 3H, Ph), 5.62 (s, 1H, CH2=C-CH3), 5.30 (s, 1H, CH2=C-CH3), 3.22 (m, 2H, -CH2-CH2-NH-), 2.55 (t, 2H, -CH2-CH2-NH-), 1.85 (s, 3H, CH2=C-CH3). 13C NMR (125 MHz, DMSO-d6, d, ppm): 167.34, 145.06, 143.50, 140.09, 130.31, 119.22, 118.79, 115.99, 115.49 (aromatic), 40.97, 34.61, 18.65. Mw/Mn=1.01. High-resolution 질량분석 결과, 계산값: 221.11, 측정값: 221.11 [M]+, 222.11 [M+H]+. 원소분석결과, 계산값: C, 65.14; H, 6.83; N, 6.33, 측정값: C, 65.17; H, 6.86; N, 6.33.
항산화 콘택트렌즈 제조. 중합에 사용할 혼합시료를 다음과 같이 제조하였다. 개시제인 AIBN 0.012 g과 가교제인 EGDMA 0.012 g, MPC 0.15 g(5 wt%)으로 고정하였다. 도파민 단량체의 중량%는 0.1, 0.3, 0.5%로 변화시켜가며 3종의 렌즈 시료를 제조하였다. Table 1에 나타난 바와 같이, 각 시료들을 바이알에 정량한 후, 각 혼합용액을 30분 동안 초음파 처리하였다. 준비된 혼합시료를 암형인 polypropylene (PP) 몰드에 주입한 후, 수형인 poly(butylene terephthalate)(PBT) 몰드로 덮는다. 이후, 온도를 90 oC로 유지한 오븐에서 4시간 동안 공중합을 수행하였다. 제조된 렌즈들은 동일한 두께(0.23 mm)를 나타내었다.
평균 가시광선 투과율 결정. 제조된 렌즈들의 가시광선 투과율은 흡광 스펙트럼 실험을 통해 조사하였다. 실험에 사용된 시편은 제조된 항산화 콘택트렌즈의 일부를 절단하여, 평평한 시편으로 만든 후, 2개의 투명한 슬라이드 사이에 고정시켜 UV-vis spectrophotometer(SHIMADZU UV-2600)를 이용하여 파장에 따른 가시광선 투과율을 측정하였다. 얻어진 스펙트럼의 가시광선 영역(380-780 nm)의 투과율을 평균하여, 평균 가시광선 투과율을 계산하였다.13
함수율 측정. 항산화 콘택트렌즈를 48시간 동안 과량의 물에 담근 후, 표면에 존재하는 수분을 제거한 후, 수화된 렌즈의 질량을 측정하여, 식 (1)을 통해 함수율(percentage of water content, PWC)을 얻었다. 각 시료 별로 3차례 실험을 하여, 평균값을 표시하였다.

접촉각 측정. 5 µL인 물방울을 렌즈 표면에 놓은 후, 3분 후에 HI-SCOPE/HS-300U를 이용하여, 접촉각을 측정하였다.
라디칼 소거율 측정을 통한 항산화 기능성 결정. 렌즈들의 항산화 기능성은 DPPH 용액(0.2 mM)의 라디칼 소거 정도를 UV-vis spectrophotometer(SHIMADZU UV-2600)를 이용하여 측정하여 결정하였다.14-16 DPPH 용액은 DPPH 0.079 g을 100 mL의 에탄올에 넣어 제조한 후, 10배 희석하여 사용하였다. 렌즈들을 20 mL 갈색 바이알에 각각 넣은 뒤, 0.2 mM DPPH를 각 바이알에 2.7 mL를 첨가하였다. 37 oC에서 시료들을 교반하면서 517 nm에서의 용액 흡광도 변화를 측정하였다. 아스코빅산의 경우, 0.04 M 농도의 수용액을 제조하여, 0.3 mL를 2.7 mL의 DPPH 용액(0.2 mM)에 첨가하여, 라디칼 소거율을 측정하였다.17

도파민 단량체 합성은 도파민과 중합기인 methacrylic 그룹도입을 통해 수행되었다. Methacrylic anhydride와 반응 전, 도파민을 sodium tetraborate decahydrate로 처리하였다. 본 과정은 고리형 bidentate ortho-benzene subunit을 형성시켜, 이후 아미드화 반응에서 디하이드록시 그룹을 보호하기 위함이다.18 이 후, methacrylic anhydride와의 아미드화 반응을 통해 중합기를 도입한 다음, 산 첨가를 통해 catechol 형태로 다시 전환시켰다. 합성된 도파민 그룹을 기반으로 하는 항산화 콘택트렌즈 분자 구조는 Scheme 1에 나타내었다. 렌즈 제조에 필요한 혼합시료는 Table 1에 표시된 중량비에 따라, 개시제(AIBN), 가교제(EGDMA), HEMA 단량체, 도파민 단량체, MPC를 혼합하여 제조한 후, 벌크상 공중합 과정을 통해 렌즈들을 제조하였다(Scheme 1). 수화젤 콘택트렌즈는 중합된 렌즈를 몰드로부터 분리한 후, 6시간 동안 탈염수에 넣어 제조하였다.
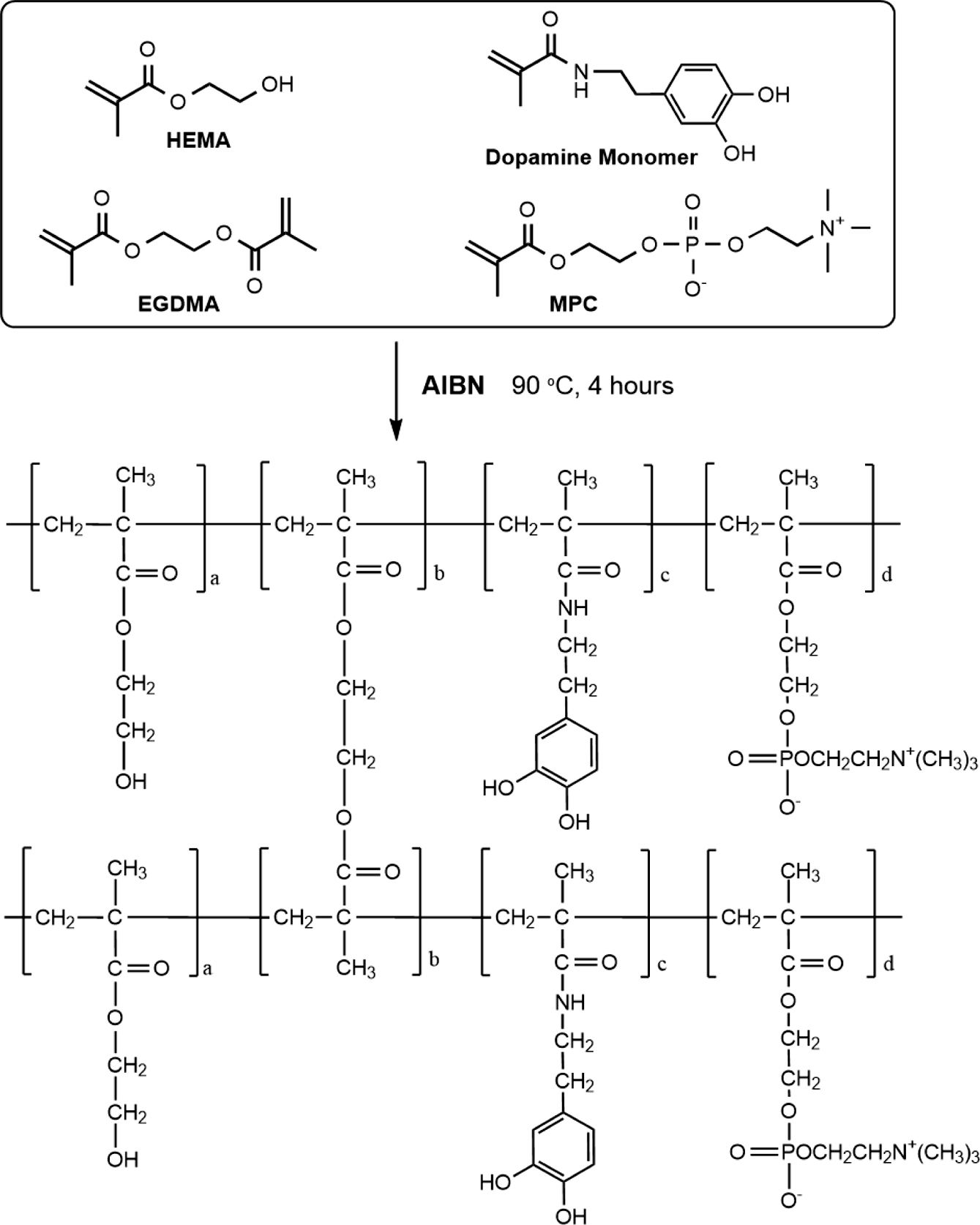
Scheme 1. Synthesis of antioxidant contact lenses via copolymerization
of HEMA, EGDMA, dopamine monomer and MPC.
일반적으로, 콘택트렌즈에 있어서 필수적인 물리적 특성 중 하나로 광학 투명도가 요구된다. 본 연구에서 항산화 콘택트렌즈들의 광학투명도는 UV-vis absorption spectroscopy를 통해 투과 스펙트럼을 얻은 후, 가시광선(파장범위: 380~780 nm) 영역에서 평균 가시광선 투과율을 계산하였다.13 Figure 1(a)에서 볼 수 있듯이, 모든 렌즈시료들은 대부분의 가시광선 영역에서 90% 이상의 높은 투과율을 나타내고 있음을 알 수 있고, 가시광선 전 영역의 평균 투과율은 97.0%(렌즈 시료-1), 94.9%(렌즈 시료-2), 95.8%(렌즈 시료-3)로 계산되었다. 분광법 결과와 유사하게, 실제 육안으로 렌즈를 관찰한 경우에도, 렌즈의 전체 면적에서 투명한 것을 알 수 있었고(Figure 1(b)), 이를 통해 높은 광학 투명도를 보인다고 해석 가능하다.
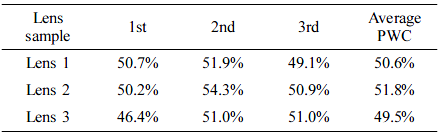
콘택트렌즈의 함수율은 평균 가시광선 투과율과 더불어 중요한 물리적 특성 중 하나로, 렌즈 착용감에 큰 영향을 미친다. 본 연구에서 항산화 렌즈의 함수율 측정은 렌즈당 3번씩 측정한 값을 평균하여 계산하였고, 얻어진 수치를 Table 2에 나타내었다. 측정 결과, 모든 렌즈 시료에서 평균 함수율이 50% 근처의 값을 나타내었다. 이는 일반 수화젤 콘택트렌즈의 함수율(38%)보다19 10% 이상 향상된 값으로, 본 항산화 콘택트렌즈 제조 시, 도입한 쌍이온 화합물인 MPC의 친수성에 기인한 결과로 해석된다.
함수율 향상과 더불어, MPC의 도입으로 인한 렌즈 표면의 친수성 변화를 살펴보기 위해, 접촉각 측정을 수행하였다. Figure 2는 항산화 콘택트렌즈의 접촉각을 측정한 결과이다. 렌즈들의 접촉각은 56~63o의 값을 나타내었다. 통상적으로 알려진 수화젤 콘택트렌즈의 경우, 접촉각이 80o 정도를 나타내는 것으로 알려져 있다.20 이같은 사실로부터 본 연구에서 제조된 렌즈들의 접촉각은 상당히 작은 값으로 평가되며, 이는 렌즈 표면의 친수성이 향상됨을 나타낸다. 이러한 렌즈 표면 친수성은 렌즈와 안구 사이에 윤활제 역할을 하는 수분의 함량을 증가시켜 착용감을 높이는 작용을 하는 것으로 알려져 있다.21
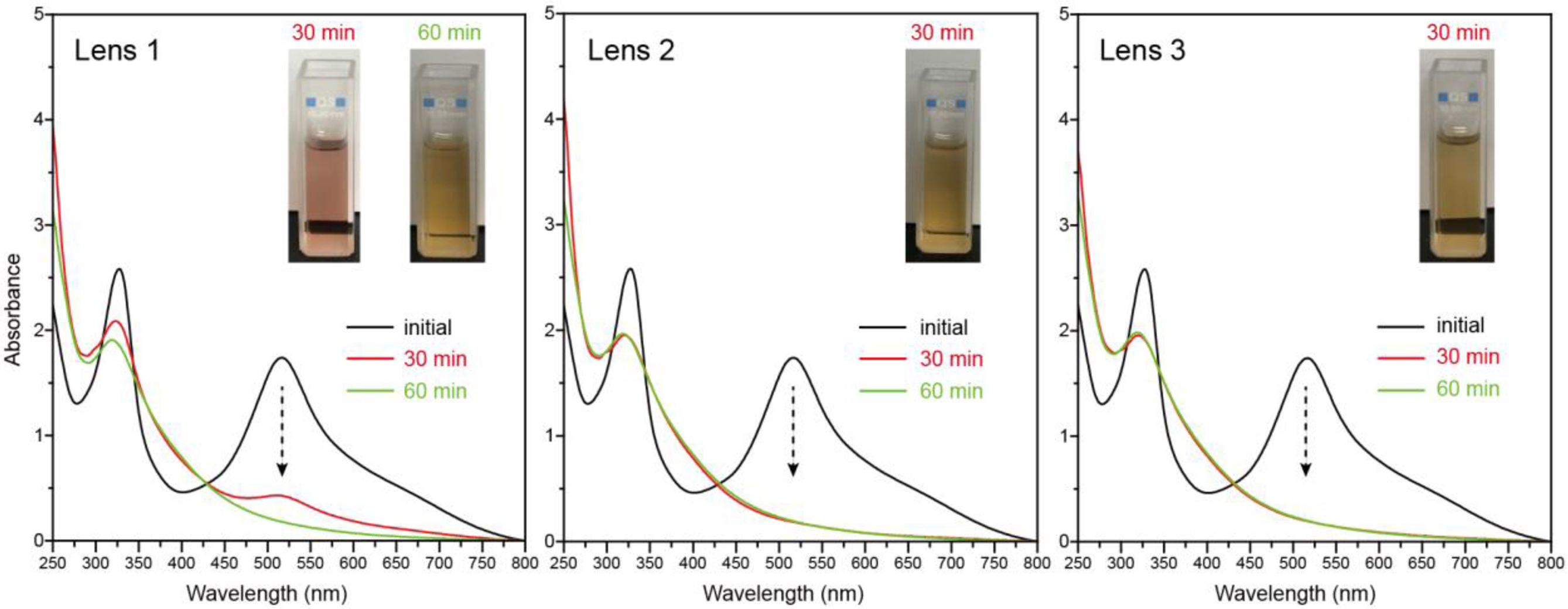
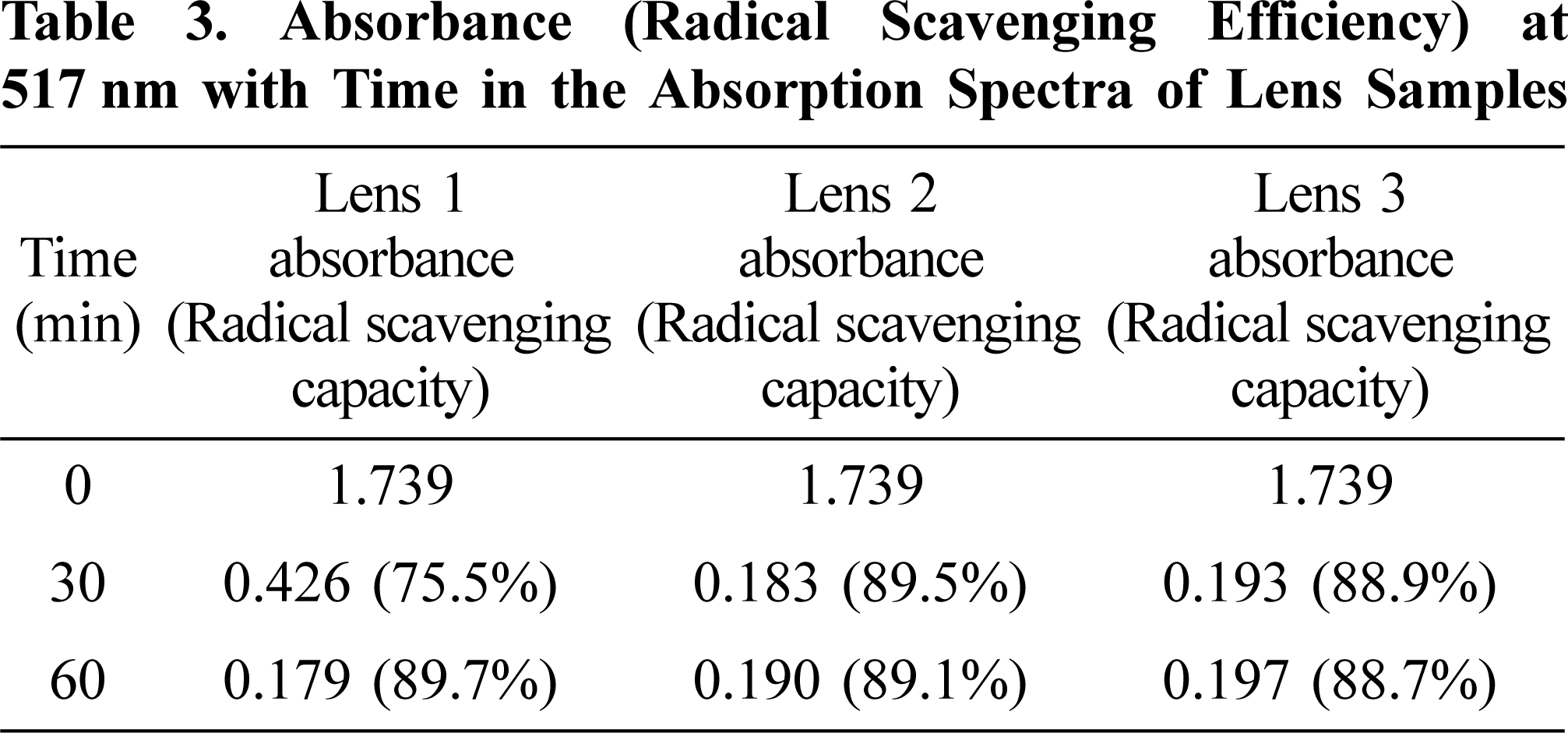
DPPH 라디칼 소거능 분석을 통해 제조된 콘택트렌즈의 항산화 기능을 결정하였다. DPPH 분석에서 렌즈의 항산화 기능성은 DPPH 라디칼의 비편재화 정도에 따라 결정된다. 흡수 스펙트럼에서 DPPH 라디칼은 517 nm 파장에서 강한 흡수 최대치를 갖기 때문에, 보라색을 나타낸다. 반면, DPPH 라디칼이 렌즈의 도파민 그룹과 반응할 경우, 도파민으로부터 수소를 받아 안정한 hydrazine(DPPH-H)로 전환되어, 517 nm에서의 흡수가 감소되는 경향을 보인다.22,23 Figure 3은 제조된 항산화 렌즈 시료와 DPPH와의 반응에 따른 흡수 스펙트럼 변화를 나타낸 결과이다. 가장 소량의 도파민 그룹을 함유하는 렌즈 1의 경우, 반응이 30분간 경과함에 따라, 517 nm의 DPPH 라디칼 흡수가 감소하였지만, 여전히 피이크 형태가 남아있는 것을 알 수 있고, 좀 더 반응이 진행된 1시간 스펙트럼은 피이크 형태가 사라짐을 확인할 수 있다. 실제로 이러한 스펙트럼 결과는 DPPH 용액의 색변화(분홍색으로부터 노란색으로)를 통해 눈으로 확인 가능하였다. 한편, 보다 많은 도파민 그룹을 함유하는 렌즈 2와 3의 경우, 30분만에 DPPH 흡수 피이크가 사라지는 것을 알 수 있었고, 이와 같은 결과는 콘택트렌즈의 항산화 기능이 도입된 도파민 양에 비례하는 것으로 해석된다. Table 3은 스펙트럼의 결과를 토대로 시간에 따른 흡광도와 라디칼 소거율을 정리한 결과이다. 60분 결과의 경우, 스펙트럼 상에서 피이크 형태를 관찰할 수 없었지만, 517 nm의 흡광도의 절대값을 사용하여 라디칼 소거율을 계산하였다. 60분에서의 라디칼 소거율은 모든 렌즈에서 90%에 육박하는 거의 동일한 값을 갖는다는 것을 알 수 있다. 본 결과에서 언급할만한 점은, 본 연구에서 제조된 항산화 콘택트렌즈는 비록 매우 소량의 도파민 그룹을 사용했음에도 불구하고, 우수한 항산화 특성을 보인다는 것이다. 항산화 과정은 도파민으로부터 DPPH 라디칼로 전자가 이동하여, ortho-benzoquinone 형태로 전환되는 메커니즘을 갖는데, 본 과정이 매우 빠르게 진행되기 때문에, 그 결과 우수한 항산화 특성을 나타내게 되는 것이다.24 이와 더불어 공중합을 통해 도파민 그룹을 polyHEMA 내에 안정적으로 고정시킴으로써, 항산화 기능을 극대화하였기 때문으로 해석된다.
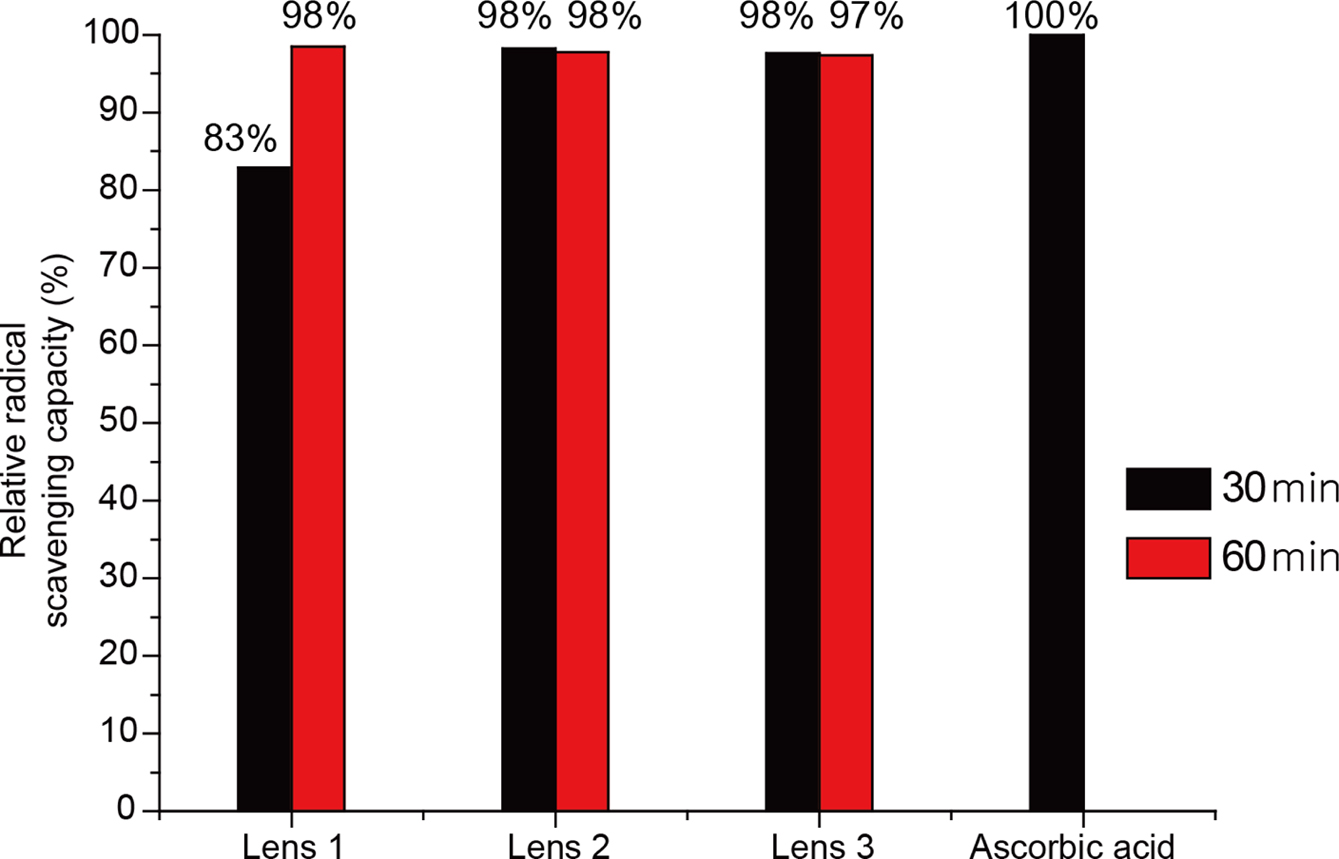
앞서 언급한 바와 같이, DPPH 용액 흡광법을 바탕으로 라디칼 소거율을 결정할 경우, 517 nm 위치에서 흡수 피이크 형태를 보이지 않음에도 불구하고, 330 nm에서 나타나는 흡수 피이크의 영향으로 517 nm에서의 흡광도는 0이 될 수 없다. 따라서 이미 알려진 항산화 물질의 소거율과의 비교는 본 연구에서 제조된 콘택트렌즈의 항산화 능력을 평가할 수 있는 공정한 지표로 이용될 수 있다. 본 연구에서는 항산화 물질로 가장 잘 알려진 아스코빅산을 선택하여, 라디칼 소거율을 측정하여 비교하였다. 동일한 조건의 DPPH 용액에서 라다칼 소거율을 측정한 결과, 아스코빅산의 경우, 91.1%의 라디칼 소거율을 나타내었다. Figure 4는 아스코빅산의 소거율을 100%로 가정한 상태에서, 상대적으로 계산된 렌즈들의 라디칼 소거율을 나타내고 있다. 본 연구에서 제조된 모든 렌즈들은 반응시간 1시간에서 계산된 상대 라디칼 소거율이 98%로, 아스코빅산과 거의 동일한 항산화능력을 보이는 것을 확인할 수 있다.
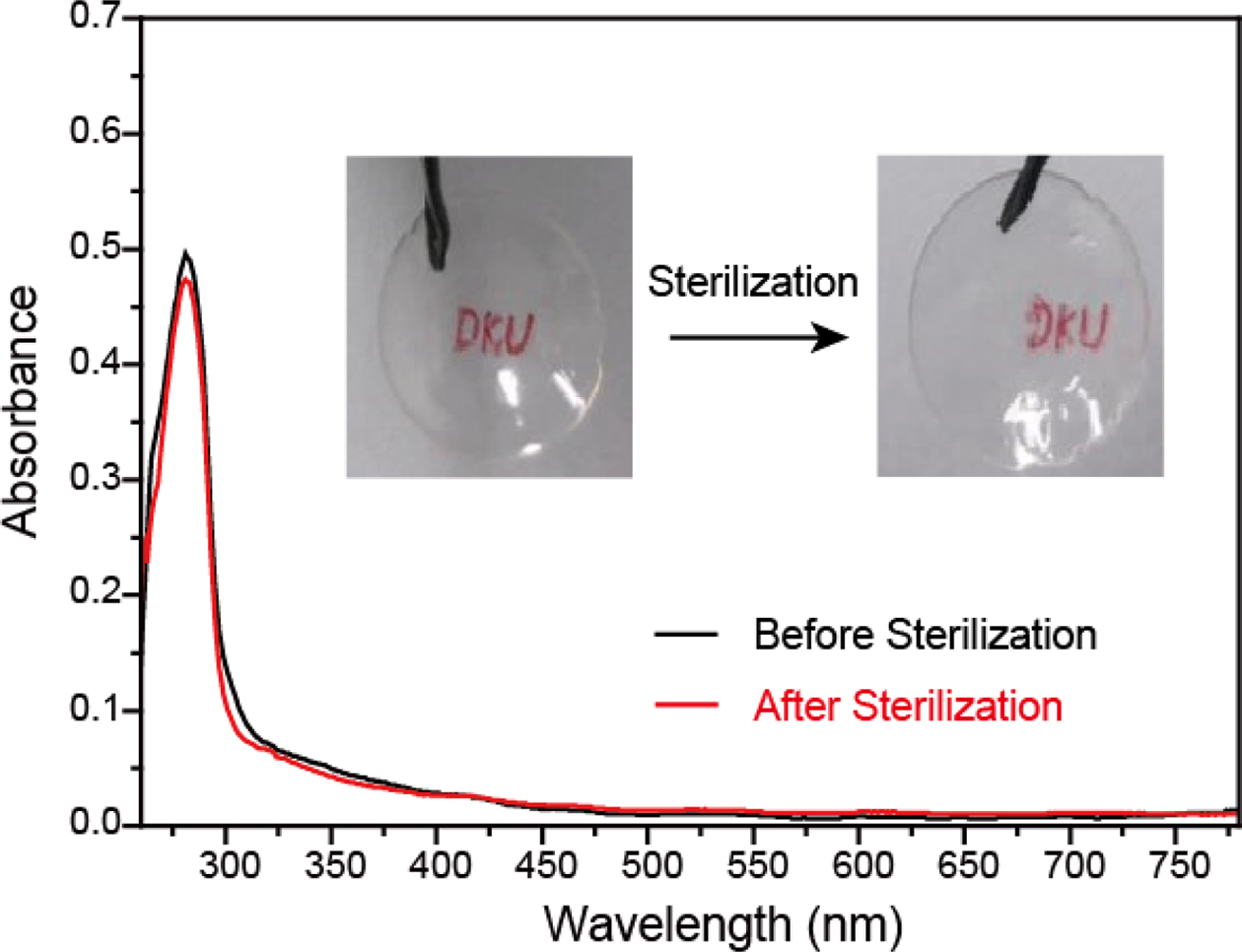
한편, 이 같은 우수한 항산화 능력으로 인하여, 콘택트렌즈 제조 시에, 빠른 산화에 의한 갈변 등의 부작용도 고려해 볼 문제다. 본 연구에서는 이를 확인하기 위해, 콘택트렌즈 멸균 조건과 유사한 열처리(탈염수, 100도에서 20분간 열처리)를 수행한 후에, 렌즈 변색 정도를 확인하였다. 그 결과, 육안으로 큰 색변화를 관찰할 수 없었을 뿐만 아니라, UV-vis 흡수 스펙트럼에서도 큰 변화를 관찰할 수 없었다(Figure 5). 이같은 보관상의 안정성은 공중합 제조 공정을 통해 도파민이 수화젤 네트워크 내부에 위치하여, 일반적인 보관 조건에서는 산화 반응이 잘 일어나지 않는 것으로 사료된다.
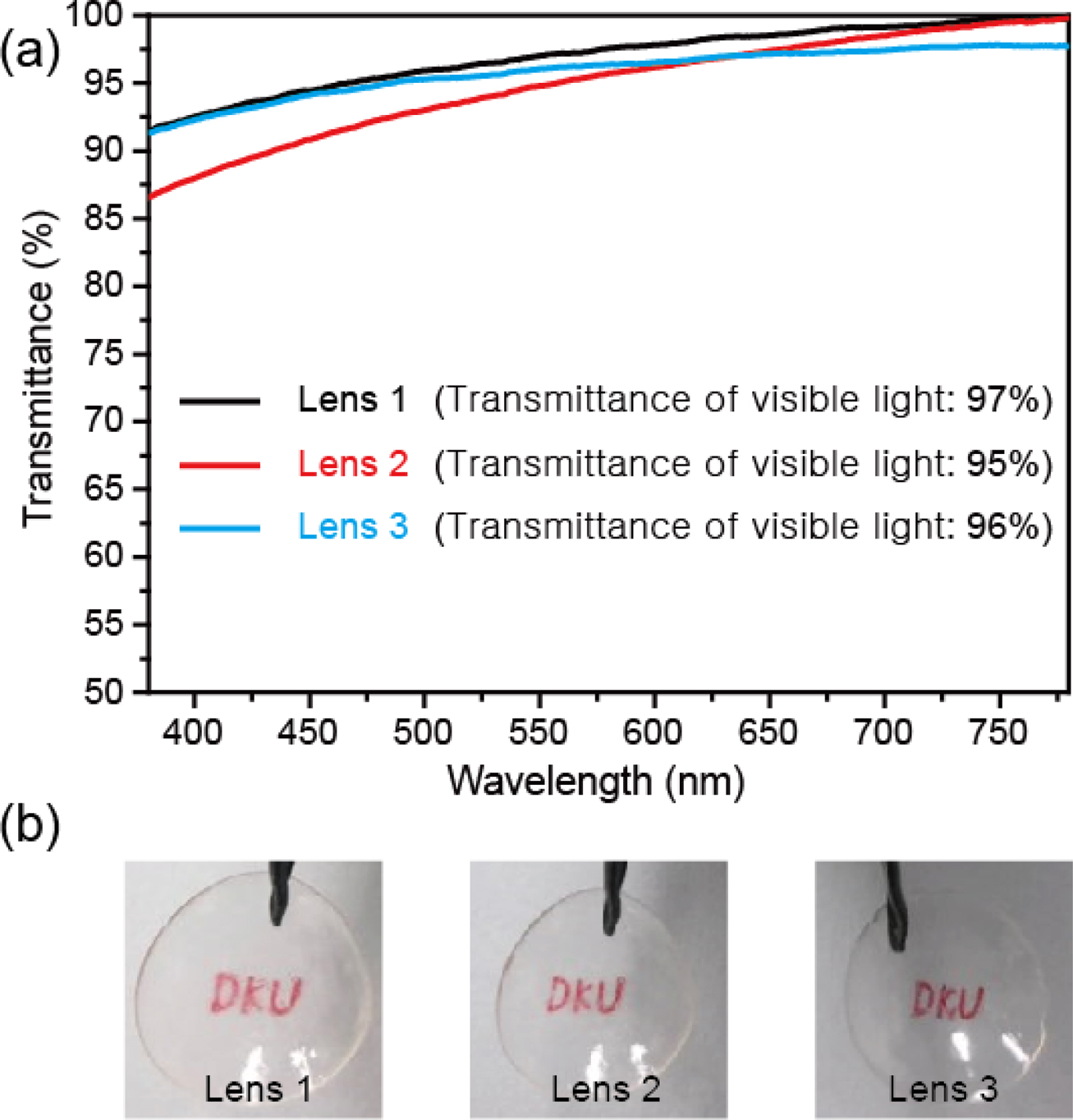
|
Figure 1 (a) Transmission spectra; (b) photos of antioxidant contact lenses. |

|
Figure 2 Contact angles of water droplets on antioxidant contact lenses. |
|
Figure 3 Absorption spectra of antioxidant contact lenses as a function of time. The photos indicate the color change of DPPH solution with time. |
|
Figure 4 Radical scavenging capacities of antioxidant contact lenses relative to ascorbic acid. |
|
Figure 5 Absorption spectra and photos of antioxidant contact lens(lens-3) before and after the thermal treatment at 100 oC for 20 min. |
|
Table 3 Absorbance (Radical Scavenging Efficiency) at 517 nm with Time in the Absorption Spectra of Lens Samples |
본 연구에서는 폴리페놀 계열인 도파민 단량체을 합성하여, HEMA, EGDMA, MPC와의 공중합을 통해 항산화 콘택트렌즈를 제조하였다. 공중합 시, MPC 중량%를 5%로 고정시키고, 도파민 단량체 중량%를 0.1, 0.3, 0.5%로 변화시켜, 3종의 항산화 콘택트렌즈를 제조하였다. 가시광선 투과율을 조사한 결과, 본 연구에서 제조된 렌즈 모두 평균 가시광선 투과율이 95% 이상을 나타내어, 우수한 광학 투명도를 나타내었다. 함수율 및 접촉각 측정을 통해 렌즈 친수성을 조사하였다. 모든 렌즈의 함수율은 50% 정도로, 기존에 알려진 수화젤 렌즈에 비해 10% 이상 향상된 값을 나타내었고, 일반적인 수화젤 렌즈의 접촉각(80o 정도)보다 상당히 낮은 56~63°의 접촉각을 나타내었기 때문에, 렌즈 표면이 높은 친수성을 유지하는 것을 알 수 있었다.
DPPH 용액의 라디칼 소거율을 흡수 분광법을 통해 렌즈들의 항산화 특성을 분석한 결과, 모든 항산화 렌즈는 1시간 이내에 90%에 육박하는 라디칼 소거율을 보였으며, 이 같은 수치는 아스코빅산의 항산화 기능 대비 98%를 해당하는 수치이다. 현재까지 폴리페놀 계열 단량체 물질을 이용한 항산화 콘택트렌즈는 보고된 바가 없다. 본 연구에서 사용한 도파민 단량체는 매우 적은 양으로 우수한 항산화 효과를 나타냈으며, 높은 렌즈 친수성으로 인하여 항산화 콘택트렌즈로의 상용화가 기대된다.
- 1. J. M. Seidel and S. M. Malmonge, Mater. Res., 3, 79 (2000).
-

- 2. B. Khodr and Z. Khalil, Free Radical Biol. Med., 30, 1 (2001).
-

- 3. G. M. Gordillo and C. K. Sen, Am. J. Surg., 186, 259, (2003).
-

- 4. K. Apel and H. Hirt, Annu. Rev. Plant Biol., 55, 373 (2004).
-

- 5. O. Senel, O. Cetinkale, G. Özbay, F. Ahçioglu, and R. Bulan, Ann. Plast. Surg., 35, 443 (1997).
- 6. E. Llorens, L. J. del Valle, and J. Puiggalí, Macromol. Res., 22, 388 (2014).
-

- 7. J. Kawabata, Y. Okamoto, A. Kodama, T. Makimoto, and T. Kasai, J. Agric. Food Chem., 50, 5468 (2002).
-

- 8. E. Giannakopoulos, K. C. Christoforidis, A. Tsipis, M. Jerzykiewicz, and Y. Deligiannakis, J. Phys. Chem. A, 109, 2223 (2005).
-

- 9. M. Scoponi, S. Cimmino, and M. Kaci, Polymer, 41, 7969 (2000).
-

- 10. M. Curcio, G. Cirillo, O. I. Parisi, F. Iemma, U. G. Spizzirri, I. Altimari, N. Picci, and F. Puoci, J. Funct. Biomater., 2, 1 (2011).
- 11. B. Kang, T. P. Vales, B.-K. Cho, J.-K. Kim, and H.-J. Kim, Molecules, 22, 1976 (2017).
-

- 12. N. Patil, C. Falentin-Daudré, C. Jérôme, and C. Detrembleur, Polym. Chem., 6, 2919 (2015).
-

- 13. H.-J. Kim, G.-C. Ryu, K.-S. Jeong, and J. Jun, Macromol. Res., 23, 74 (2015).
-

- 14. L. Poláková, V. Raus, L. Kostka, A. Braunová, J. Pilar, V. Lobaz, J. Pánek, and Z. Sedláková, Biomacromolecules, 16, 2726 (2015).
-

- 15. G. J. Papariello and M. A. M. Janish, Anal. Chem., 37, 899 (1965).
-

- 16. A. A. Soares, C. G. M. de Souza, F. M. Daniel, G. P. Ferrari, S. M. G. da Costa, and R. M. Peralta, Food Chem., 112, 775, (2009).
-

- 17. B. Kim, B. Kang, T. P. Vales, S. K. Yang, J. Lee, and H.-J. Kim, Macromol. Res., 26, 35 (2018).
-

- 18. Y. Hu, D. Wang, and G. Li, Anal. Methods, 7, 6103 (2015).
-

- 19. K.-S. Song, T.-H. Kim, and A.-Y. Sung, J. Korean Chem. Soc., 57, 300 (2013).
- 20. C.-H. Lin, H.-L. Cho, Y.-H. Yeh, and M.-C. Yang, Colloids Surf., B, 136, 735 (2015).
-

- 21. C. S. A. Musgrave and F. Fang, Materials, 12, 261 (2019).
-

- 22. M. B. Arnao, A. Cano, and M. Acosta, Food Chem., 73, 239 (2001).
-

- 23. S. C. T. Nicklisch and J. H. Waite, MethodsX, 1, 233 (2014).
-

- 24. C. Iuga, J. R. Alvarez-Idaboy, and A. Vivier-Bunge, J. Phys. Chem. B, 115, 12234 (2011).
-

- Polymer(Korea) 폴리머
- Frequency : Bimonthly(odd)
ISSN 0379-153X(Print)
ISSN 2234-8077(Online)
Abbr. Polym. Korea - 2023 Impact Factor : 0.4
- Indexed in SCIE
 This Article
This Article
-
2019; 43(5): 787-792
Published online Sep 25, 2019
- 10.7317/pk.2019.43.5.787
- Received on Jun 13, 2019
- Revised on Jul 15, 2019
- Accepted on Jul 16, 2019
 Services
Services
Shared
 Correspondence to
Correspondence to
- Byoung-Ki Cho
-
Department of Chemistry, Dankook University, Chungnam 31116, Korea
- E-mail: chobk@dankook.ac.kr
- ORCID:
0000-0002-2297-7707










 Copyright(c) The Polymer Society of Korea. All right reserved.
Copyright(c) The Polymer Society of Korea. All right reserved.