- Preparation of Antioxidant Hydrogel Contact Lenses Based on Hindered Amine Light Stabilizer
Department of Chemistry, Dankook University, Chungnam 31116, Korea
*Department of Chemistry, Chosun University, Gwangju 61452, Korea- 입체장애가 큰 아민 광 안정제를 기반으로 하는 항산화 기능성 수화젤 콘택트렌즈 제조
단국대학교 화학과, *조선대학교 화학과
In this work, we prepared antioxidant hydrogel contact lenses based on a hindered amine light stabilizer (HALS) which is 1,2,2,6,6-pentamethylpiperidin-4-yl methacrylate. The synthesis of the antioxidant hydrogel contact lenses was performed via the copolymerization of HALS monomer, 2-hydroxyethyl methacrylate and ethylene glycol dimethacrylate. Three contact lenses were prepared by varying the weight ratio (3, 5, 7%) of HALS monomer. Although the HALS group was incorporated in the hydrogel contact lenses, the prepared lenses exhibited visible light transmittance and water content similar to conventional hydrogel contact lenses without HALS group. The antioxidant activities of the HALS-based lenses were evaluated using 2,2-diphenyl-1-picrylhydrazyl radical scavenging assay. Consequently, the antioxidant lenses showed more than 25% higher radical scavenging activities than that (52.2%) of a control lens without HALS group. These values are more than 80% of the antioxidant activity of ascorbic acid, which is well-known as an antioxidant.
본 연구에서는 입체장애가 큰 아민 광 안정제(hindered amine light stabilizer, HALS)인 1,2,2,6,6-펜타메틸-4-피퍼리딜 메타크릴레이트 단량체를 이용하여 항산화 수화젤 콘택트렌즈를 제조하였다. 렌즈 합성은 2-하이드록시에틸 메타크릴레이트, 에틸렌 글리콜 디메타크릴레이트와의 공중합을 통해 이루어졌으며, HALS 단량체 무게 비율을 3, 5, 7%로 조절하여 3종의 렌즈들을 준비하였다. 제조된 렌즈는 HALS 그룹이 도입되었음에도 불구하고, 기존 수화젤 콘택트렌즈와 유사한 가시광선 투과율 및 함수율을 나타내었다. 2,2-다이페닐-1-피크릴하이드라질 라디칼 소거 분석법을 이용하여 항산화 기능성을 확인한 결과, HALS 그룹을 포함하지 않는 대조군 렌즈의 라디칼 소거율(52.2%)에 비해 항산화 렌즈 시료들은 25% 이상 높은 소거율을 보였다. 본 결과는 대표적 항산화 물질인 아스코빅산의 항산화 기능대비 80% 이상에 해당하는 수치이다.
The cationic surfactant treated GO and polystyrene (PS) nanocomposites were prepared. Nanocomposites with surfactant treated GO showed enhanced dispersion in PS and demonstrated improved barrier properties.
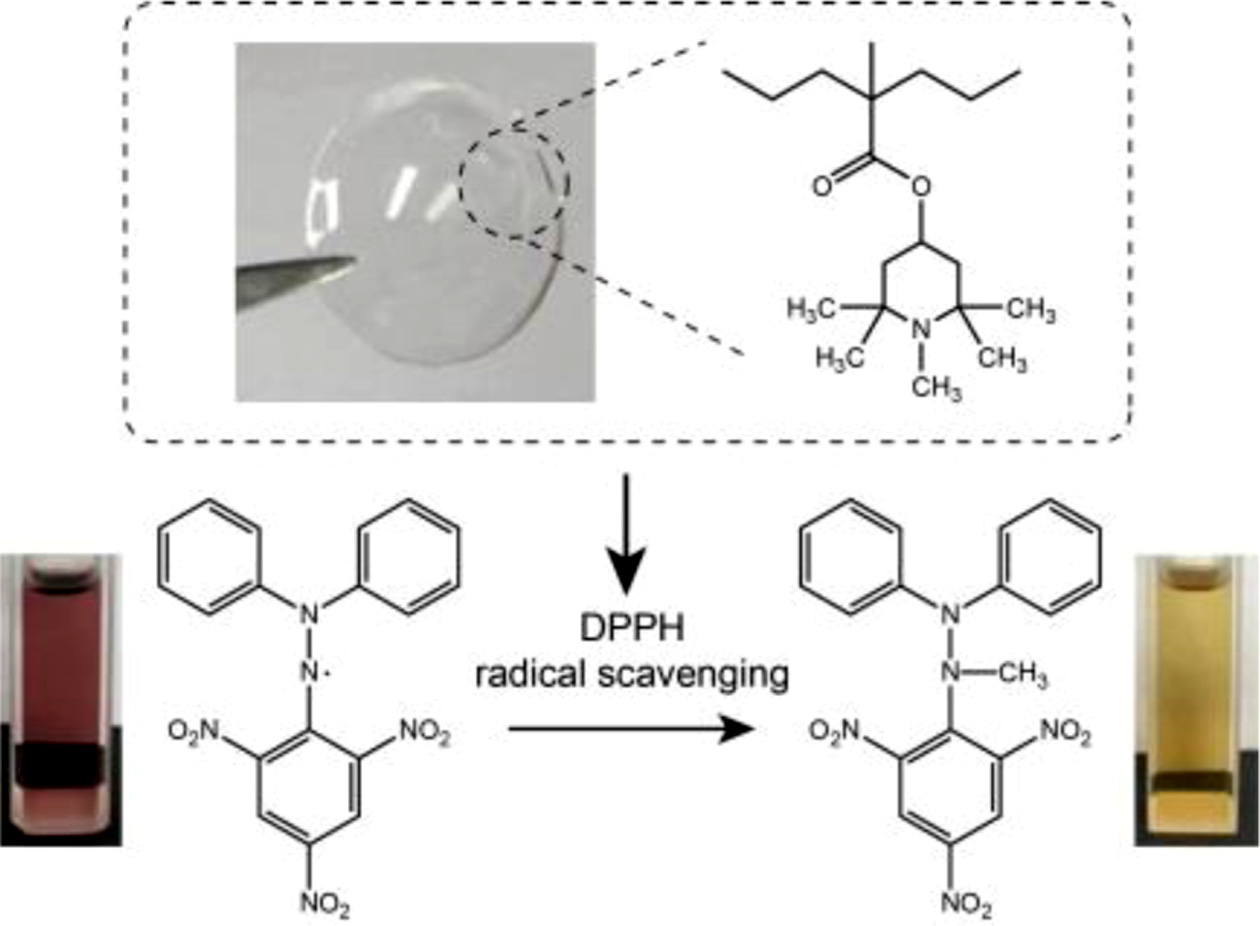
Keywords: hydrogel, contact lenses, antioxidant, hindered amine light stabilizer, radical scavenging assay
과산화 음이온 라디칼로 알려진 활성 산소종(reactive oxygen species, ROS)들은 상처 치유 과정에서 중요한 역할을 수행하는 것으로 알려져 있다.1-3 생체 내 조직이 손상될 경우, 활성 산소종 형태의 라디칼 형성에 관여하는 식세포에 존재하는 효소가 종종 활성화된다. 한편, 특정 조건하에서 이러한 라디칼 농도가 바람직하지 않은 방향으로 증가될 경우, 건강한 세포마저도 손상되어, 염증반응을 일으키는 문제를 야기시킨다.4
수화젤 콘택트렌즈(hydrogel contact lens)는 시야가 넓고 안경의 착용에서 오는 미용상의 단점을 피할 수 있는 장점이 있어 널리 사용되어 왔다. 현재는 시력교정, 치료용 이외에도 미용의 용도로 그 영역이 확대되면서 관련 시장이 지속적으로 성정하고 있는 추세이다. 한편, 콘택트렌즈의 장점에도 불구하고, 최근 전자 기기의 장시간 사용에 따른 안구 내 활성 산소의 생성, 축적이 야기되고, 이는 안구 질환의 원인이 될 수 있다. 즉, 렌즈를 장시간 착용하게 되면, 렌즈에서 발생되는 활성산소가 안구에 누적되고, 시력을 담당하는 중요부위인 황반 주변 세포가 파괴될 수 있다.
Poly(2-hydroxyethyl methacrylate) (pHEMA)로 구성된 가교고분자는 우수한 기계적 물성, 수용액 환경에서 이상적인 함수율, 높은 생체 적합성으로 대표적인 수화젤 콘택트렌즈 재료 물질로 사용된다.5 수화젤 콘택트렌즈 제조에 필요한 중합 조건이 단순히 벌크상에서 수행될 수 있기 때문에, 특정 기능성 구현이 가능한 물질을 중합과정에 도입할 경우, 다양한 기능성 수화젤 콘택트렌즈를 효과적으로 제조할 수 있다. 일례로, 항산화 기능을 갖는 천연물인 케프세틴 등을 pHEMA와 혼합시켜, 항산화 특성이 향상된 수화젤을 제조한 연구결과가 보고된 바 있다.6 그러나 이 경우는, 수화젤과 항산화 물질이 화학적 결합이 아닌 단순히 물리적 혼합을 통해 제조되었기 때문에, 사용 시간이 경과함에 따라 항산화 물질의 방출로 인한 기능 저하를 피할 수 없다. 따라서 수화젤 콘택트렌즈의 항산화 기능을 지속적으로 구현하기 위해서는 항산화 물질을 수화젤 구조에 화학적으로 고정시킬 필요가 있다.
한편, 입체장애가 큰 아민을 함유하는 광 안정제(hindered amine light stabilizer, HALS)는 활성 산소종들과 반응할 수 있는 항산화 물질로 분류할 수 있다. 활성 산소와의 반응을 통해, HALS 화합물들은 안정하고 비독성의 나이트록사이드(nitroxides) 및 하이드록실아민(hydroxylamines)들로 전환이 가능하다.7 이러한 항산화 특성을 나타내는 HALS 화합물을 중합 가능한 단량체로 변환 후,8 HEMA와의 공중합을 통해 콘택트렌즈를 제조할 경우, HALS가 pHEMA에 공유결합으로 연결되기 때문에, 기존에 보고된 항산화 물질 유출 등의 문제점을 해결할 수 있다. 결과적으로, 수화젤 콘택트렌즈에 지속적인 항산화 기능을 부여할 수 있을 것이다. 그러나 이런 장점에도 불구하고, 현재까지 HALS와 HEMA와의 공중합을 통한 항산화 기능성 콘택트렌즈 제조에 대한 연구는 전무한 실정이다. 이러한 연구 배경을 토대로, 본 논문에서는 중합 가능한 HALS 단량체를 수화젤 콘택트렌즈 중합 단계에 도입하여, HALS 그룹이 화학적으로 결합된 항산화 기능을 갖는 수화젤 콘택트렌즈 제조에 관한 내용을 세계 최초로 보고하고자 한다. 본 연구에서는 1,2,2,6,6-펜타메틸-4-피퍼리딜 메타크릴레이트(1,2,2,6,6-pentamethylpiperidin-4-yl methacrylate)를 HALS 단량체로 사용하였다. 공중합 시에 HALS 단량체의 중량%를 3%(렌즈샘플 1), 5%(렌즈샘플 2), 7%(렌즈샘플 3)로 변화시켜 가며 수화젤 콘택트렌즈를 제조하였고, 이에 따른 항산화 능력을 비교 분석하였다.
재료. 본 연구에 사용된 시약들인 하이드록시에틸 메타크릴레이트(2-hydroxyethyl methacrylate, HEMA), 1,2,2,6,6-펜타메틸-4-피퍼리딜 메타크릴레이트(1,2,2,6,6-pentamethyl-piperidin-4-yl methacrylate), 에틸렌 글리콜 디메타크릴레이트(ethylene glycol dimethacrylate, EGDMA), 2,2-아조디이소부틸로나이트릴(2,2-azobis(2-methylpropionitrile), AIBN), 2,2-다이페닐-1-피크릴하이드라질(2,2-diphenyl-1-picrylhydrazyl, DPPH)를 Sigma-Aldrich사로부터 구입하여 정제 없이 사용하였다.
공중합을 통한 항산화 렌즈 샘플 제조. 우선 중합에 사용할 혼합시료를 다음과 같이 제조하였다. 개시제인 AIBN 0.02 g과 가교제인 EGDMA 0.02 g으로 고정시킨 후, HEMA와 HALS 단량체의 양을 각각 4.81~4.61 g, 0.15~0.35 g으로 변화시켜가며 바이알에 정량한 후, 30분 동안 초음파 처리를 수행하였다. 준비된 혼합시료를 암형인 폴리프로필렌(polypropylene, PP) 몰드에 주입한 후, 수형인 폴리부틸렌 테레프탈레이트(polybutylene terephthalate, PBT) 몰드로 덮는다. 이후, 온도를 90 ℃로 유지한 오븐에 4시간 동안 넣고 열중합을 수행하였다. 동일한 방법을 통해 HALS 단량체가 포함되지 않은 대조군 렌즈도 함께 제조하였다. 제조된 렌즈들은 동일한 두께(0.23 mm)를 나타내었다.
가시광선 투과율 측정. UV-vis spectrophotometer (SHIMADZU UV-2600)를 이용하여 제조된 수화젤 콘택트렌즈들의 가시광선 투과율을 측정하였다. 시편은 수화된 렌즈를 부분 절단하여 렌즈의 굴곡을 없앤 후, 2개의 유리 슬라이드 사이에 넣는다. 제작된 시편을 폴리이미드(polyimide) 필름을 사용하여 분광기 내에 고정시킨 후, 투과율을 측정한다.
함수율 측정. 제조된 수화젤 콘택트렌즈를 48시간 동안 과량의 물에 담근 후, 표면 수분 제거 후, 수화된 렌즈의 질량을 측정하여, 식 (1)을 통해 함수율(percentage of water content, PWC)을 계산하였다. 각 시료 별로 5차례 실험을 하여, 평균값을 표시하였다.

항산화 기능 측정. 시간에 따른 DPPH 용액(0.2 mM)의 라디칼 소거 정도를 UV-vis spectrophotometer(SHIMADZU UV-2600)를 통해 측정하여, 렌즈들의 항산화 기능성을 결정하였다.9-11 DPPH 용액은 DPPH 0.079 g을 100 mL의 에탄올에 넣어 제조한 후, 10배 희석하여 사용했다. 렌즈 샘플(각 샘플당 4개의 렌즈)들을 20 mL 갈색 바이알에 각각 넣은 뒤, 0.2 mM DPPH를 각 바이알에 2.7 mL 첨가했다. 37 ℃에서 상기 바이알들을 초음파(sonication)처리를 하면서 517 nm에서의 용액 흡광도를 측정했다. 30분, 2, 4, 6, 9, 15시간마다 측정값을 기록하였다. 아스코빅산의 경우, 0.04 M 농도의 수용액을 제조하여, 0.3 mL를 2.7 Ml의 DPPH 용액(0.2 mM)에 첨가하여, 항산화 기능을 측정하였다.12

항산화 수화젤 콘택트렌즈 분자 구조는 Scheme 1에 나타내었다. 렌즈 제조에 필요한 혼합시료는 Table 1에 나타낸 렌즈 샘플 1-3에 해당하는 중량비에 따라, 개시제(AIBN), 가교제(EGDMA), HEMA 단량체, HALS 단량체를 혼합하여 제조한 후, 공중합 과정을 통해 렌즈들을 제조하였다(Scheme 1). 중합된 렌즈를 몰드로부터 탈착한 후, 6시간 동안 탈염수 수용액에 보관하여, 수화젤 콘택트렌즈를 제조하였다.
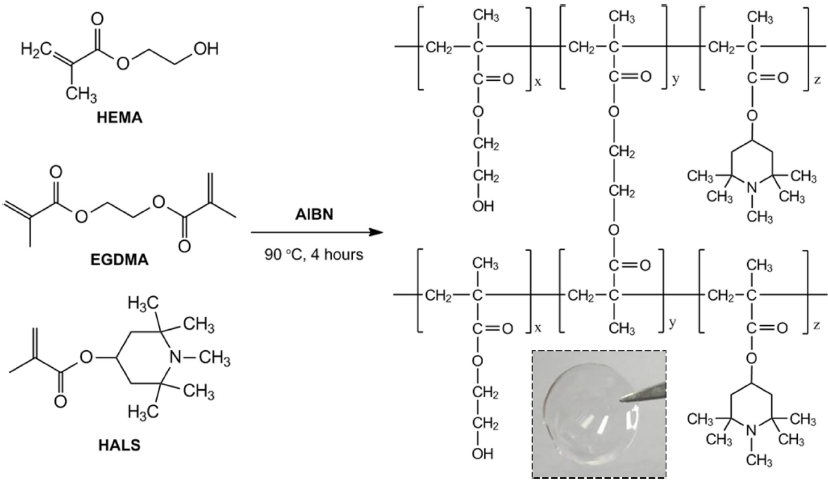
Scheme 1. Synthesis of antioxidant contact lenses via copolymerization of HEMA, EGDMA, and HALS. The photo is the lens after copolymerization.
수화젤 콘택트렌즈에 있어서 중요한 물리적 특성으로 광학 투명도가 요구된다. 따라서 제조된 항산화 수화젤 렌즈 샘플들의 가시광선(380~780 nm 파장 영역) %투과율을 자외선-가시광선 흡수 분광법을 통해 조사하였다.13 항산화 렌즈 샘플과 더불어, HALS 그룹을 포함하지 않은 대조군 렌즈의 %투과율도 측정하여, 비교 분석하였다. Figure 1에서 볼 수 있듯이, 가시광선 전 파장 영역에서 대조군 렌즈와 항산화 렌즈 샘플(1-3)들이 90% 이상의 높은 투과율을 나타내는 것을 알 수 있다. 얻어진 흡수 스펙트럼을 토대로 계산한 결과, 대조군 및 항산화 렌즈 샘플 1-3에 대한 가시광선 범위 평균 투과율은 97.4, 97.9, 97.8, 97.6%로 계산되었다. 분광 분석 결과와 동일하게, 실제 육안으로 확인한 경우에도, 수화젤 렌즈 표면에 불투명한 부분을 관찰할 수 없었다. 이를 통해 중합 시에, 첨가된 HALS 단량체들이 pHEMA 네트워크 사슬 구조 내에 균일하게 분포되어, 가시 광선 산란을 초래하지 않음을 알 수 있다.
다음으로 수화젤 콘택트렌즈의 함수율을 측정하였다. 함수율 측정은 각 항산화 렌즈 시료당 5번의 측정한 값을 평균하여 Table 2에 나타내었다. 렌즈 시료의 함수율 측정 전에, 함수율 비교를 위해 HALS 그룹을 포함하지 않은 대조군 렌즈의 함수율을 측정하였다. 측정 결과 40%의 함수율을 보였는데, 이는 통상적으로 보고된 pHEMA 수화젤에서 나타내는 함수율(38%) 값과 유사한 것을 알 수 있다.14 이와 유사하게, HALS 그룹을 포함하는 항산화 렌즈 시료들도 40-41%의 함수율을 유지하는 것을 확인하였다. 결과적으로, 항산화 특성을 위해 첨가한 HALS 그룹이 본 실험에서 첨가량 영역에서 수화젤 콘택트렌즈의 함수율에 크게 영향을 주지 않음을 알 수 있다.
제조된 항산화 렌즈 시료의 항산화 기능은 DPPH 용액 하에서, DPPH 라디칼 소거에 따른 517 nm 파장 변화 측정을 통해 확인하였다(Figure 2).15 DPPH 분석의 경우, Figure 2(c)에서 볼 수 있듯이, HALS 그룹에서 질소원자에 연결된 메틸 그룹 라디칼 전달 반응에 기인한 것으로 해석할 수 있다. 이 경우, 517 nm에서 최대 파장을 흡수 피이크가 감소하는 현상은 HALS 그룹의 항산화 작용으로 인하여 DPPH 라디칼이 DPPH-CH3로 변화되는 것을 의미한다.16 항산화 렌즈 시료의 측정 전에, 대조군 렌즈를 준비하여 DPPH 라디칼 소거율을 측정하였다. Figure 2(a)와 2(b)는 각각 대조군 렌즈와 렌즈 샘플 3의 시간경과에 따른 흡광 스펙트럼의 변화를 나타내고 있다. 시간이 지남에 따라서, 대조군 렌즈와 렌즈 샘플 모두 517 nm에서 나타나는 흡수 피이크의 세기가 감소함을 알 수 있다. 대조군 렌즈의 경우, 초기에 감소에 비해 2시간 이후, 감소 정도가 크지 않음을 알 수 있다. 반면, 렌즈 샘플 3의 경우, 지속적으로 감소하여 15시간 후에는 피이크 형태를 구분할 수 없을 정도로 흡광 신호가 줄어듦을 확인하였다. 이러한 흡광 스펙트럼의 변화는 육안으로도 확인할 수 있다. Figure 2(c)에서 볼 수 있듯이, DPPH 용액은 라디칼 형태로 존재 시 자주색을 띠는 반면, HALS 그룹에 의해 라디칼 소거 시, 노란색의 용액으로 변화되는 것을 관찰할 수 있다. 실제로, HALS 그룹을 포함하지 않는 대조군 렌즈로 처리한 DPPH 용액은 여전히 자주색을 유지하였지만, HALS를 포함하는 렌즈 시료 모두는 노란색으로 변화됨을 확인할 수 있었다.17
Table 3은 각 렌즈 샘플에 대해 시간에 따라 517 nm 최대 흡수 파장에서 측정한 흡광도를 정리한 것이다. DPPH assay 실험은 동일 조건에서 시료당 3번씩 진행하였고, Table 3에 제시한 값은 평균값을 나타낸 것이다. 렌즈 샘플 1과 2도 렌즈 샘플 3과 유사한 흡광 스펙트럼 및 DPPH 용액의 변색 결과를 나타내었다. HALS 첨가량에 따른 DPPH 소거율을 보면, 상대적으로 HALS 첨가량이 적은 렌즈 샘플 1이 15시간에서 77.5%의 소거율을 나타내었으며, HALS 첨가량이 5%이상의 렌즈 샘플 2와 3은 85% 이상의 소거율을 나타내었다. Table 3의 소거율 자료를 토대로 시간에 따른 소거율 변화를 Figure 3에 그래프로 표시하였다. HALS을 포함하는 항산화 렌즈들이 대조군 렌즈에 비해 효과적으로 라디칼을 제거함을 알 수 있고, HALS 첨가량 증가에 따라 소거율이 다소 증가하는 것을 알 수 있다.
위의 DPPH 용액의 흡광법을 이용하여 라디칼 소거율을 결정할 경우, 517 nm 위치에서 흡수 피이크 형태를 보이지 않음에도 불구하고, 330 nm 근처에서 흡수하는 피이크의 영향으로 0의 흡수 세기를 갖을 수 없다. 따라서, 이미 잘 알려진 항산화 물질의 소거율과의 비교는 HALS를 기반으로 하는 렌즈의 항산화 능력을 평가하는데 유용한 지표로 사용될 수 있다. 본 연구에서는 대표적 항산화 물질로 알려진 아스코빅산의 라디칼 소거율을 측정하여 비교하였다. 동일한 DPPH 용액 조건하에서 아스코빅산의 경우, 95.2%의 라디칼 소거율을 나타내었다. Figure 4는 아스코빅산의 소거율을 100%라 가정하여, 계산된 상대 소거율을 나타내고 있다. 대조군 렌즈의 경우, 아스코빅산 대비 54.8%의 항산화 특성을 보이는 반면, 항산화 렌즈 시료 1-3들은 81.4%, 92.8%, 90.3%의 항산화 능력을 나타내었다.

|
Figure 1 Transmission spectra of control lens and antioxidant lenses. |

|
Figure 2 Absorption spectra of (a) control lens; (b) lens sample 3 as a function of time; (c) radical scavenging reaction of DPPH solution. |

|
Figure 3 Radical scavenging capacities of lens samples as a function of time. The error bars indicate the maxima and minima obtained from DPPH assay experiments. |

|
Figure 4 Relative radical scavenging capacities of lens samples in comparison to ascorbic acid. |
|
Table 3 Absorbance (Radical Scavenging Efficiency) at 517 nm with Time in the Absorption Spectra of Lens Samples |

본 연구에서는 HALS 물질로 알려진 1,2,2,6,6-펜타메틸-4-피퍼리딜 메타크릴레이트 단량체와 2-하이드록시에틸 메타크릴레이트, 에틸렌 글리콜 디메타크릴레이트와의 벌크상 공중합을 통해 항산화 콘택트렌즈를 제조하였다. 공중합 시, HALS 단량체 무게 비율을 3, 5, 7%로 조절하여 3종의 수화젤 콘택트렌즈들을 합성하고, 합성된 렌즈 시료들의 항산화 특성을 HALS를 포함하지 않은 대조군 렌즈 및 대표적 항산화 물질인 아스코빅산과의 비교를 통해 결정하였다. 제조된 항산화 렌즈들은 HALS 그룹이 도입되었음에도 불구하고, 대조군 렌즈와 유사한 가시광선 투과율과 함수율을 나타내고 있음을 알 수 있었다. DPPH 용액의 라디칼 소거율을 통해 항산화 특성을 분석한 결과, 대조군 렌즈에 비해 25% 이상의 특성 향상이 있음을 확인할 수 있었고, 이 같은 수치는 아스코빅산의 항산화 기능 대비 80%를 초과하는 것으로, 우수한 항산화 능력을 나타냄을 알 수 있었다. 현재까지 HALS 물질을 이용한 항산화 수화젤 콘택트렌즈는 보고된 바가 없기 때문에, 본 논문 내용은 HALS를 이용한 수화젤 콘택트렌즈 제조에 있어서 세계 최초의 결과이며, 또한 HALS의 산화된 형태를 함유하는 pHEMA 수화젤이 독성이 없다는 보고된 사실로부터, HALS를 이용하여 항산화 기능이 부여된 콘택트렌즈의 상용화가 기대된다.
- 1. B. Khodr and Z. Khalil, Free Radical Biol. Med., 30, 1 (2001).
-

- 2. G. M. Gordillo and C. K. Sen, Am. J. Surg., 186, 259, (2003).
-

- 3. K. Apel and H. Hirt, Annu. Rev. Plant Biol., 55, 373 (2004).
-

- 4. O. Senel, O. Cetinkale, G. Özbay, F. Ahçioglu, and R. Bulan, Ann. Plast. Surg., 35, 443 (1997).
- 5. J. M. Seidel and S. M. Malmonge, Mater. Res., 3, 79 (2000).
-

- 6. M. Curcio, G. Cirillo, O. I. Parisi, F. Iemma, U. G. Spizzirri, I. Altimari, N. Picci, and F. Puoci, J. Funct. Biomater., 2, 1 (2011).
- 7. M. C. Krishna, W. DeGraff, O. H. Hankovszky, C. P. Sár, T. Kálai, J. Jekö, A. Russo, J. B. Mitchell, and K. Hideg, J. Med. Chem., 41, 3477 (1998).
-

- 8. K. Kejlová, J. Labský, D. Jírová, and H. Bendová, Toxicol. In Vitro, 19, 957 (2005).
-

- 9. L. Poláková, V. Raus, L. Kostka, A. Braunová, J. Pilar, V. Lobaz, J. Pánek, and Z. Sedláková, Biomacromolecules, 16, 2726 (2015).
-

- 10. G. J. Papariello and M. A. M. Janish, Anal. Chem., 37, 899 (1965).
-

- 11. A. A. Soares, C. G. M. de Souza, F. M. Daniel, G. P. Ferrari, S. M. G. da Costa, and R. M. Peralta, Food Chem., 112, 775 (2009).
-

- 12. B. Kim, B. Kang, T. P. Vales, S. K. Yang, J. Lee, and H.-J. Kim, Macromol. Res., 26, 35 (2018).
-

- 13. H.-J. Kim, G.-C. Ryu, K.-S. Jeong, and J. Jun, Macromol. Res., 23, 74 (2015).
-

- 14. K.-S. Song, T.-H. Kim, and A.-Y. Sung, J. Korean Chem. Soc., 57, 300 (2013).
-

- 15. B. Kang, T. P. Vales, B.-K. Cho, J.-K. Kim, and H.-J. Kim, Molecules, 22, 1976 (2017).
-

- 16. P. Gijsman, Polym. Degrad. Stabil., 145, 2 (2017).
-

- 17. S. C. T. Nicklisch and J. H. Waite, MethodsX, 1, 233 (2014).
-

- Polymer(Korea) 폴리머
- Frequency : Bimonthly(odd)
ISSN 0379-153X(Print)
ISSN 2234-8077(Online)
Abbr. Polym. Korea - 2023 Impact Factor : 0.4
- Indexed in SCIE
 This Article
This Article
-
2019; 43(5): 694-699
Published online Sep 25, 2019
- 10.7317/pk.2019.43.5.694
- Received on Apr 13, 2019
- Revised on May 14, 2019
- Accepted on May 26, 2019
 Services
Services
Shared
 Correspondence to
Correspondence to
- Byoung-Ki Cho
-
Department of Chemistry, Dankook University, Chungnam 31116, Korea
- E-mail: chobk@dankook.ac.kr
- ORCID:
0000-0002-2297-7707












 Copyright(c) The Polymer Society of Korea. All right reserved.
Copyright(c) The Polymer Society of Korea. All right reserved.