- Turn-On Detection of Cs Ions Based on Conjugated Polymer-Graphene Oxide Composite
Geunseok Jang, Eunbee Cho, Laurence M. Harwood*, and Taek Seung Lee†

Organic and Optoelectronic Materials Laboratory, Department of Advanced Organic Materials and Textile System Engineering, Chungnam National University, Daejeon 34134, Korea
*Department of Chemistry, University of Reading, Reading RG6 6AH, United Kingdom- 공액화 고분자-그래핀 옥사이드 복합체의 턴-온 형광 변화를 이용한 세슘 이온 감지
충남대학교 유기소재·섬유시스템공학과, *Department of Chemistry, University of Reading
New type of “turn-on” fluorescent sensor for Cs ion was developed using a composite of blue-emissive conjugated polymer (CP) and graphene oxide (GO). Ethylene glycol units were introduced to the side chain of CP, which could interact with Cs ions. The CP and GO formed a stable, nonfluorescent composite, because of hydrophobic and π-π interactions between them. In the presence of Cs ions, the CP was released from the CP-GO composite because of higher affinity of Cs ions with ethylene glycol units in the CP. Such a weaker interaction between CP and GO led to the recovery of initial blue fluorescence of the CP. The degree of fluorescence restoration would be a measure of the concentration of Cs ions. Thus, fluorescence “turn-on” from CP-GO was attributed to the presence of Cs ions.
세슘 이온의 검출과 함께 형광이 증가하는 턴-온 형광센서를 공액화 고분자(CP)와 그래핀 옥사이드(GO)로 구성된 복합체로 제조하였다. 세슘 이온과 상호작용을 위해 CP의 곁사슬에 테트라에틸렌 글라이콜(TEG)기를 도입하였다. GO는 유기분자와 소수성 상호작용하여 소수성인 CP와 쉽게 복합체를 형성하는 특성을 가지며, 복합체를 형성하면 CP에서 GO로 에너지 전달이 일어나 CP의 형광이 사라지게 된다. CP-GO 복합체가 세슘 이온에 노출되면 CP의 곁사슬인 테트라에틸렌 글라이콜과 세슘 이온이 결합하고, 이로 인해 CP와 GO의 상호작용이 약회되어 CP가 GO로부터 유리되며, 이탈된 CP는 원래의 형광을 회복하게 된다. 이는 세슘 이온을 선택적으로 감지하는 형광 턴-온 센서로 사용가능하게 된다.
Keywords: conjugated polymers, graphene oxide, Cs ion detection, fluorescence, sensors
이 연구는 충남대학교 학술연구비에 의해 지원되었으며, 이에 감사드립니다.
방사성 동위원소는 원자력 발전소, 의료 폐기물 등에서 발견되며 인체에 노출될 수 있는 위험을 가지고 있다. 특히, 후쿠시마 핵연료 발전소의 사고는 다량의 방사성 동위원소의 유출로 인해 세슘 이온과 같은 위험 원소들의 생체 노출에 대한 위험 및 경각심에 대해 많은 관심을 받게 되었다.1,2 세슘 이온과 같은 방사성 동위원소들은 생체에 노출이 되면 건강에 치명적인 부작용을 야기시키는 문제점을 가지고 있는데, 악성 종양이나, 장기에 치명적인 암을 유발시키는 것으로 알려져 있다.3 일반적으로 이러한 원소들은 원자 흡수 분광법(atomic absorption spectroscopy, AAS),4 이온 선택 전극(ion-selective electrode),5 유도결합플라즈마 질량분석기(inductively coupled plasma mass spectroscopy, ICP-MS)같은6 장비로 정밀한 분석이 가능하지만, 분석료가 비싸고 분석시료를 파괴하는 단점을 가지고 있어, 보다 저렴하고 쉽게 분석하기 위한 연구들이 많이 진행되고 있다.7,8
활발히 진행되는 연구 중에서 에틸렌 글라이콜 유도체(ethylene glycol derivative)나 크라운 에테르(crown ether)같은 유기물을 이용하여 세슘 이온과 같은 방사성 동위원소를 검출하는 연구가 많이 진행되었다.9,10 에틸렌 글라이콜이나 크라운 에테르와 같은 유기물은 구조 내에 존재하는 산소원자가 방사성 동위원소와 결합하는 특성이 있기 때문에 보다 쉽게 검출이 가능하다는 장점을 갖고 있다. 또한 위에서 언급한 물질들은 분자의 사슬 길이 조절이 가능하여 사슬 길이에 따라 다양한 방사성 동위원소들을 선택적으로 검출하는 연구도 보고되었다.11 에틸렌 글라이콜의 반복 단위가 6-9개일 경우에 세슘 이온에 선택적으로 결합하는 것으로 알려져 있으며, 대표적으로 24-crown-8이 있다.12
유기물을 이용한 세슘 이온 감지를 위해 유기물의 광학 특성 중 하나인 형광 변화를 이용하여 세슘 이온을 감지하는 형광 센서가 연구되고 있다.13,14 유기재료 중, 공액화 고분자 (conjugated polymer, CP)의 연구는 다양한 분야에서 이루어지고 있으며,15-17 CP의 경우, 저분자 형광 센서와18-20 비교하여 감지 물질에 대한 민감도가 우수한 것으로 알려져 있어 다양한 물질들을 검출하는데 매우 효과적이다.21-25 또한 다른 분석법과는 다르게 형광 변화를 이용하여 감지 물질과 접촉 후 쉽게 결과를 확인할 수 있다는 장점이 있어서 형광 센서 분야에서 큰 각광을 받고 있다. 가장 흔하게 사용되는 방식은 검출 시 형광이 사라지는 턴-오프(turn-off) 시스템이며, 금속 이온 검출에 매우 효과적인 특징이 있다.26-29 형광 변화를 이용한 감지 방법 중 검출과 함께 형광이 증가하는 턴-온(turn-on) 센서는 형광이 증가하므로 턴-오프 센서보다 판별이 더 쉬운 장점이 있다.30-33
또한 이러한 턴-온 방식의 센서를 제조하기 위해 그래핀 옥사이드(graphene oxide, GO)가 형광 센서 분야에 자주 사용되었다.34 GO는 그래핀이 산화되어 판상으로 존재하는 물질이며, 기계적 물성과 광학적 물성이 특이하여 다양한 연구분야에서 활용되고 있는데, 센서분야에서는 가시광영역의 빛을 흡수하는 특성을 이용한 연구가 많이 진행되었다.35 GO는 유기물과의 소수성 결합(hydrophobic interaction)을 쉽게 할 수 있고, 특히 GO 주변에 형광 물질이 존재할 경우, 형광물질이 방출하는 빛을 흡수하는 특성때문에 “quencher”역할을 하며, 이러한 특성을 이용해 형광 변화를 유도하여 턴-온 형광 센서의 기질로도 많이 이용되었다.36
본 연구에서는, 세슘 이온을 감지하기 위한 형광 턴-온 센서를 제조하기 위해 CP-GO 복합체를 사용하였다. 사용된 CP는 세슘 이온과 선택적으로 결합하기 위해서 CP 곁사슬에 세슘 이온을 결합할 수 있는 테트라에틸렌 글라이콜(tetraethylene glycol, TEG)기를 도입하였다. 제조된 CP-GO는 GO의 형광 소광 특성으로 인해 CP의 형광이 소광된 상태로 존재한다. 이러한 미형광 CP-GO가 검출 대상물인 세슘 이온에 노출되면 CP의 곁사슬인 TEG에 세슘 이온이 우선적으로 결합되는 과정에서 GO와 CP간 결합이 약해지며 CP가 GO의 표면에서 박리되게 된다. 이에 따라 GO에 의해 소광되었던 CP의 원래 형광이 다시 증가하는 턴-온 센서 시스템을 이용하여 세슘 이온을 감지하였다.
기기. 1H과 13C NMR 스펙트럼은 Bruker DRX-300 분광기를 사용하여 얻었으며(한국기초과학지원연구원), UV/vis 스펙트럼은 Perkin Elmer Lambda 365 분광기를 사용하여 측정하였다. 형광 스펙트럼은 제논 램프를 광원으로 장착한 Varian Cary Eclipse 분광기를 사용하여 얻었으며 FTIR은 Bruker Tensor 27 분광기를 사용하였다. 원소분석(EA)은 Thermo Scientific의 FLASH 2000을 이용하여 분석하였으며, GPC를 이용한 CP의 분자량 측정은 영린기기의 YL9100를 사용했다.
재료 및 시약. GO와37 단량체(M1-M3)는38,39 이전 연구의 합성법을 참고하여 합성하였다. Tetraethylene glycol monomethyl ether, diethylene glycol monomethyl ether, tetrakis(triphenylphosphine)palladium(0)은 Sigma-Aldrich에서 구입하여 사용하였다. Bromine은 Junsei에서 구입하였으며, hydroquinone은 Samchun Pure Chemical Co. Ltd에서 구입하여 정제없이 사용하였다.
TCP(Tetraethylene Glycol-Conjugated Polymer)의 중합. 100 mL 3구 플라스크에 M1(0.504 g, 0.90 mmol)과 1,4-benzenediboronic acid bis(pinacol)ester(0.330 g, 1.0 mmol)를 THF와 톨루엔 혼합 용매(10 mL)에 녹인 후, 2 M K2CO3 수용액(5 mL)과 aliquot 336을 첨가하여 아르곤 가스 하에서 이 혼합물을 70 ℃에서 40 시간 동안 교반시켜 반응하였다. 반응이 종결 후, 실온으로 냉각시킨 이 반응혼합물을 메탄올에 부어 침전을 얻었다. 이 생성물은 여과하여 얻은 후 증류수와 메탄올로 세척하였고 감압 하에 실온에서 건조시켰다(0.32 g, 75%). 1H NMR: 7.71 (s, 4H), 7.12 (s, 2H), 4.17 (m, 4H), 3.82-3.49 (m, 36H), 3.35 (s, 6H) 13C NMR: 150.4, 136.7, 130.6, 129.1, 116.64, 71.8, 70.7, 70.6, 70.5, 70.4, 69.7, 69.1, 59.0; FT-IR (KBr pellet, cm-1): 2885 (C-H), 1487 (C=C), 1108 (C-O-C). Anal Calcd for C30H44O10: C, 63.81%, H, 7.85% Found: C, 60.8%; H, 8.05%.
DCP(Diethylene Glycol-Conjugated Polymer)의 중합. 100 mL 3구 플라스크에 M2(0.346 g, 0.90 mmol)와 1,4-benzenediboronic acid bis(pinacol)ester(0.330 g, 1.0 mmol)를 THF와 톨루엔 혼합 용매(10 mL)에 녹인 후, 2 M K2CO3 수용액(5 mL)과 aliquot 336을 첨가하여 아르곤 가스 하에서 이 혼합물을 70 ℃에서 40시간 동안 교반시켜 반응하였다. 회수과정은 TCP와 동일하다(0.19 g, 71%). 1H NMR: 7.68 (s, 4H), 7.09 (s, 2H), 4.16 (m, 4H), 3.95-3.42 (m, 20H), 3.39 (s, 3H), 3.35 (s, 3H), 13C NMR: 150.4, 129.1, 116.7, 71.9, 70.7, 69.8, 69.2, 59.0; FTIR (KBr pellet, cm-1): 2887 (C-H), 1485 (C=C), 1109 (C-O-C). Anal Calcd for C22H28O6: C, 68.02%; H, 7.27%; O, 24.71%. Found: C, 60.3%; H, 6.4%.
OCP(Octyl-Conjugated Polymer)의 중합. 100 mL 3구 플라스크에 M3(0.448 g, 0.91 mmol)과 1,4-benzenediboronic acid bis(pinacol)ester(0.330 g, 1.0 mmol)를 THF와 톨루엔 혼합 용매(10 mL)에 녹인 후, 2 M K2CO3 수용액(5 mL)과 aliquot 336을 첨가하여 아르곤 가스 하에서 이 혼합물을 70 ℃에서 40시간 동안 교반시켜 반응하였다. 회수과정은 TCP와 동일하다(수율 0.23 g, 38%). 1H NMR: 7.71 (s, 4H), 7.10 (s, 2H), 3.99 (m, 4H), 1.75 (m, 4H), 1.41 (m, 20H), 0.88 (s, 3H) 13C NMR: 150.4, 129.1, 116.7, 71.9, 70.7, 69.8, 69.2, 59.0; FTIR (KBr pellet, cm-1): 2852 (C-H), 1469 (C=C), 1209 (aromatic C-H). Anal Calcd for C30H46O2: C, 82.14%; H, 10.57%. Found: C, 78.72%; H, 6.76%.
TCP-GO의 제조.40 클로로포름(2 mL)에 TCP(0.8 mg)를 녹인 용액을 GO(0.6 mg)가 분산된 증류수(10 mL)에 첨가했다. Tip sonicatior를 이용하여 두 용액을 50분 동안 혼합시킨 후, 원심분리기를 이용해서 14000 rpm에서 15분 동안 침전물을 원심분리하여 회수하였다. 증류수와 에탄올을 사용하여 수세하고 원심분리 과정을 3번 반복하여 침전물을 회수하고, 회수한 침전물은 증류수에 재분산하여 보관하였다.
세슘 이온 감지 실험. TCP-GO 용액(3 mL, 에탄올:물=3:7)에 6×10-4 M의 다양한 금속이온 용액(K+, Na+, Cs+, Zn2+, Cu2+, Co2+, Sr2+)을 첨가하여 TCP-GO의 형광변화를 관찰하였다. 세슘 이온은 최대 3×10-3 M까지 농도를 변화시키며 TCP-GO 용액에 첨가하여 형광변화를 관찰하여 민감도 실험을 진행하였다. 형광변화 관찰 및 분석은 415 nm의 형광파장에서 확인하였으며, 모든 형광 분석은 석영 셀에서 측정하였다.
CPs는 스즈키 커플링 반응을 이용하여 곁사슬 길이가 다른 3종류의 구조로 중합하였으며, TCP, DCP, OCP는 단량체인 M1, M2, M3를 각각 이용하였다. M1, M2, M3은 각각의 곁사슬 구조를 다르게 설계하였으며, 각각의 CP는 2 M K2CO3 용액과 팔라듐 촉매를 첨가하여 반응 후, 메탄올에 침전시키고 메탄올, 아세톤 세척을 거쳐 건조하였다(Scheme 1). TCP 곁사슬의 반복단위를 구성하는 M1은 테트라 에틸렌 글라이콜(tetraethylene glycol)을 포함한 구조이며, DCP의 M2는 다이에틸렌 글라이콜(diethylene glycol)을 마지막으로 OCP의 M3은 옥틸기(octyl group)를 가지고 있는 단량체이다. 이처럼 곁사슬 구조가 각기 다른 3종류 CP를 설계하여 중합한 이유는 곁사슬가 세슘 이온과 결합에 미치는 영향을 확인하기 위함이며, 세슘 이온에 가장 민감한 TCP를 이용하여 형광 센서 연구를 진행하였다. 각 CP는 원소분석, FTIR, NMR 분광기를 이용하여 화학 구조를 분석하였으며, UV, 형광 분광기를 이용하여 광학 특성을 분석하였다. GPC를 이용하여 각 CP의 수평균 분자량(Mn)을 분석한 결과, TCP는 1.46×104, DCP는 1.41×104, OCP는 3.50×104이었다.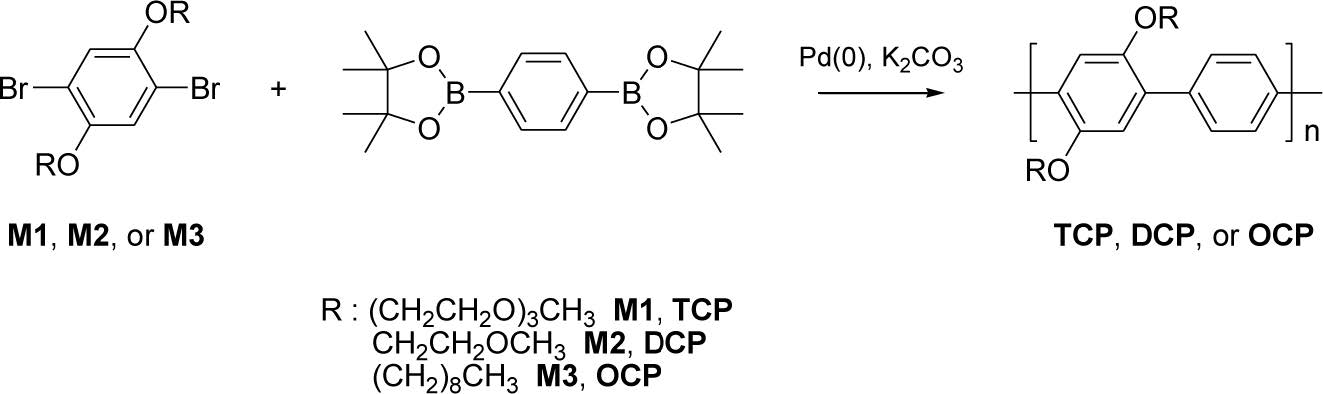
Scheme 1. Synthesis of CPs.
세 종류의 CP 모두 클로로폼에 잘 녹는 특성이 있기 때문에 TCP, OCP, DCP의 UV와 형광 스펙트럼을 클로로폼에 녹여 측정한 결과를 Figure 1에 나타냈다. 형광 스펙트럼에서 TCP는 417 nm, DCP는 410 nm, OCP는 430 nm에서 최대 형광파장을 가져 청색 발광을 갖고 있으며, 세가지 CP가 광학적 특성이 매우 유사하였다. 유사한 형광 파장을 보이는 이유는 3종류의 CP가 곁사슬 길이와 화학적 구조가 각기 다르지만, 주사슬이 페닐렌기로 이루어진 CP이기 때문에 PL 스펙트럼뿐만 아니라 UV 스펙트럼도 유사하였다. 이 3종류의 CP 중에서 세슘 이온과 결합할 수 있는 곁사슬을 가진 TCP를 이용하여 세슘 이온 감지 실험을 진행하였다.
세슘 이온 감지에 사용할 TCP-GO 복합체 제조에 사용되는 GO를 XPS와 SEM을 이용하여 분석하고 TCP-GO 복합체는 FTIR을 이용하여 분석을 하였다. XPS를 이용하여 분석한 결과, GO에 존재하는 C 1s 피크와 O 1s 피크를 284.5와 533 eV에서 확인하였으며(Figure 2(a)), SEM 이미지로 GO 특성인 판상 형태를 확인하였으며, 크기는 1-2 µm이었다(Figure 2(b)). TCP는 유기용매에 쉽게 용해되고 GO는 물에 분산이 잘 되기 때문에, 성질이 다른 두 용매를 두 물질 혼합에 사용해야 한다. 상이한 용매에 각각 존재하는 TCO와 GO를 혼합하면 용매간 층분리가 나타나기 때문에 tip sonication으로 강하게 교반하며 소수성 작용을 이용하여 TCP를 GO 표면에 도입하였다. DCP나 OCP도 동일한 방법을 이용하여 GO 표면에 도입하는 실험을 진행하였다. 제조된 TCP-GO 복합체는 FTIR을 이용해 각각의 IR 흡수밴드를 확인하여 TCP-GO 제조가 완성된 것을 확인하였다. GO는 판상 표면에 카보닐 그룹(C=O)과 카복실산 그룹(COOH)을 가지고 있어서 1687과 1229 cm-1에서 IR 밴드를 확인하였고, TCP는 C-H와 C-O-C의 IR 밴드를 2885와 1108 cm-1에서 확인하였다. TCP-GO 복합체는 TCP와 GO의 IR 밴드를 모두 가지고 있기 때문에, 이 분석을 바탕으로 복합체가 형성된 것을 확인하였다(Figure 2(c)).
세슘 이온 감지는 GO와 방향족기간 약한 결합 중 하나인 소수성 결합을 이용하여 복합체를 만든 후, 이 약한 결합으로 구성된 TCP-GO 복합체를 세슘 이온으로 각각 분리하는 것이 세슘 이온 감지 메커니즘의 핵심이다(Scheme 2). GO는 가시광 영역의 대부분 파장을 흡수하는 특성이 있어서 인접 분자의 형광을 흡수하는 물질로 잘 알려져있다.36 따라서 TCP-GO 복합체가 형성되면 GO의 존재로 TCP의 형광이 사라진 무형광 TCP-GO 복합체가 생성되고, 이를 세슘 이온에 노출시키면 TCP의 곁사슬인 TEG기가 세슘 이온과 결합하여 GO와 TCP의 소수성 결합이 자연스럽게 약화되며, GO의 표면에서 TCP가 유리되어 TCP의 원래 형광이 발현되며 세슘 이온을 감지하는 턴-온 센서 역할을 수행한다.
TCP-GO 복합체가 세슘 이온에 노출되어 TCP가 세슘 이온과 결함으로 인해 TCP가 GO의 표면에서 유리되는 것을 SEM으로 관찰하였다. TCP와 복합체 형성하기 전후 GO의 표면이 크게 달라졌으며, 평활한 GO의 표면(Figure 3(a))이 TCP와 복합체를 형성하면서 거칠어졌다(Figure 3(b)). 또한 TCP 도입에 의하여 TCP-GO 복합체의 거친 표면이 세슘 이온 노출 후 다시 평활해졌다. 이는 세슘 이온에 노출 이후에 TCP가 TCP-GO 복합체 상태로 존재하는 것이 아닌, TCP가 GO 표면에서 유리된 상태로 변화함을 GO 표면 형태 변화를 관찰하여 확인하였다.
TCP-GO 복합체에 다양한 금속 이온들을 노출시켜서 TCP-GO 복합체의 세슘 이온에 대한 선택적 감지의 가능성을 보였고, 타금속 이온에 비하여 크게 형광이 증가되었다(Figure 4(a), (b)). TCP-GO 복합체가 세슘 이온에 노출되면 다른 금속이온과는 다르게 형광이 크게 증가하며, 약 450% 정도 형광 강도가 증가하였다. 하지만, 세슘 이온을 제외한 다른 금속 이온들의 경우에는 TCP-GO 복합체가 노출이 되어도 형광이 변하지 않았다. TCP는 강한 청색 형광을 방출하는 광학 특성이 있으며, 이러한 발광은 세슘 이온에 노출된 TCP-GO 복합체가 세슘 이온과 TCP 곁사슬의 상호작용에 의해 TCP-GO간 결합력이 약해져 TCP가 GO의 표면에서 유리되며, 이 때 소광되었던 TCP의 형광이 다시 증가하기 때문이다.
Figure 4에서 확인한 TCP-GO의 선택적인 형광변화는 세슘 이온 감지가 가능한 센서로 역할 수행이 가능하다는 것을 의미하며, TCP의 곁사슬이 중요하게 작용하는 것을 의미한다. 또한 턴-온 센서의 특징인 주변 형광 신호가 약하고 센서와 반응하는 표적 물질에서만 형광 신호가 강하게 나타나는 현상을 이용할 수 있기 때문에, TCP-GO 복합체의 세슘 이온 검출은 UV광에서 형광 변화는 육안으로 쉽게 관측 가능하며, TCP-GO 복합체에 세슘 이온을 노출시킨 시료에서만 강한 청색 형광이 관측되었다(Figure 4(c)). 하지만, 다른 금속 이온에 노출된 시료의 경우에는 형광 변화가 거의 없는 것을 육안으로 확인이 가능하였고, TCP-GO 복합체가 세슘 이온에 선택적으로 감응하고 이는 형광 사진 통해 쉽게 판별된다.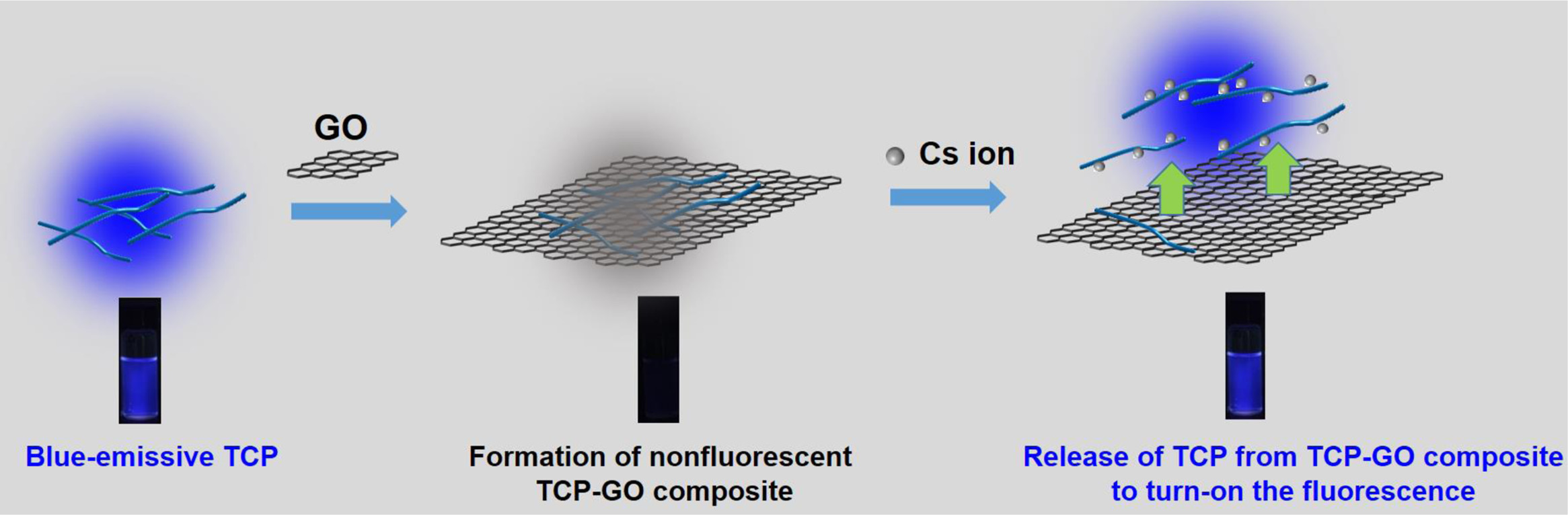
Scheme 2. Schematic illustration of Cs ion sensing mechanism with TCP-GO composite in ethanol-water solution.
TCP-GO 복합체의 세슘 이온 감지 민감도를 형광 증가를 통하여 확인하기 위하여 세슘 이온의 농도에 따른 형광변화실험을 진행하였다(Figure 5). 세슘 이온 농도는 최대 3×10-3 M로 설정하였으며 총 8개의 농도를 설정하여, 이러한 농도의 세슘 이온에 노출된 TCP-GO 복합체의 형광 스펙트럼 변화를 바탕으로 최대 발광 파장에서 형광 변화를 선형 그래프로 변환시켰다. 이러한 선형 그래프로부터 검출한계(limit of detection, LOD)를 분석한 결과 세슘 이온에 대한 TCP-GO의 LOD는 3.8×10-6 M이었다(LOD=3σ/m, σ: 공시료 신호의 표준편차, m: 검량선의 기울기).
TCP-GO 복합체를 사용한 세슘 이온 감지는 TCP 곁사슬에 도입된 TEG기와 세슘 이온과 상호작용에 의해 TCP와 GO간 결합의 약화와 관련된 TCP 형광 증가에 기반한다. 이러한 TEG기와 세슘 이온간 상호작용의 영향을 비교하기 위하여, EG기의 길이가 다른 CP와 알킬기로 이루어진 CP에 대한 세슘 이온과 상호작용에 대하여 조사하였다.
EG 반복단위의 영향을 확인하기 위해 TCP와 다른 반복단위를 갖는, 즉 다이에틸렌 글라이콜기가 도입된 DCP를 합성하였으며, 이는 테트라 에틸렌 글라이콜보다 짧은 반복단위를 가지고 있으며, 이미 보고된 세슘 이온을 결합하는 최소 길이보다 짧은 구조이다.11 EG 반복단위에 있는 산소에 의한 영향을 확인하기 위해 탄소로만 이루어져 있는 옥틸기를 곁사슬에 도입한 OCP를 합성하였다. 각각 중합체는 TCP-GO 제조할 때와 동일한 방식으로 GO를 이용하여 복합체인 DCP-GO, OCP-GO를 제조하였다. 두 복합체를 TCP-GO 복합체에서와 동일한 조건에서 세슘 이온에 대한 선택성 실험을 진행한 결과, 두 복합체 모두 금속 이온의 종류와 상관없이 형광 변화가 나타나지 않았다(Figure 6).
결국 EG 반복단위를 이용하여 세슘 이온을 감지하기 위하여 EG의 길이 조절에 따른 특정 결합이 존재하여야 한다. 이를 바탕으로, 세슘 이온을 감지하기 위해서는 TCP에 도입된 TEG 곁사슬의 길이가 가장 적합하였다.

|
Figure 1 Absorption (solid) and emission spectra (dotted) of TCP (■), DCP (●) and OCP (▲) in chloroform. |

|
Figure 2 (a) XPS spectrum; (b) SEM image of GO; (c) FTIR spectra of GO, TCP and TCP-GO. |

|
Figure 3 SEM images of (a) GO; (b) TCP-GO; (c) TCP-GO after exposure to Cs ions. |

|
Figure 4 (a) Changes in fluorescence spectra of TCP-GO in H2OEtOH (7:3 v/v) solution in the presence of various metal ions (6×10-4 M); (b) relative fluorescence intensity of TCP (0.64 mg)-GO (0.4 mg) in the presence of various metal ions (6×10-4 M); (c) photographs of TCP-GO in the presence of metal ions under ambient (top) and UV light (365 nm, bottom). |

|
Figure 5 (a) Changes in fluorescence spectra; (b) plot of relative fluorescence intensity of TCP (0.64 mg)-GO (0.4 mg) composite in the presence of various Cs ion concentrations. |

|
Figure 6 Fluorescence intensity of (a) DCP-GO; (b) OCP-GO in the presence of various metal ions (6×10-4 M). CP 0.64 mg; GO 0.4 mg. |
방사성 동위원소 중 하나인 세슘 이온을 감지하기 위해 공액화 고분자 기반 턴-온 형광 센서를 합성하였다. TCP 곁사슬에 도입한 TEG기는 세슘 이온과 상호작용으로 인해 TCP-GO 복합체의 결합을 약화시키고, 이로 인해 TCP가 GO에서 박리되는 결과를 얻었다. 세슘 이온과 우선적인 상호작용에 의한 TCP의 유리로 인하여 GO에 의해 소광되었던 TCP의 강한 청색 형광이 더이상 GO로 에너지 이동이 일어나지 않게 되며 형광이 복원되는 메커니즘에 기반한 턴-온 형광 센서이다. 청색 발광 TCP는 구조적으로 단순하지만 GO와 쉽게 복합체를 형성하고 분리되는 특성 때문에 세슘 이온의 선택적 감지가 가능하였다. 본 연구에서 제조된 복합체의 턴-온 시스템은 세슘 이온에 뛰어난 민감도 및 선택성을 보였다. CP와 GO를 이용한 복합체를 세슘 이온을 감지하기 위한 형광센서로 연구는 아직까지 드물기 때문에, 이러한 시스템을 이용한 형광 센서는 다양한 분야에서 세슘 이온을 감지하기 위한 응용 연구로 활용할 수 있다.
- 1. K. Hirose, J. Environ. Rad., 111, 13 (2012).
-

- 2. D. Van-Renterghem, R. Cornelis, and R. Vanholder, Anal. Chim. Acta, 257, 1 (1992).
-

- 3. M. Liezers, O. T. Farmer, and M. L. Thomas, J. Radioanal. Nucl. Chem., 282, 309 (2009).
-

- 4. H. Groll, C. Schnurerpatschan, Y. Kuritsyn, and K. Niemax, Spectrochim. Acta B, 49, 1463 (1994).
-

- 5. P. S. Ramanjaneyulu, A. N. Kumar, Y. S. Sayi, K. L. Ramakumar, S. K. Nayak, and S. Chattopadhyay, J. Hazard. Mater., 205, 81 (2012).
-

- 6. H. Vanhoe, C. Vandecasteele, J. Versieck, and R. Dams, Anal. Chem., 61, 1851 (1989).
- 7. B. Radaram, T. Mako, and M. Levine, Dalton Trans., 42, 16276 (2013).
-

- 8. V. Souchon, I. Leray, and B. Valeur, Chem. Commun., 4224 (2006).
-

- 9. Y. Inokuchi, O. V. Boyarkin, R. Kusaka, T. Haino, T. Ebata, and T. R. Rizzo, J. Phys. Chem. A, 116, 4057 (2012).
-

- 10. A. Depauw, N. Kumar, M.-H. Ha-Thi, and I. Leray, J. Phys. Chem. A, 119, 6065 (2015).
-

- 11. T. Terashima, M. Kawabe, Y. Miyabara, H. Yoda, and M. Sawamoto, Nat. Commun., 4, 2321 (2013).
-

- 12. S. Yoshida, Y. Hazama, Y. Sumida, T. Yano, and T. Hosoya, Molecules, 20, 10131 (2015).
-

- 13. N. Kumar, Q. Pham-Xuan, A. Depauw, M. Hemadi, N.-T. Ha-Duong, J.-P. Lefevre, M.-H. Ha-Thi, and I. Leray, New J. Chem., 41, 7162 (2017).
-

- 14. S. H. Jung, T. K. Hyun, J.-Y. Kim, and J. H. Jung, RSC Adv., 5, 26662 (2015).
-

- 15. A. Facchetti, Chem. Mater., 23, 733 (2011).
-

- 16. D. Kim, J. Kim, and T. S. Lee, Sens. Actuat. B: Chem., 264, 45 (2018).
-

- 17. D. T. McQuade, A. E. Pullen, and T. M. Swager, Chem. Rev., 100, 2537 (2000).
-

- 18. M. H. Lee, J. S. Kim, and J. L. Sessler, Chem. Soc. Rev., 44, 4185 (2015).
-

- 19. E. M. Nolan and S. J. Lippard, Acc. Chem. Res., 42, 193 (2009).
-

- 20. J. J. Gruskos, G. Zhang, and D. Buccella, J. Am. Chem. Soc., 138, 14639 (2016).
-

- 21. Y. Qu, X. Zhang, Y. Wu, F. Li, and J. Hua, Polym. Chem., 5, 3396 (2014).
-

- 22. F. Li, F. Meng, Y. Wang, C. Zhu, and Y. Cheng, Tetrahedron, 71, 1700 (2015).
-

- 23. C.-G. Qian, S. Zhu, P.-J. Feng, Y.-L. Chen, J.-C. Yu, X. Tang, Y. Liu, and Q.-D. Shen, ACS Appl. Mater. Interfaces, 7, 18581 (2015).
-

- 24. F. Lv, X. Feng, H. Tang, L. Liu, Q. Yang, and S. Wang, Adv. Funct. Mater., 21, 845 (2011).
-

- 25. H. Namgung, J. J. Lee, Y. J. Gwon, and T. S. Lee, RSC Adv., 8, 34291 (2018).
-

- 26. M. Zhu, Y. Zhou, L. Yang, L Li, D. Qi, M. Bai, Y. Chen, H. Du, and Y. Bian, Inorg. Chem., 53, 12186 (2014).
-

- 27. L. Dong, Q. Miao, Z. Hai, Y. Yuan, and G. Liang, Anal. Chem., 87, 6475 (2015).
-

- 28. A. N. Swinburne, M. J. Paterson, A. Beeby, and J. W. Steed, Org. Biomol. Chem., 8, 1010 (2010).
-

- 29. H. Namgung, Y. J. Gwon, J. Kim, G. Jang, S. E. Pepper, M. D. Ogden, K. R. Whittle, L. M. Harwood, and T. S. Lee, Polymer, 158, 320 (2018).
-

- 30. H. Yuan, J. Qi, C. Xing, H. An, R. Niu, Y. Zhan, Y. Fan, W. Yan, R. Li, B. Wang, and S. Wang, Adv. Funct. Mater., 25, 4412 (2015).
-

- 31. T. Feng, D. Feng, W. Shi, X. Li, and H. Ma, Mol. BioSyst., 8, 1441 (2012).
-

- 32. J. Noh, B.-J. Chae, B.-C. Ku, and T. S. Lee, J. Polym. Sci., Part A: Polym. Chem., 52, 1898 (2014).
-

- 33. S. K. Lim, P. Chen, F. L. Lee, S. Moochhala, and B. Liedberg, Anal. Chem., 87, 9408 (2015).
-

- 34. S. K. Bhunia and N. R. Jana, ACS Appl. Mater. Interfaces, 3, 3335 (2011).
-

- 35. C.-H. Lu, H.-H. Yang, C.-L. Zhu, X. Chen, and G.-N. Chen, Angew. Chem. Int. Ed., 48, 4785 (2009).
-

- 36. J. Kim, S.-J. Park, and D.-H. Min, Anal. Chem., 89, 232 (2017).
-

- 37. W. S. Hummers and R. E. Offeman, J. Am. Chem. Soc., 80, 1339 (1958).
-

- 38. U. Lauter, W. H. Meyer, and G. Wegner, Macromolecules, 30, 2092 (1997).
-

- 39. R. M. Pankow, N. S. Gobalasingham, J. D. Munteanu, and B. C. Thompson, J. Polym. Sci., Part A: Polym. Chem., 55, 3370 (2017).
-

- 40. D. Y. Yoo, N. D. K. Tu, S. J. Lee, E. Lee, S.-R. Jeon, S. Hwang, H. S. Lim, J. K. Kim, B. K. Ju, H. Kim, and J. A. Lim, ACS Nano, 8, 4248 (2014).
-

- Polymer(Korea) 폴리머
- Frequency : Bimonthly(odd)
ISSN 0379-153X(Print)
ISSN 2234-8077(Online)
Abbr. Polym. Korea - 2023 Impact Factor : 0.4
- Indexed in SCIE
 This Article
This Article
-
2019; 43(2): 302-308
Published online Mar 25, 2019
- 10.7317/pk.2019.43.2.302
- Received on Dec 18, 2018
- Revised on Jan 14, 2019
- Accepted on Jan 15, 2019
 Services
Services
Shared
 Correspondence to
Correspondence to
- Taek Seung Lee
-
Organic and Optoelectronic Materials Laboratory, Department of Advanced Organic Materials and Textile System Engineering, Chungnam National University, Daejeon 34134, Korea
- E-mail: tslee@cnu.ac.kr
- ORCID:
0000-0002-3943-1145









 Copyright(c) The Polymer Society of Korea. All right reserved.
Copyright(c) The Polymer Society of Korea. All right reserved.